
27 Билет
Гальванический Элемент -это устройство, предназначенное для преобразования хим.энергии ОВР в электрическую. Простейшим элементом яв-ся элемент Вольта. Он хар-ся тем, что 2 электрода находятся в общем электролите. Схему ГЭ можно записать след.образом:
(-)А, Zn|H2SO4|Cu,K(+)
A(-)Zn-2e→Zn(2+)
K(+)2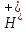 +2e→H2↑
+2e→H2↑
Zn+2H+→Zn(2+)+H2↑
Zn+H2SO4→ZnSO4+H2↑
Главное отличие Даниэля-Якоби состоит
в том, что электроды опущены в растворы
своих солей, поэтому при работе такого
ГЭ на аноде(А) протекает ок-ие металла
электрода, а на катоде(К) происходит
вос-ие катионов металла электролита из
катодного пространства. При работе ГЭ
на каждом электроде возникает собственный
электродный потенциал. Разность этих
электродных потенциалов н-ся электродвижущей
силой работы ГЭ (ЭДС). ЭДС= ϕ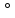 кат-
ϕ
кат-
ϕ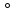 ан(для
элемента Даниэля-Якоби). ϕ кат всегда
больше ϕан. Эдс всегда величина
положительная.
ан(для
элемента Даниэля-Якоби). ϕ кат всегда
больше ϕан. Эдс всегда величина
положительная.
Элемент Даниэля
Работа гальванических элементов основана на пространственном разделении процессов приема и отдачи электронов. Рассмотрим один из наиболее старых гальванических элементов - элемент Даниэля. Он состоит из цинкового электрода, погруженного в раствор сернокислого цинка, и медного, погруженного в раствор сернокислой меди. Оба раствора разделены цилиндром из пористого материала. Схематически конструкцию этого элемента можно представить следующим образом;
(-)Znl ZnSCU - раствор | CuSO4 - раствор! Си(+)
Действие элемента Даниэля основано на том, что с поверхности цинка в раствор переходят ионы цинка Zn2+; при этом по проводнику, соединяющему цинк и медь, электроны от цинка перетекают к меди, где они взаимодействуют с ионами меди (Си2+), находящимися в соприкосновении с поверхностью меди, и нейтрализуют их. Цинк представляет собой отрицательный электрод элемента, медь - положительный. Элемент Даниэля представляет собой прибор, который непосредственно (минуя фазу тепла), теоретически полностью, превращает освобождающуюся химическую энергию в электрическую в соответствии с реакцией
ЭДС всякого работающего элемента является величиной существенно положительной. ЭДС гальванического элемента, т.е. наибольшая разность потенциалов между электродами его равна алгебраической сумме отдельных разностей (скачков) потенциала, существующих на поверхностях раздела между различными фазами, образующими данный элемент.
Итак, при работе элемента Якоби-Даниэля протекают следующие процессы:
1) реакция окисления цинка: Zn - 2е ® Zn2+.
Процессы окисления в электрохимии получили название анодных процессов, а электроды, на которых идут
процессы окисления, называют анодами;
2) реакция восстановления ионов меди: Сu2+ + 2е « Сu.
Элемент Вольта
Он состоит из медной (Сu) и цинковой (Zn) пластинок, опущенных в раствор серной кислоты (H2SO4). Вследствие химической реакции, происходящей между цинком и серной кислотой, на цинке образуется излишек электронов. Цинк заряжается отрицательно и является отрицательным полюсом. Раствор и медная пластинка, в него погруженная, заряжаются положительно. В результате возбуждается ЭДС, равная примерно одному вольту, которая сохраняется все время, пока цепь не замкнута.
