
Лекции / organic_2011_5
.pdf
O |
O |
O |
|
NEt , t |
H2O |
|
3 |
|
|
|
Fe3+ (Cu2+) |
или |
Br |
OH |
|
N |
|
Возможные направления нуклеофильной атаки
|
?2 |
|
O |
|
SN2 замещение |
|
H |
|
H |
Е2 элиминирование |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
?1 |
|
Br |
|
|
O |
|
- |
|
Nu O- |
|
Nu- Nu |
O |
- Br- Nu O |
||
|
|
- Nu- |
|||
?1 |
Br |
Br |
SN2 |
SN2 |
|
Nu- |
Nu |
||||
Высокая нуклеофильная подвижность галогена в α-галоидкетонах!
81
O
O
O
Nu

82
O
Cl
Ph
фенацилхлорид "черемуха"
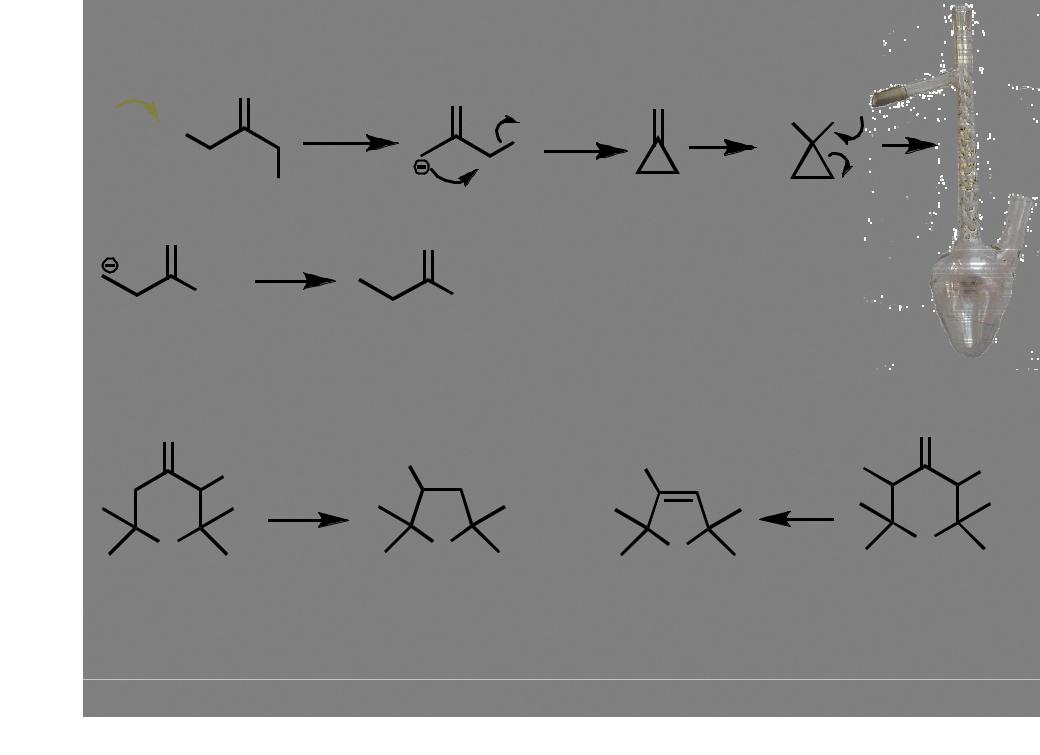
Перегруппировка Фаворского |
|
|
|
|||
?2 |
|
O |
O |
|
O |
Nu O- |
|
Nu- |
|
||||
H |
|
Br |
Nu- |
|||
|
|
- NuH |
|
- Br- |
|
|
|
|
|
|
|
||
|
|
Br |
|
|
|
|
|
O |
NuH |
O |
|
|
|
|
|
|
нуклеофил - сильное основание |
|||
|
Nu |
- Nu- |
Nu |
|||
|
|
|
|
|||
Примеры:
O |
H2NOC |
H NOC |
|
|
Br |
Br |
|||
|
2 |
|||
|
NH3 |
|
NH3 |
|
N |
|
N |
N |
|
H |
|
H |
H |
83
O
Br
N
H

NC |
O |
84 |
|
O |
H3CO2C |
|
|
Br |
|
CN- |
CH3O- |
N |
N |
N |
O |
O |
O |
α,β-Ненасыщенные карбонильные соединения
Методы синтеза
Окисление алкенов, аллилгалогенидов, аллиловых спиртов
|
O |
OH |
MnO2/H2O |
|
MnO2 |
(SeO ) |
|
(CH3COCH3/Al(OR)3) |
2 |
|
|
[O]
Br |
[O] = DMSO, (CH3)2CHNO2/OH- |
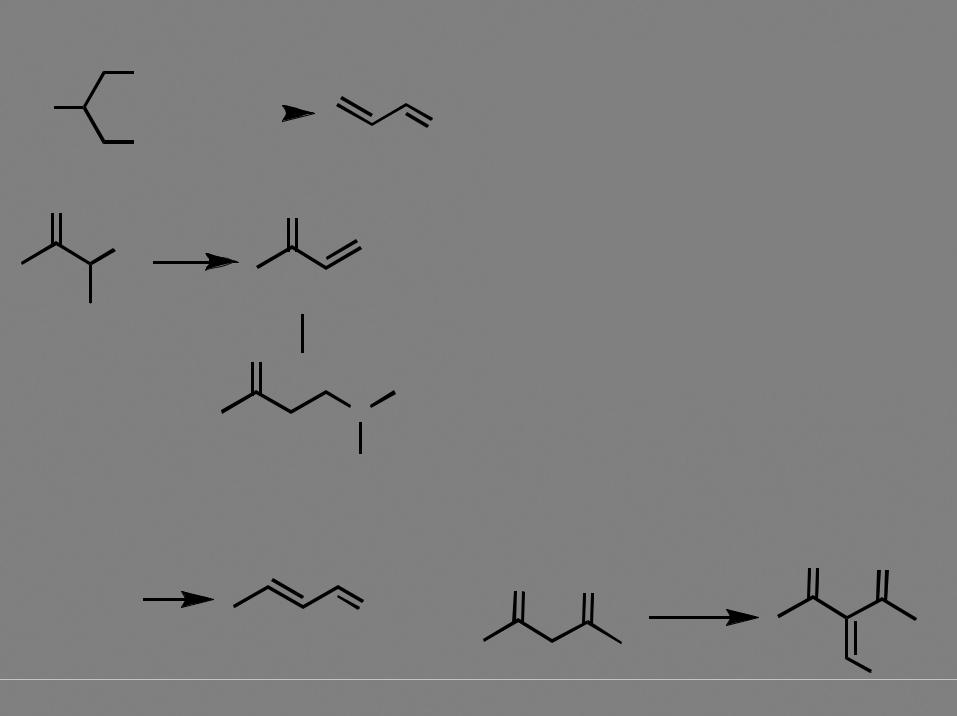
Реакции элиминирования |
85 |
||||||
|
|||||||
HO |
|
|
|
OH |
KHSO4 |
|
O |
|
|
|
|
||||
|
|
|
|
|
|||
|
|
|
|||||
|
|
|
OH |
t |
|||
|
|
|
|
||||
|
|
|
|
|
|
акролеин |
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|||
Br NEt3
t
1. CH3I  2. Ag2O/H2O, t O
2. Ag2O/H2O, t O
N
основание Манниха
Реакции конденсации кротонового типа
O O
2CH3CHO |
H+ |
O |
O |
|
O |
RCHO |
|
|
|
NEt3 |
|
|
|
|
R

Свойства |
|
|
|
|
86 |
Электронное строение |
|
|
|
|
|
MO бутадиена |
|
MO гетеродиена |
|
||
|
|
|
|
O |
|
|
π2* |
|
π2* |
|
|
π* |
|
|
π* |
π* |
π* |
|
π |
1 |
|
π1 |
|
|
|
|
* |
|
|
π |
π2* |
π |
|
|
|
π1 |
π2 |
|
|||
|
|
|
|||
|
|
π |
π |
||
|
|
|
|
||
этен |
|
этен |
π1 |
||
|
|
O |
|||
|
|
|
|
|
|
Возможность n−π перехода обуславливает наличие интенсивного поглощения в |
|||||
УФ-области. |
|
|
|
|
|
Сопряжение с карбонильной группой заметно смещает положение полосы поглощения ее валентных колебаний: ацетальдегид – 1720 см-1, акролеин – 1695 см-1 (уменьшение порядка связи С=О)

|
α |
O |
|
87 |
|
O |
O |
||
β |
|
Возникновение частичного положительного заряда на β-углеродном атоме
Протоны у β-углеродного атома находятся
в более слабом поле (спектр ЯМР 1Н коричного альдегида)

88
Взаимодействие с нуклеофильными реагентами
|
O |
|
|
O |
|
OH |
|
|
|
|
|
|
|
|
|
α |
O |
Nu- |
Nu |
|
Nu |
|
|
или |
|
1,2-присоединение |
|
||||
β |
|
|
|
|
|
|
|
|
O |
|
Nu |
|
O |
Nu |
O |
|
|
|
|
|
|
1,4-присоединение |
|
Кислый катализ нуклеофильного присоединения |
|
|
|
||||
|
|
OH |
|
|
OH |
|
|
|
|
|
|
|
1,2-присоединение |
|
|
|
|
|
|
|
|
|
|
α |
OH |
|
Nu- |
Nu |
|
|
|
|
или |
|
|
|
|||
β |
|
|
|
|
|
|
|
|
|
OH |
Nu |
|
|
OH |
|
|
|
|
|
|
|
1,4-присоединение |
|
В том случае, когда первоначально происходит присоединение 1,2, дальнейшее нуклеофильное присоединение по связи С=С невозможно – отсутствует активация сопряжением с акцепторным заместителем!

Взаимодействие α,β-ненасыщенных карбонильных соединений |
89 |
|||||
|
|
|||||
с нуклеофильными реагентами |
|
|
|
|
||
|
|
|
|
|
|
|
|
реагент |
альдегиды |
кетоны |
примечания |
|
|
|
|
|
|
|
|
|
|
H2/катализатор |
С=С > C=O |
C=C |
|
|
|
|
|
|
|
|
|
|
|
NaBH4 |
C=O |
C=O |
|
|
|
|
|
|
|
|
|
|
|
LiAlH4 |
C=O, C=C |
C=O, C=C |
Не селективно, |
|
|
|
|
|
|
преимущественно С=О |
|
|
|
|
|
|
(либо и С=С, и С=О) |
|
|
|
|
|
|
|
|
|
|
Na/Hg/H+ |
C=C, затем С=О |
C=C, затем С=О |
Возможно дальнейшее |
|
|
|
|
восстановление в пинакон |
|
|
||
|
|
|
|
|
|
|
|
ROH |
C=O |
C=O |
При взаимодействии с |
|
|
|
|
(в кислой среде) |
(основный |
этиленгликолем |
|
|
|
|
|
катализ) |
образуются диоксаланы (по |
|
|
|
|
|
|
С=О), кислый катализ |
|
|
|
|
|
|
|
|
|
|
H3O+ |
C=C |
C=C |
|
|
|
|
|
|
|
|
|
|
|
CH3COCH3/ |
C=O |
C=O |
|
|
|
|
Al(OR)3 |
|
|
|
|
|

90
реагент |
альдегиды |
кетоны |
примечания |
|
|
|
|
NaHSO3 |
C=O |
C=C, затем С=О |
|
|
|
|
|
амины |
C=O |
C=C |
|
|
|
|
|
гидразин |
C=O, C=C |
C=C, C=O |
|
|
|
|
|
гидроксиламин |
C=O |
C=C |
В кетонах – сначала по С=С, |
|
|
|
затем замыкание цикла (по |
|
|
|
С=О) |
HCN |
C=O |
C=C |
|
|
|
|
|
RMgX |
C=O |
C=C, C=O |
Для кетонов обычно смесь |
|
|
|
продуктов |
RMgX/Cu+ |
C=C |
C=C |
|
или |
|
|
|
R2CuLi |
|
|
|
RLi |
C=O |
C=O |
|
|
|
|
|
карбанионы |
C=C |
C=C |
Присоединение по |
|
|
|
Михаэлю |
