
Лекции / organic_2011_5
.pdf
CH3CHO
HO
O
H+ |
H+ |
H3C |
O |
кротоновый альдегид может выступать в качестве метиленовой компоненты
 OH
OH
CH2 |
HO |
O |
O |
41 |
|
H3C  OH
OH
- H+
H3C |
OH |
|
|
OH |
|
C |
- H+ O |
C |
H |
||
H2 |
|
|
 Y X n
Y X n
реакционная способность группы Х, определяющаяся сопряжением с группой У мало зависит от n, где n может быть равно и 0
(правило винилогии)
Кневенагель |
пиперидин, |
|
|
|
R |
X |
R |
X |
|
O |
+ |
триэтиламин |
|
|
|
|
|
||
R |
Y |
|
R |
Y |
X, Y - сильные акцепторы по мезомерному эффекту - СOR, CO2R, CN, NO2 в качестве катализатора используется слабое (органическое) основание реакция всегда сопровождается дегидратацией
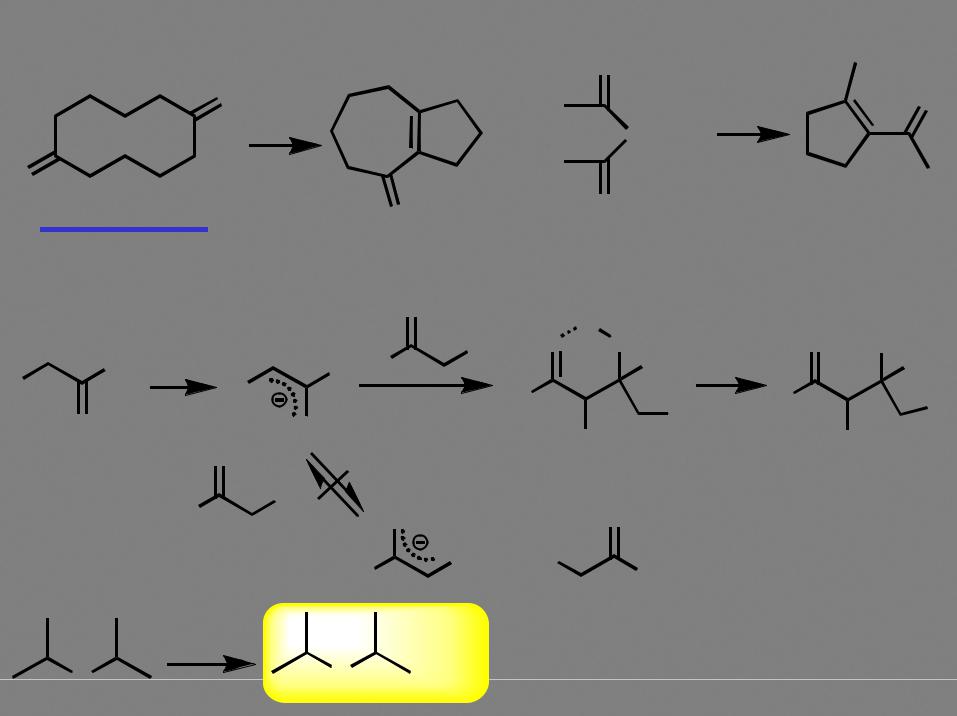
Очень легко протекают реакции внутримолекулярной конденсации |
|
42 |
|||||||
с замыканием 5- или 6-членного цикла: |
|
O |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
HO- |
|
O |
|
|
HO- |
|
|
|
(CH2)4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Использование сильных оснований позволяет проводить перекрестную конденсацию |
|||||||||
с минимальным количеством побочных продуктов |
|
|
|
|
|||||
|
|
|
O |
|
|
Li |
|
|
|
|
|
|
|
R2 |
O |
|
O |
OH |
|
R1 |
|
R1 |
R3 |
O |
H2O |
||||
LDA |
|
|
R3 |
|
R3 |
||||
R |
- 78o |
R |
|
|
R1 |
R2 |
R1 |
|
R2 |
O |
OH |
|
|
|
|||||
|
|
|
|
R |
|
|
R |
||
|
|
O |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
R3 |
R2 |
O |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|||
|
|
R3 |
R2 |
+ R |
R1 |
|
|
|
|
|
|
|
|
|
|
|
|||
|
PhLi |
|
|
|
|
|
|
|
|
N |
|
N |
|
LDA |
|
|
|
|
|
H |
|
Li |
|
|
|
|
|
|
|

Использование силиловых эфиров |
|
|
|
43 |
|||||||||
|
|
|
|
|
|
||||||||
|
|
O |
o |
OSi(CH3)3 |
|
|
|
O |
|||||
|
|
|
|
|
|
|
|||||||
|
|
|
1. LDA, - 78 |
|
|
|
|
RCH CHO |
|
|
|
||
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
2. (CH ) SiCl |
|
|
|
|
TiCl4, -78o |
|
|
R |
||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||||
|
|
|
3 3 |
|
|
|
|
|
2. H2O |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
||
Другие электрофилы |
|
|
|
|
|
|
|||||||
 В обычных условиях (водная щелочь) концентрация карбонильного соединения
В обычных условиях (водная щелочь) концентрация карбонильного соединения  значительно превосходит концентрацию енола (енолят-аниона). Следовательно, в среде присутствует большое количество электрофила - неенолизованного карбонильного соединения, которое конкурирует с другими прибавляемыми электрофилами в случае их сопоставимой реакционной способности.
значительно превосходит концентрацию енола (енолят-аниона). Следовательно, в среде присутствует большое количество электрофила - неенолизованного карбонильного соединения, которое конкурирует с другими прибавляемыми электрофилами в случае их сопоставимой реакционной способности. 
OH O O
Возможные направления электрофильной атаки в случае енола |
|
|
||||||
E+ |
E |
|
E |
OH |
|
OH |
-H+ |
O |
OH |
OH |
-H+ |
O |
|
||||
|
|
|
|
E+ |
E |
|
E |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|

44
Направления реакции электрофила с енолят-анионом:
E+ |
E |
O |
|
O |
O |
O |
|
||
|
|
|
E |
E+ |
|
|
|
|
Эффективность электрофильной атаки определяется либо сильным кулоновским взаимодействием между нуклеофилом и электрофилом (зарядовый контроль), либо эффективным перекрыванием орбиталей (вакантной электрофила и несущей пару электронов – нуклеофила) – орбитальный контроль.
В соответствии с этим, электрофилы, несущие значительный положительный заряд на электрофильном центре (атоме) или имеющие плохо поляризуемую вакантную орбиталь («жесткие электрофилы») взаимодействуют с центром, на котором находится больший по величине отрицательный заряд (неподеленная пара электронов на хорошо поляризуемой орбитали) – «жесткий центр».
Это ситуация зарядового контроля.
«Мягкий электрофил» - и «мягкий нуклеофил» - центры, обладающие, соответственно, вакантную и занятую орбитали, которые способны эффективно поляризоваться при взаимодействии друг с другом с образованием химической связи.
Орбитальный контроль

45
Карбонильный атом углерода – «мягкий электрофил», который взаимодействует с «мягким» нуклеофильным центром – атомом углерода енола или енолят-аниона
(реакции конденсации альдольно-кротонового типа)
O |
OH |
|
COCH3 |
|
|
|
|
O |
|
|
|
R |
|
|
|
|
RCHO |
CH3COCl |
|
|
O |
O |
|
Si(CH3)3 |
|
(CH3)3SiCl |
O |
||
|
|
LDA |
|
CH2
O - жесткийцентр С - мягкий центр
(CH3O)2SO2
CH3I
O 
 O
O

O |
46 |
LDA |
|
|
O |
O- |
O |
CH3I |
|
(CH3O)2SO2 |
SN2 |
|
SN2 |
"мягкий" |
|
"жесткий" |
электрофил |
|
электрофил |
Этилат-анион не обладает достаточной основностью для полного превращения кетона в анион. Поэтому сам кетон выступает в роли электрофила по отношению к енолят-аниону.
O |
EtO- |
O- |
|
O |
|
|
|
+ CH3OEt + |
|
|
|
|
|
|
|
|
H3C |
I |
SN2 |
|
|
|
||
O |
|
O |
|
|
+
OH
продукты самоконденсации

Низкая региоселективность |
|
O |
|
47 |
|
реакции алкилирования |
|
|
|
||
|
|
|
|
||
O |
|
|
O |
O |
|
|
|
|
|||
LDA, -78o |
+ |
30% |
CH3I |
+ |
|
ДМЭ |
OH |
20o |
|||
|
|
||||
|
|
30% |
70% |
||
|
|
|
термодинамический контроль!
70%
кинетический контроль!
Другой способ избежать самоконденсации – превращение карбонильного соединения в енамин.
|
|
|
|
E |
O |
NH |
N |
N |
O |
|
E+ |
|
H3O+ |
|
|
H+ |
|
||
|
енамин |
E |
|
|
|
|
|

N E |
|
|
N |
|
E+ |
|
|
|
|
|
|
||
|
|
|
|
|
E+ |
|
O |
O |
1. RCOCl |
N |
|||
|
|
|||||
|
|
|
||||
|
R |
|
2. H3O+ |
|
||
Реакция нитрозирования |
|
|
|
|
|
|
кислаясреда |
EtOH |
NaNO2 |
EtONO |
|||
H3O+ |
|
|||||
|
|
|
|
|
||
O |
HO |
|
|
O |
|
|
|
|
|
|
|
||
EtOH |
|
|
|
Nδ+ |
Et |
|
NaNO2 |
|
|
|
|||
|
|
|
O |
|
||
H O+ |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
O |
O |
|
|
NOH H3O+ |
||
NO |
|
|
|
|||
|
|
|
|
|
|
t |
48
N N
E  E
E
более устойчивый катион - продукт термодинамического контроля
1. RX (SN2) |
O |
||
|
|
R |
|
2. H3O+ |
|
|
|
|
|
|
|
|
OH O- |
-H+ |
|
|
|
N |
|
|
|
- EtOH |
|
|
|
OEt |
|
|
|
H+ |
|
O |
|
диацетил - |
|
|
|
||
|
O |
по запаху напоминает |
|
|
сливочное масло |
||
|
|
||

щелочная среда |
|
O |
|
|
49 |
O |
O |
O |
O- |
|
|
|
|
||||
RONO |
|
δ+ |
N |
|
|
|
|
-EtO- |
|||
LDA |
|
N |
O Et * |
OEt |
|
O |
O |
|
|
|
|
NO |
|
|
|
|
|
|
NOH |
*реакция сложноэфирной конденсации |
|||
|
|
||||
|
|
|
(типа Кляйзена) |
|
|
Галоидирование
Кислый катализ
O
Br2
H+
HO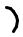
-Br-
Br Br
при катализе кислотами реакция галоидирования  карбонильных соединений является автокаталитической - протоны (галогеноводород)
карбонильных соединений является автокаталитической - протоны (галогеноводород)
являются продуктом реакции
O
Br
-H+ 
OH
Br

Основный катализ
O |
O |
O |
O |
|
Br2 |
||||
|
Br2 |
|
||
|
HO- |
-Br- |
Br3C |
|
HO- O |
O |
Br |
|
|
OH |
|
|||
Br3C |
Br3C |
- CBr3- |
CO2H |
|
|
||||
CO2- + CHBr3 |
реакция галоформногораспада |
|||
|
бромоформ |
|
|
|
Реакция Манниха |
|
O |
||
|
|
|
||
O |
H2N Cl- |
O |
|
|
R |
CH2O (параформ) |
N |
N |
|
|
|
"основание манниха" |
||
|
|
|
||
|
H2N Cl- |
|
|
|
CH2O |
N |
N |
|
|
50
HO-
N
иминиевая соль - электрофил
