
Лекции / organic_2011_5
.pdf
Электронное строение – УФ-спектроскопия. |
11 |
|
O MO гетеробутадиена 

π 




















n
π
С С
С
ЯМР 1Н
O
R CH3 δ 2-2.3 м.д.
π
|
|
|
|
|
|
|
|
n |
Возможность электронного перехода |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
n-π* обеспечивает интенсивное пог- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
π |
лощение с максимумом при 220 нм |
|
|
|
|||||||
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
(e ~ 103) |
С O
O
|
O |
дезэкранирующее |
||
|
|
|
|
|
|
|
|
|
и анизотропное влияние |
|
|
|
|
|
R |
|
|
H |
карбонильной группы |
δ 8-9 м.д.

12
Реакционная способность карбонильной группы
Взаимодействие с электрофилом – образование связи за счет электронов на несвязывающем уровне (неподеленной пары электронов)
|
O |
H+ |
OH |
|
OH |
|
|
|
|||
R |
R' |
R |
R' |
R |
R' |
Связь С=О полярная вследствие большей электроотрицательности атома кислорода, что обеспечивает возможность нуклеофильной атаки по атому углерода
|
O |
|
O |
R |
R' |
R |
R' |
Реакция с нуклеофилом – взаимодействие нижней свободной молекулярной орбиталью – НСМО, возможно вследствие ее несимметричности

орбиталь нуклеофила с |
13 |
неподеленной парой электронов
НСМО |
π |
НСМО |
π |
ВЗМО |
π |
ВЗМО |
π |
|
C=C |
|
C=O |
связывающее взаимодействие |
связывающее взаимодействие |
||
равно антисвязывающему |
больше антисвязывающего |
||
Реакции нуклеофильного присоединения
O |
O H |
_ + HO |
X R |
RXH |
X |
+ H |
|
|
|
R |
|
- H+ основный катализ (увеличение силы нуклеофила) |
|||
O |
RX- |
O X R |
RXH |
HO X R |
|
||||
|
|
|
- RX- |
|

кислотный катализ |
|
|
|
|
|
|
|
|
14 |
||
O |
|
OH |
|
HO |
H |
R - H+ |
HO |
X R H+ |
|
|
|
|
H+ |
δ+ |
RXH |
|
X |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
X R |
|
X |
R |
|
R |
|
|
|
RX |
XR |
|
|
|
X |
RXH |
RHX X R |
- H+ |
|||||
|
|
|
|
|
|
|
|
|
|||
|
|
-H2O |
|
|
|
|
|
|
|
|
|
О-нуклеофилы (вода, спирты)
Реакция гидратации обратима, равновесие, как правило, смещено влево. Альдегиды в большей степени находятся в гидратной форме (атом водорода является акцептором по сравнению с алкилом, стерика – переход от sp2 к sp3-гибридному атому), акцепторные заместители способствуют образованию гидратной формы (увеличение положительного заряда на карбонильном атоме углерода).
|
O |
H3O+ |
|
OH |
H2O HO OH2 |
||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
±
H+
HO OH

O
Cl3C

H
0 %
± H2O
CH2O
O
F3C CF3
15
OH H2O Cl3C
 OH
OH
H 100 %
хлоральгидрат (антисептик для КРС)
|
CH2O |
|
|
|
|
|
HO |
OH |
HO |
O |
OH |
HO |
O n OH |
формалин |
|
|
OH |
параформ |
||
|
|
|
|
HO |
OH |
|
H2O |
HO |
OH |
|
|
||
|
OH |
|
|
|||
|
|
|
|
|
|
|
P2O5, t F3C |
CF3 |
|
|
|
|
|
|
|
|
|
~ 0 % |
~ 50 % |
|
H2SO4
CH2O t
O
O O
триоксан
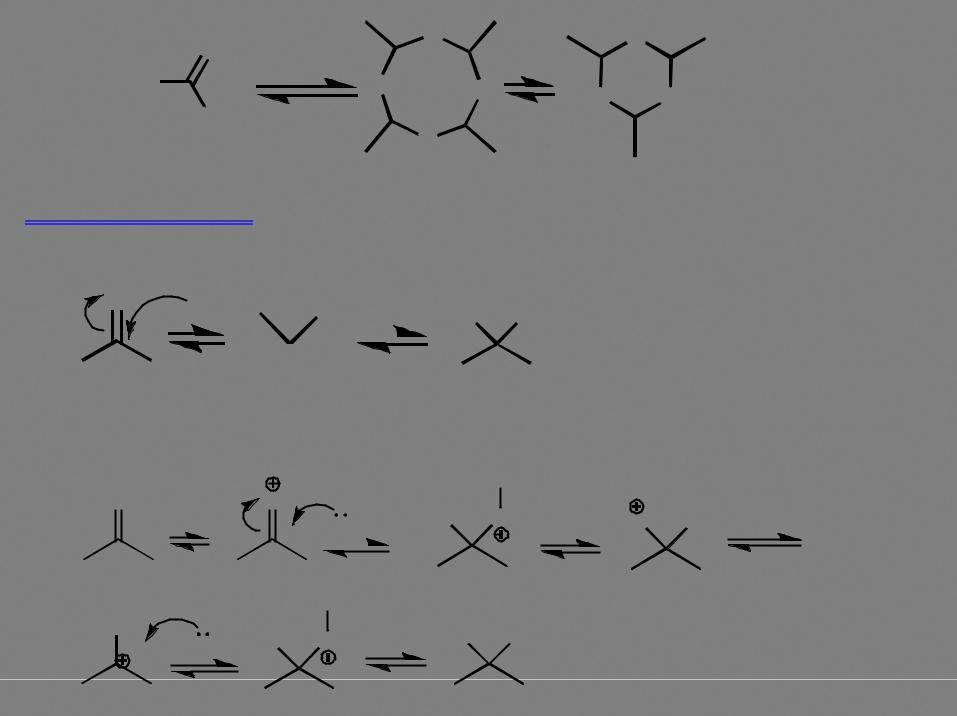
|
O |
|
O |
|
O |
16 |
|
|
|
|
|||
|
|
|
|
|
|
|
H3C |
H2SO4 |
O |
O |
O |
|
|
H |
O |
|
||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
метальдегид |
паральдегид |
|
||
Спирты. Основныйкатализ
O |
RO- |
- |
OR ROH HO OR |
|
O |
ROH  -RO-
-RO-
полуацеталь (дальше реакция не идет!)
Спирты. Кислотный катализ
O |
|
OH |
|
H |
|
|
H+ |
HO |
OR |
±H H2O |
|||
|
ROH |
|||||
OR |
|
H |
|
|
|
|
ROH |
RO OR |
± H+ RO |
OR |
ацеталь |
||
|
|
|
|
|
OR
±
H2O

17
Реакция обратима. Для протекания слева направо необходимо удаление воды, справа налево реакция идет в водном растворе (избыток воды)
|
|
|
|
SH |
|
OH |
|
|
H2 |
Ni |
S |
SH |
|
OH |
O |
|
|
O |
|
||||
|
C |
|
|
H+, -H2O |
H+, -H O |
|
|
R |
R |
EtOH |
S |
|
O |
||
|
|
|
|
|
2 |
||
|
|
|
|
H3O+ |
|
H O+ |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
Hg2+ |
|
|
|
|
H3CO |
OCH3 |
|
O |
|
EtO |
OEt |
|
|
|
|
CH3OH |
CH(OEt)3 |
|
|
|
|
|
|
BF3 |
H+ |
|
|
Ацетали (кетали) устойчивы к действию нуклеофилов, гидролизуются в кислой среде
Полуацетали гидролизуются с образованием карбонильных соединений как в кислой, так и в основной (нуклеофильной) среде
OH |
O |
* |
|
|
O |
* |
|
* OH циклический полуацеталь |
кольчато-цепное таутомерное равновесие (углеводы, мутаротация - изменение величины оптического вращения)
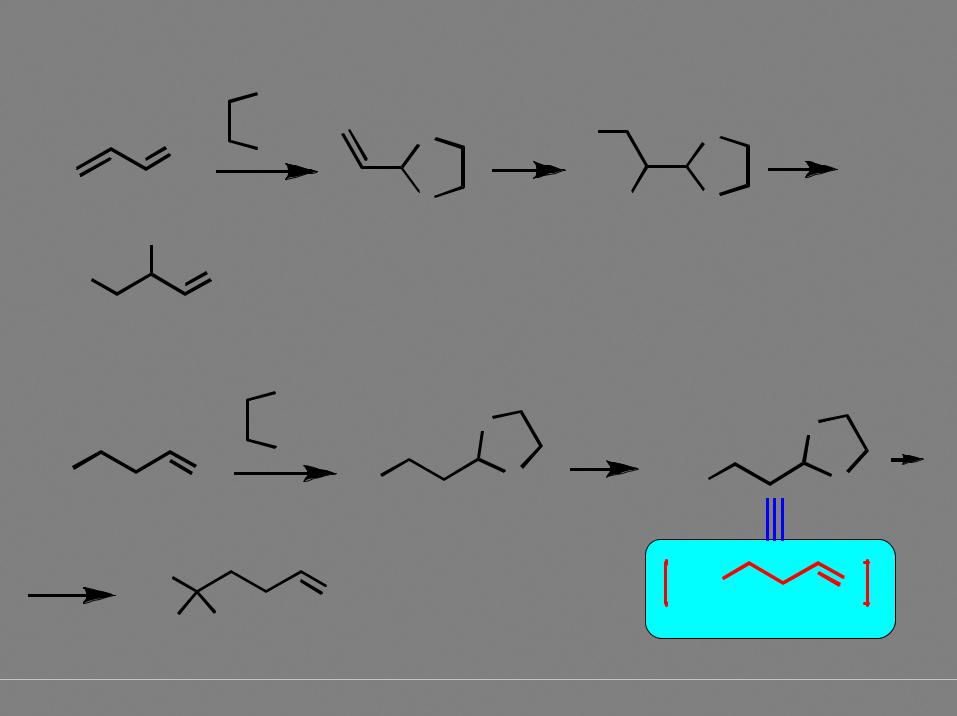
18
Ацеталь как защитная группа |
|
|
|
|
|
|
OH |
|
|
|
|
O |
OH |
O |
MnO4- HO |
O |
H3O+ |
|
H+, -H2O |
O |
HO- |
O |
|
|
|
HO |
|
||
OH
HO
Cl
1.RCOR
2.H3O+
O |
защита устойчива в щелочной среде (к действию нуклеофилов) |
|
OH |
|
|
|
|
|
O |
O |
|
|
OH |
|
Mg |
|
O |
H+, -H O |
Cl |
O эфир ClMg |
O |
|
2 |
|
|
|
HO |
|
O |
ClMg |
O |
|
|
|||
R |
R |
|
|
|
|
не бывает! |
|

19
|
OH |
|
|
|
|
|
|
O |
OH |
|
O |
R |
Li |
R |
H3O+ |
|
|
|
|||||
Br |
H+ |
Br |
O |
|
|
|
O |
|
|
|
O |
||||
|
|
|
|
R
 O
O
S-нуклеофилы
Тиоспирты (меркаптаны) реагируют с карбонильными соединениями аналогично спиртам, например:
|
|
SH |
|
|
R |
O |
SH |
R |
S |
|
|
|
||
|
H+, -H2O R |
|
||
R |
|
S |
||

 SH
SH
SH
O
R R' sp2
CH2O |
S |
1. BuLi |
|
|
|
|
|||
Et2O.BF3 S |
|
Cl |
S |
|
|
|
|
|
|
|
1. BuLi |
2. |
Br |
|
|
2. RX |
|
|
|
|
S |
|
1. BuLi |
|
|
S |
R |
2. R'CHO |
|
|
3. HgCl2/H2O |
|||
|
|
|
||
Cl |
20 |
S |
1. BuLi |
|
O |
|
2. HgCl2/H2O |
OH
O
R'
R
NaHSO3 HO SO3Na
H3O+ |
R' sp3R |
Бисульфитное производное - образуют альдегиды и пространственно незатрудненные кетоны. Растворимо в воде и может быть использовано для отделения альдегидов.
Галогенид-ион - нуклеофил
Cl
O |
HCl (газ) |
OH |
Cl- HO Cl + H+ |
Cl- Cl Cl |
|
||||
|
|
|
|
+ другие продукты |
|
|
|
-H2O |
Cl |
