
- •Белорусский национальный технический университет
- •СОСТОЯНИЕ НАСЫЩЕНИЯ
- •ПРОЦЕСС КИПЕНИЯ
- •Распределение температур при кипении
- •2 ОСНОВНЫХ РЕЖИМА КИПЕНИЯ
- •а) однородно–эмульсионный; б, д) расслоённый;
- •Схема образования пузыря в несмачиваемой впадине на стенке
- •Минимальный радиус пузыря
- •Скорость роста пузыря на поверхности
- •Диаметр и частота отрыва пузырей
- •Кривая кипения при заданных tc , t
- •Кривая и кризисы кипения при заданном q
- •Критическая плотность теплового потока
- •Коэффициент теплоотдачи при кипении
- •Эмпирические формулы для расчета коэффициента
- •Сравнение коэффициентов теплоотдачи при конвекции и фазовых переходах, Вт/(м2К)
- •Переход от св/конвекции к кипению в большом объеме
- •Расчет теплообмена при развитом пузырьковом кипении
- •Безразмерное описание теплообмена при
- •Безразмерное описание теплообмена при пузырьковом кипении (2)
- •Теплоотдача при кипении и вынужденной конвекции


 Белорусский национальный технический университет
Белорусский национальный технический университет
Кафедра ЮНЕСКО “Энергосбережение и возобновляемые источники энергии”
ТЕПЛОПЕРЕДАЧА
Лекция 14. Теплообмен при кипении
Г.И.Пальчёнок

ТП |
Лекция 14 |
Кипение / конденсация, Плавление / затвердевание (замерзание),
Сублимация / десублимация – процессы фазового перехода из одного агрегатного состояния (фазы) в другое.
Правило фаз Гиббса: |
= n – m + 2 |
– число степеней свободы или вариантность – количество независимых параметров состояния,
необходимое для полного описания системы , n – число компонентов смеси,
m – число фаз
Энергосбережение и возобновляемые источники энергии |
Г.И.Пальчёнок |
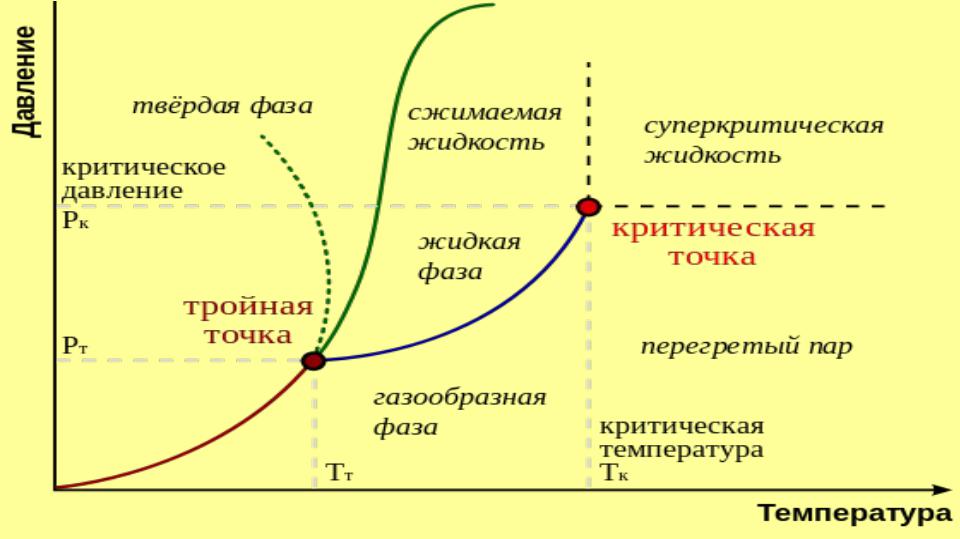
т-к – линия насыщения (вода: tн= 100oC, pн= 1 бар ≈ 1 атм). т – тройная точка (вода: to=0.01oC, po=0.006 бар)
к – критическая точка (вода: to=374oC, po=220.6 бар) – плотности
жидкости и насыщенного пара равны, а поверхностное натяжение жидкости = 0,
исчезает граница раздела фаз жидкость-пар.


СОСТОЯНИЕ НАСЫЩЕНИЯ
Состояние равновесия жидкой и газообразной фаз одного компонента (например, воды), полностью характеризуемое одним параметром состояния (одной степенью свободы) рн или Тн
(или рs или Тs)
Уравнение Клапейрона – Клаузиуса
устанавливает однозначную зависимость темературы от давления на линии насыщения:
dp |
|
|
|
r |
|
|
|
|
|
|
|
T ( |
|
|
|||
dT |
s |
|
|
) |
|

ТП |
Лекция 14 |
При кипении вещество переходит из жидкой фазы
в газообразную (пар), и теплота фазового перехода – скрытая
теплота парообразования – затрачивается на преодоление сил межмолекулярного взаимодействия и работу расширения.
При конденсации пара при тех же условиях выделяется такое же количество теплоты –
скрытая теплота конденсации.
Аналогично – фазовые переходы и теплоты
плавления/затвердевания (твердое-жидкость)
сублимации/десублимации (твердое – газ)

ПРОЦЕСС КИПЕНИЯ
Кипение – процесс образования пара в жидкости или на поверхности, перегретых сверх температуры насыщения при данном давлении.
Величина необходимого перегрева Т = (Т – Тs)
уменьшается при наличии центров парообразования в жидкости (растворенный газ, частицы) и на поверхности (микровпадины, неоднородности, адсорбированный газ и т.п.).
Чистая вода способна как переохлаждаться не замерзая до температуры -33°C, так и быть перегрета до +200°C.
Если вся жидкость значительно перегрета (например, при резком сбросе давления, т.е. снижении Тs), то
паровые пузыри образуются (жидкость вскипает) во всем
объеме.

Распределение температур при кипении

2 ОСНОВНЫХ РЕЖИМА КИПЕНИЯ
Пузырьковое кипение – на начальной стадии кипения на поверхности нагрева возникают отдельные паровые пузырьки, интенсифицирующие теплообмен:
–поверхность имеет прямой контакт с жидкостью, причем пограничный слой турбулизуется и "утоньшается" паровыми пузырями;
–отрывающиеся пузыри увлекают из погран. слоя в ядро потока перегретую жидкость (молярный перенос теплоты).
Пленочное кипение – при увеличении температурного напора на поверхности образуется сплошной слой пара, отделяющий ее от жидкости. Интенсивность теплоотдачи резко снижается.

