- •1.1 Введение, назначение курса, государственный стандарт
- •1.2 Определения и термины для научных методов
- •Логический метод – логически воспроизводится история развития объекта без случайных, несущественных деталей.
- •1.3 Краткая история развития мировоззрения и естествознания на Земле
- •Мировоззрение древних народов, зарождение научных методов, Вклад древнегреческих ученых в начало наук
- •2.1 Мировоззрение древних народов
- •2.2 Древнегреческая натурфилософия
- •Архимедова механика. Наука в эпоху с 1-го по 15-й век. Введение в математику, математика как язык естественных наук Приложения к лекциям м.Ф. Шабанова. Лекция № 3
- •3.1 Архимедова механика
- •Архимедова механика, которой пользовались древние греки и после них до наших дней.
- •3.Правило винта, домкрата.
- •3.3 Введение в математику, математика как язык и основа естественных наук.
- •Аксиомы
- •Введение в физику. Наука о движении кинематика и ее законы. Динамика, законы Ньютона, как основа механистической картины мира. Приложения к лекциям м.Ф. Шабанова. Лекция № 4
- •4.1 Введение в физику
- •4.2 Наука о движении - кинематика и ее законы Обозначения и единицы измерения.
- •Общие законы движения
- •1 Закон. Если на тело не действуют другие тела, оно сохраняет состояние покоя или равномерного прямолинейного движения. Это закон инерции, первый закон Ньютона.
- •Движение тела по окружности.
- •Динамика, обозначения и единицы измерения.
- •При расстоянии между ними - r
- •Приложения к лекциям м.Ф. Шабанова. Лекция № 5
- •5.1 Гидродинамика, стационарное и турбулентное течение, капилляры.
- •Применение уравнения Бернулли:
- •5.2 Колебания. Волны, звук
- •2. Если нечетное π то вычитание
- •3. Сложение колебаний с близкими частотами ω1, ω2
- •Затухающие колебания.
- •Волновой процесс.
- •Звук, звуковые волны
- •Приложения к лекциям м.Ф. Шабанова. Лекция № 6.
- •6.1 Теплофизика и термодинамика
- •Тепловое расширение твердых тел
- •Уравнение теплопроводности Фурье
- •Уравнение переноса или диффузии газа
- •6.2 Основные положения молекулярно-кинетической теории вещества, законы для идеальных и реальных газов
- •6.3 Газовые законы для идеального газа
- •Законы Гей-Люссака 1802 г.
- •Уравнения Клаперона-Менделеева
- •Связь между скорости движения молеку с температурой и давлением газа
- •6.3 Циклы Карно, тепловые машины Работа газа при расширении
- •6.4 Химия наука о веществе, химических реакциях и химических системах.
- •6.5 Органическая химия
- •Электричество, электродинамика. Электромагнитная картина мира Приложение к лекциям Шабанова м.Ф. Лекция № 7.
- •Особенности электромагнитной картины мира.
- •7.1 Электростатика
- •7.2 Электрический ток, электрические цепи
- •7.3 Электромагнитное излучение и его измерение.
- •Спектральные линии
- •7.4 Геометрическая оптика.
- •Световой поток, сила света и освещенность.
- •Основные составляющие мира. Приложение к лекциям Шабанова м.Ф. Лекция № 8. Структурные составляющие мира - микромир, макромир, мегамир.
- •8.1 Основные, фундаментальные составляющие мира
- •Формула (1) отражает рост массы – m от скорости V. Формула отражает зависимость энергии от массы тела. Обозначения в формулах:
- •Энергия
- •8.2 Свойства и значение информации
- •Особенности современной физики. Понятие о строении материи. Приложение к лекциям Шабанова м.Ф. Лекция № 9.
- •9.1 Ученые и развитие науки в хх-ом веке
- •9.2 Законы сохранения в замкнутых системах и законы симметрии
- •Законы симметрии.
- •9.3 Атомная физика ядра атомов и элементарные частицы
- •Астрономическая картина мира Приложение к лекциям Шабанова м.Ф. Лекция № 10.
- •10.1 Астрономические явления, связанные с вращением Земли и ее движением по орбите
- •10.2 Измерения времени, календарь
- •Календарь.
- •10.3 Солнечная система.
- •10.31 Наша звезда Солнце.
- •Основные типы ядерных реакций, их энерговыделение.
- •10. 32 Планеты солнечной системы
- •19.33 Планеты – гиганты – Юпитер, Сатурн, Уран, Нептун.
- •10.4 Образование солнечной системы, космогонические гипотезы.
- •10.5 Образование Вселенной, элементы космологии.
- •Горячая Вселенная.
- •Адронная эра
- •Биология. Основные понятия, классификации, законы биологии. Приложение к лекциям Шабанова м.Ф. Лекция №11
- •11.1 Основные понятия, уровни биосистеми их составляющие
- •11.2 Генетика, генетический код, одноклеточные организмы
- •11.3 Законы биологии и их возможные применения
- •Литература.
- •История Земли. Возникновение и развитие жизни на Земле Приложение к лекциям Шабанова м.Ф. Лекция №12
- •12.1 Образование Земли и ее строение
- •12.2 Происхождение и развитие жизни на Земле
- •12.3 Биологические эры в истории Земли
- •12.4 Происхождение и эволюция человека
- •Литература.
- •Приложение к лекциям Шабанова м.Ф. Лекция №13
- •13.1 Общесистемные законы, правила и свойства для природных, технических, биологических и социально-экономических систем.
- •4. Закон единства и взаимодействия противоположностей. Всякая система содержит взаимодействующие противоположности, и это взаимодействие служит двигателем эволюции.
- •Заключение по системным законам
- •13.2 Особенности системного анализа социально-экономических систем (сэс) и возможности использования компьютеров в подготовке и принятии решений
- •Управление сэс всегда происходит в условиях неопределённости по трем причинам:
- •13.3 Возможности компьютерных методов разработки и принятия решений
- •Литература.
- •14.1 Законы кибернетики в приложении к управлению социально экономическими системами
- •Cинергетика и информационное управление Приложение к лекциям Шабанова м.Ф. Лекция №15
- •15.1 Синергетика и традиционное научное мышление
- •15.2 Информационное управление человеком и общественной системой
- •15.3 Методы информационного управления и информационной войны
- •Литература.
- •16.2 Научные прогнозы будущего, учение в.И. Вернадского о ноосфере.
- •Литература
6.3 Циклы Карно, тепловые машины Работа газа при расширении
|
Р
V
|
dA=р·dv;
А= Работа совершается газом при расширении числено равна площади под графиком функции. По уравнению Клайперона - Менделеева Р=Rт/V, Подставим в первое уравнение тог
А= Рис 20 Работа совершаемая газом по диаграмме РV.
|
Процесс называется адиабатическим, если нет теплообмена системы с окружающей средой по первому началу терморегуляции. Работа равна изменению внутренней энергии системы. dv=0; dА=–dEв. В адиабатическом процессе работа совершается за счет изменения температуры. A=р·dv=–СvdТ
А =R/Сv
=R/Сv![]()
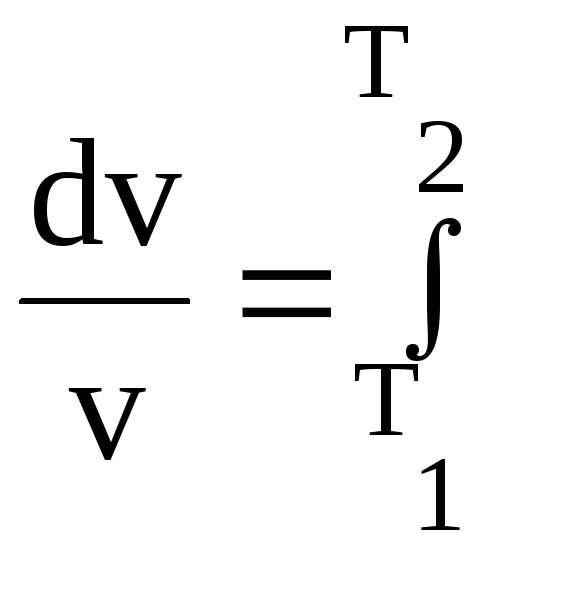 dт/т=lnT1–lnТ2
dт/т=lnT1–lnТ2
|
Цикл Карно.
1 4
2
3
|
Работа, совершаемая при круговом процессе графически равна площади, ограниченной замкнутой кривой цикла. КПД
= При этом Т2>Т1 |
Рис.21 Цикл Карно, работа равна площади цикла.
Энтропия dv/Т=ds
Полный дифференциал некой величины - s зависит только от состояния системы и не зависит от пути перехода системы в это состояние. Эта величина названа Клаузисом энтропия. В тепловых процессах энтропия определяет часть энергии которую можно превратить в работу, это как бы мера свободной энергии теплового процесса. В более широком смысле энтропия определяет степень упорядочности. Поскольку в природе самопроизвольно нарастает хаос, во всех необратимых процессах энтропия возрастает! Наведение порядка уменьшает энтропию! Человек, или самоорганизующая система, могут наводить порядок при наличии у них материи, энергии и информации, которые они берут из окружающей среды.
6.4 Химия наука о веществе, химических реакциях и химических системах.
Материя существует в виде вещества и физических, энергетических полей.
Химические свойства вещества – состав, строение, свойства, способы получения и применения.
Химические реакции - образование новых веществ, закономерности протекания в различных условиях.
Химические системы – растворы, сплавы, физико-химические и биохимические формы природных химических систем.
Физические свойства вещества – агрегатное состояние ( газ, жидкость, твердое тело, плазма), плотность, твердость или мягкость, упругость, хрупкость, цвет, блеск, запах, вкус, растворимость, теплопроводность, электрические и магнитные свойства.
Все остальные свойства относятся к химии.
Явления при которых изменяются физические свойства вещества называются физическими, а если меняются химические свойства, это химические явления.
Химические методы исследования – наблюдения химических явлений с поиском закономерностей и теоретического обоснования, химический эксперимент с заранее поставленной целью, измерение химических параметров и свойств моделирование натуральное, аналоговое, имитационное, в том числе с применением ЭВМ.
Химический элемент это атом с определенным зарядом ядра.
Атом это мельчайшая частица химического элемента, состоящий из положительно заряженного массивного ядра и легкой, отрицательно заряженной электронной оболочки. Атом химически не делим, он может изменяться только в атомных и ядерных физических реакциях. Химический элемент обозначается первой и одной из последних букв латинского алфавита, входящих латинское название элемента.
Молекула это мельчайшая частица вещества, состоящая из химически связанных атомов. Связь атомов в молекулу осуществляется за счет изменения их электронных орбит.
Химическая формула это изображение состава вещества или химической реакции с помощью знаков химических элементов и числовых индексов.
Изотопы, нуклиды это атомы одного химического элемента, имеющие различный атомный вес, из за различного количества нейтронов в ядре. Масса протона 1,675 *10 ^-24 грамм, примерно такая же масса у нейтрона. Электрон в 1836 раз легче протона. Поэтому масса атома определяется количеством протонов и нейтронов в ядре, пренебрегая массой электронной оболочки.
Атомная масса (вес) это отношение средней массы данного элемента, сучетом его природного изотопного состава, к одной атомной единицы. Атомная масса легчайшего элемента – водорода близка к единице. Аналогичным образом определяется молекулярная масса (вес), по сумме масс атомов входящих в молекулу.
Аллотропия это способность химического элемента существовать в виде нескольких простых веществ, например кислород –О2 и озон – О3, углерод в виде графита и алмаза.
Моль это количество вещества в граммах (в системе СИ в кг), равное молекулярной массе молекулы. В одном моле любого вещества содержится 6,02 * 10^23 молекул, это число Авагадро –NA. Число молекул -n в массе вещества – m определяется формуле (1),
n = m/M*NA
Валентность это способность атомов одного элемента присоединять один или более атомов другого элемента.
В 1869 году Д.И. Менделеев написал первый вариант таблицы химических элементов, а в 1971 году сформулировал периодический закон. Свойства элементов, а также свойства образуемых ими простых и сложных веществ находятся в периодической зависимости от заряда ядра атома. В таблице Менделеева имеется 7 периодов, расположенных по строкам таблицы. Свойства элементов находящихся в одной строке изменяются по определенному периоду. По столбцам таблицы расположены группы элементов с сходными свойствами и одинаковой валентностью.
В 1911 – 1913 гг. Э. Резерфорд и Н. Бор разработали и предложили планетарную модель атома, в которой вокруг тяжелого, положительно заряженного ядра движутся по орбитам электроны. При чем электроны находятся на строго определенных, квантованных орбитах, где они не излучают энергию. При переходе с одной орбиты на другую электроны излучают или поглощают строго определенные порции энергии в виде световых квантов. Орбиты электронов могут быть круговыми, гантелеобразными и лепестковыми. При образовании сложных молекул атомы элементов связываются общими электронными парами, движущими по пересекающим орбитам. Заполнение орбит электронами идет по строго определенным уровням – s, p, d, f, и так далее. Валентные электроны обеспечивающие связь атомов находятся на верхних уровнях. Планетарная модель атома и ее развитие объяснила многие химические свойства веществ и спектральное излучение атомов.
Химическая связь атомов в молекуле может быть ковалентной, ионной, металлической и водородной. В ковалентной связи атомов между ними образуются общие орбиты электронов с помощью валентных электронов. В ионной связи атомы притягиваются друг к другу, имея разный заряд. Атомы становятся положительно и отрицательно заряженными после обмена электронами между ними. Атомы металлов связываются за счет свободных электронов в кристаллической решетки, это металлическая связь. Водородная связь осуществляется атомами водорода. Многие органические молекулы имеют водородную связь.
Химические реакции приводят к образованию сложных веществ или распаду молекул на атомы. Их классификация многообразна. Они могут быть обратимыми и не обратимыми. Если скорости прямой и обратной реакции равны то наступает химическое равновесие. С выделением тепла (экзотермические) или поглощением тепла (эндотермические). По числу и составу исходных веществ реакции могут быть соединения, разложения, замещения и обмена. По изменению степени окисления – окислительно-восстановительные и не окислительно-восстановительные. По наличию катализатора реакции могут быть католическими и не католическими. Вещества католизирующие биохимические реакции в организмах называются ферментами. По агрегатному составу реагирующих веществ – гомогенные и гетерогенные. Скорость реакций определяется природой реагирующих веществ, их концентрацией, температурой и наличием катализатора. Реакции обычно ускоряются при повышении температуры, концентрации, давления и наличием катализаторов или ферментов.
Явление растворения характеризуется составом и концентрацией растворов. Растворение в воде называется гидратацией. В электрохимических растворах вещества самопроизвольно распадаются на положительные ионы – катионы, и отрицательные – анионы. При пропускании электрического тока катионы притягиваются к отрицательно заряженному катоду, а анионы к аноду. Процесс протекания тока в электролитах и количество осажденного чистого металла на катоде описывается формулами Фарадея, исследовавшего этот процесс.
Окислительно-восстановительные реакции при которых изменяется степень окисления элементов, путем перехода электронов от восстановителя к окислителю. Наиболее известный окислитель – кислород. Оксиды – соединения состоящие из двух элементов, один из которых кислород. Кислород самое распространенный элемент в земной коре его там более 49%. Окисление часто происходит в виде горения с выделением тепла. Не соединяются к кислородом инертные газы, галогены и благородные металлы ( золото и платина).
Основания это электролиты образующие при диссоциации в водных растворах анионы ОН-, например NaOH = Na+ + OH-. Для них характерна щелочная среда, сактивным взаимодействием с многими веществами.
Кислоты это электролиты образующие при диссоциации в водных растворах катионы водорода – Н+. По степени диссоциации кислоты могут быть сильные и слабые. Нерастворимы в воде стеариновые кислоты H2(SiO)3. Кислоты могут быть кислородными H2SO4 и без кислородными HCl. По числу атомов водорода они могут быть одноосновные, двухосновные, трехосновные. Кислоты активно реагируют с металлами, щелочами, солями, образуя новые соли.
Галогены – хлор, фтор, бром, иод реагируют со всеми металлами, кроме благородных, с водородом и водой. При этом образуются соли металлов или кислоты при взаимодействии с кислородом.
Активными и распространенными веществами являются сера, фосфор, азот, менее активен кремний. Кремний по количеству в земной коре (26%) стоит на втором месте после кислорода. Он применяется во многих производствах от строительства в виде песка до сверхчистого кремния в полупроводниковых приборах. Углерод основа живых клеток. Он имеется во многих органических молекулах.
Металлы составляют около 80% всех известных элементов. Они имеют небольшое число электронов на внешних орбитах 1-2 и реже 3. В периодах (по строкам таблицы Менделеева) металлические свойства убывают с ростом атомного веса. Все периоды, кроме первого, начинаются с металлов. По группам (столбцам таблицы), наоборот металлические свойства усиливаются с ростом атомного веса. Самый легкий металл – литий, плотность 0,53 г в куб. см. Самый тяжелый осьмий –22,6 г в куб. см. Самый легкоплавкий – ртуть, плавится при -38,9 оС, а огнеупорный – вольфрам +3416 оС. Всем металлам свойственны; кристаллическая решетка, блеск, непрозрачность, ковкость, тепло и электропроводность. Эти свойства закономерно меняются по таблице Менделеева, в зависимости от расположения электронных оболочек, особенно для валентных электронов. Все металлы отдают электроны и становятся положительно заряженными ионами – катионами. Таким образом металлы восстановители в окислительно-восстановительных реакциях. Все металлы, кроме благородных, реагируют с щелочами, кислотам, солями, кислородом, водой и не металлами с различной степенью активности. По этой причине металлам свойственна коррозия. Устойчивы к коррозии благородные металлы и покрывающиеся тонкой пленкой окислов (алюминий, медь и др.)
Особенно активны щелочные металлы – натрий, калий , бром. Множество природных веществ образуют соединения кальция Са, магния Mg, алюминия Al. Оксид алюминия Al2O3 – корунд, отличается высокой прочностью, твердостью, огнупорностью, за счет кристаллической решетки. Самый известный металл – железо Fe 56. Имеются четыре модификации железа, отличающиеся химическими и физическими свойствами. Железо реагирует с щелочами, кислотами, солями, кислородом, водой. Поэтому железо необходимо защищать от коррозии. Получают металлы с помощью термической и химической обработки природных руд, в которых находятся окислы или соли металлов.