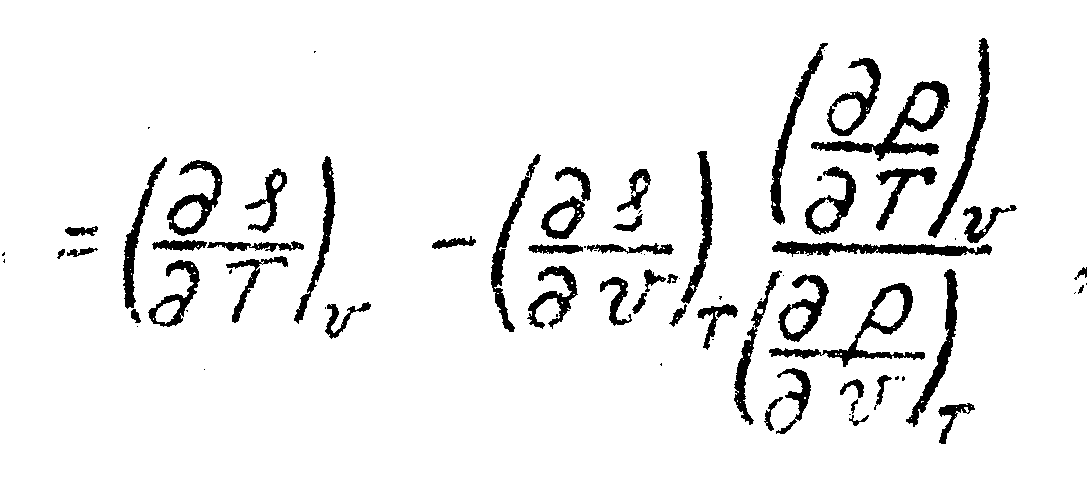2013.Термодинамика / Paskal / 2011_09_27 / 2011_09_27 / IMG_0026-68
.doc- 68 -Для системы Ван-дер-Ваальса
![]()
Интегрируя это выражение, получим формулу для энтропии система Ван-дер-Ваяльса
![]() (1.6*6)
где
(1.6*6)
где![]() -
константа интегрирования, не зависящая
ни от TV ни от
-
константа интегрирования, не зависящая
ни от TV ни от
![]() При
неограниченном возрастании объёма
энтропия систему Ван- дер-Ваальса
приближается к энтропии идеального
газа;при этом изменяется только второй
член правой части (1,6,6), тек как
При
неограниченном возрастании объёма
энтропия систему Ван- дер-Ваальса
приближается к энтропии идеального
газа;при этом изменяется только второй
член правой части (1,6,6), тек как![]() не зависит от объёма
не зависит от объёма
![]() (1.6.6)
Подставляя в
(1.6.6)
Подставляя в![]() (1.6.6)
и (1.6.7), легко увидеть, что изохорная
теплоемкость для системы Ван-дер-Ваальса
такова же, как и для идеального газа.
(1.6.6)
и (1.6.7), легко увидеть, что изохорная
теплоемкость для системы Ван-дер-Ваальса
такова же, как и для идеального газа.
Таким образом;
![]() (1.6.7)
(1.6.7)
и
есть уравнение изобары Ван-дер-Ваальса![]() в
неявном ви-
в
неявном ви-
де,
Чтобы получить явный вид изобары ,
необходимо решить кубическое
относительно v
уравнение
Ван-дер-Ваальса и решение подставить в
(1,6.8). Однако можно исследовать общий
характер изобары, обходя
эту громоздкую процедуру. Для этого
преобразуем произвольную
при
помощи якобианов.![]()
![]()