
- •Введение
- •1 Коллекторские свойства горных пород
- •1.1 Типы пород–коллекторов
- •1.2 Залегание нефти, газа и воды
- •1.3 Гранулометрический состав горных пород
- •1.4 Пористость
- •1.4.1 Виды пористости
- •1.4.2 Структура порового пространства
- •1.5 Проницаемость
- •1.5.1 Линейная фильтрация нефти и газа в пористой среде
- •1.5.2 Радиальная фильтрация нефти и газа в пористой среде
- •1.5.3 Классификация проницаемых пород
- •1.5.4 Оценка проницаемости пласта, состоящего из нескольких продуктивных пропластков различной проницаемости
- •1.5.5 Зависимость проницаемости от пористости
- •1.5.6 Виды проницаемости
- •1.6 Насыщенность коллекторов
- •1.7 Зависимость проницаемости от насыщенности коллекторов
- •1.8 Удельная поверхность
- •1.9 Коллекторские свойства трещиноватых пород
- •1.10 Карбонатность горных пород
- •1.11 Набухаемость пластовых глин
- •1.12 Механические свойства горных пород
- •1.13 Тепловые свойства горных пород
- •2 Состав и физико-химические свойства природных газов и нефти
- •2.1 Состав и физико-химические свойства природных газов
- •2.1.1 Состав природных газов
- •2.1.2 Способы выражения состава
- •2.1.3 Аддитивный подход расчета физико-химических свойств
- •2.1.4 Уравнение состояния
- •2.1.5 Уравнение состояния реальных газов
- •2.1.6 Вязкость газов
- •2.1.7 Растворимость газов в нефти и воде
- •2.1.8 Упругость насыщенных паров
- •2.2 Состав и физико-химические свойства нефти
- •2.2.1 Состав нефти
- •2.2.2 Физико–химические свойства нефти
- •2.2.2.1 Плотность нефти
- •2.2.2.2 Вязкость нефти
- •2.2.2.3 Реологические свойства нефти
- •2.2.2.4 Газосодержание нефти
- •2.2.2.5 Давление насыщения нефти газом
- •2.2.2.6 Сжимаемость нефти
- •2.2.2.7 Объёмный коэффициент нефти
- •2.2.2.8 Тепловые свойства нефти
- •2.2.2.9 Электрические свойства нефти
- •2.3 Различие свойств нефти в пределах нефтеносной залежи
- •3 Фазовые состояния углеводородных систем
- •3.1 Схема фазовых превращений однокомпонентных систем
- •3.2 Схема фазовых превращений двух – и многокомпонентных
- •3.4 Краткая характеристика газогидратных залежей
- •3.6 Фазовые переходы в воде, нефти и газе
- •4 Состав и физико-химические свойства пластовых вод
- •4.1 Химические свойства пластовых вод
- •4.1.1 Минерализация пластовой воды
- •4.1.2 Тип пластовой воды
- •4.1.3 Жесткость пластовых вод
- •4.1.4 Показатель концентрации водородных ионов
- •4.2 Физические свойства пластовых вод
- •4.2.1 Плотность
- •4.2.2 Вязкость
- •4.2.3 Сжимаемость
- •4.2.4 Объёмный коэффициент
- •4.2.5 Тепловые свойства
- •4.2.6 Электропроводность
- •4.3 Характеристика переходных зон
- •5.1 Роль поверхностных явлений при фильтрации в пористой среде
- •5.2 Поверхностное натяжение
- •5.3 Смачивание и краевой угол
- •5.4 Работа адгезии и когезии, теплота смачивания
- •5.5 Кинетический гистерезис смачивания
- •5.6 Свойства поверхностных слоев пластовых жидкостей
- •6 Физические основы вытеснения нефти водой и газом из пористых сред
- •6.1 Источники пластовой энергии
- •6.2 Силы, действующие в залежи
- •6.3 Поверхностные явления при фильтрации пластовых жидкостей и причины нарушения закона Дарси
- •6.4 Общая схема вытеснения из пласта нефти водой и газом
- •6.5 Нефтеотдача пластов при различных условиях дренирования залежи
- •6.6 Роль капиллярных процессов при вытеснении нефти водой из пористых сред
- •6.7 Зависимость нефтеотдачи от скорости вытеснения нефти водой
- •7. 1 Методы увеличения извлекаемых запасов нефти
- •7.2 Моющие и нефтевытесняющие свойства вод
- •7.3 Обработка воды поверхностно-активными веществами
- •7.4 Применение углекислого газа для увеличения нефтеотдачи
- •7.5 Вытеснение нефти из пласта растворами полимеров
- •7.6 Щелочное и термощелочное заводнение
- •7.7 Мицеллярные растворы
- •7.8 Термические методы повышения нефтеотдачи пластов
- •7.9 Извлечение нефти газом высокого давления
- •Список литературы
- •Содержание
- •Физика пласта
2.1.8 Упругость насыщенных паров
Упругость насыщенных паров углеводородов характеризует то давление, при котором газ начинает конденсироваться и переходить в жидкое состояние. У индивидуальных углеводородов в чистом виде упругость паров (Q) есть функция только температуры: Q =ƒ (Т). Величина упругости насыщенных паров углеводородов повышается с ростом температуры, и она тем выше, чем ниже плотность углеводорода. Аналогично с ростом молекулярной массы углеводорода величина упругости насыщенный паров углеводородов уменьшается при равных температурах (рис. 2.11).
Зависимость упругости пара от температуры: Q =ƒ (Т) – нелинейная функция. Для ее линеаризации шкала упругости пара принята логарифмической, и это создает удобства для пересчета величины упругости пара при нужной температуре. Анализ зависимостей представленных на рисунке 2.11 свидетельствует, что давление паров метана наибольшее. При нормальных условиях его нельзя превратить в жидкость (пунктирная линия), так как его критическая температура (Ткр.) = – 82,4о С (190,75 К).
На рисуеке 2.12, а изображены зависимости объёма жидкого и парообразного пропана. При сжатии от точки М до точки А имеется перегретый (ненасыщенный) пар, зависимость объёма жидкости от давления при конкретной температуре имеет гиперболическую форму.

Рисунок 2.11 – Кривые упругости насыщенных паров чистых углеводородов: 1 – метан; 2 – этан; 3 – пропан; 4 – изобутан; 5 – бутан; 6 – изопентан; 7 – пентан; 8 – изогексан; 9 – гексан; 10 – изогептан; 11 – гептан; 12 – октан; 13 – нонан; 14 – декан
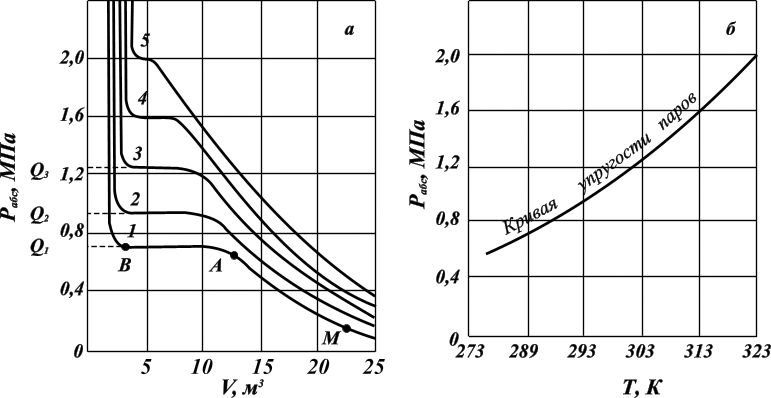
Рисунок 2.12 – Зависимости давления от объёма и температуры (а) и кривая упругости насыщенных паров (б) при температурах, К: 1 – 283; 2 – 293; 3 – 303; 4 – 313; 5 – 323
В точке А пар становится насыщенным, а при дальнейшем изменении объёма (участок АВ) он постепенно переходит в жидкость при неизменном давлении. В точке В заканчивается переход пара в жидкость. При дальнейшем сжатии пара будет резко повышаться давление при почти неизменном объёме. Горизонтальный участок АВ соответствует неизменности давления в процессе конденсации паровой фазы в жидкую фазу. Величина этого давления и есть упругость насыщенного пара газового компонента при данной температуре. Чем ближе значение температуры, при которой измеряется упругость насыщенного пара газового компонента к значению критической температуры, тем короче горизонтальный участок. На основе полученных данных строят кривую упругости насыщенных паров, представляющую зависимость давления от температуры испарения данной жидкости (рис. 2. 12, б).
У смеси углеводородов упругость паров является функцией и температуры, и общего давления смеси: Q = ƒ (Т, Рсм). Величина её зависит от упругости паров отдельных компонентов при данной температуре и от их мольных концентраций. Общее давление смеси влияет на упругость паров каждого компонента, и это влияние учитывается по закону Рауля:
Р = ∑ рi
и
![]() (2.39)
(2.39)
где Р – общее давление;
рi – парциальное давление i-го компонента;
Qi – упругость паров i-го компонента;
Nxi – мольная доля i-го компонента в жидкости.
Упругость паров смеси компонентов повышается с увеличением общего давления. Это влияние ничтожно при низких давлениях (≈ до 1 МПа), а при высоких давлениях упругость паров резко увеличивается.
