
- •Контрольные работы общая химия
- •1. Классы неорганических соединений
- •1.1. Классификация неорганических веществ
- •1.2. Понятие о степени окисления
- •1.3. Оксиды
- •1.4. Основания
- •1.5. Кислоты
- •1.6. Соли
- •1.7. Примеры решения задач
- •1.8. Задачи для самостоятельного решения
- •2. Химическая термодинамика
- •2. 1. Основные понятия
- •2.2. Первый закон термодинамики. Энтальпия
- •2.3. Термохимия
- •2.4. Энтропия. Энергия Гиббса
- •2.5. Примеры решения задач
- •2.6. Задачи для самостоятельного решения
- •3. Химическая кинетика и равновесие химических реакций
- •3.1 Кинетика химических реакций
- •3.1.1 Зависимость скорости от концентрации
- •3.1.2.Зависимость скорости от температуры
- •3.1.3. Зависимость скорости реакции от катализатора
- •3.2. Равновесие химических реакций
- •3.2.1. Равновесие в гомогенных системах
- •3.2.2. Равновесие в гетерогенных системах
- •3.3. Примеры решения задач
- •3.4. Задачи для самостоятельного решения
- •4. Растворы
- •4.1. Общие свойства растворов
- •4.1.1. Классификации растворов
- •4.1.2. Коллигативные свойства растворов
- •4.2 Свойства растворов электролитов
- •4.2.1. Равновесие в растворах электролитов
- •4.2.2. Ионно-обменные реакции в растворах электролитов
- •4.2.3. Ионное произведение воды
- •4.2.4. Гидролиз солей
- •4.3. Примеры решения задач
- •4.4. Задачи для самостоятельного решения
- •5. Электрохимические процессы
- •5.1. Степень окисления элемента
- •6.2. Окислительно-восстановительные реакции
- •5.3. Основные понятия электрохимических процессов
- •5.4. Ряд напряжений металлов
- •5.5. Гальванический элемент
- •5.6. Электролиз
- •5.7. Явление поляризации. Напряжение разложения
- •5.8. Примеры решения задач
- •5.9. Задачи для самостоятельного решения
- •Контрольные вопросы
- •6. Коррозия металлов
- •6.1.1. Классификация коррозионных процессов
- •Катодные процессы при коррозии
- •6.2. Методы защиты от коррозии
- •6.3. Примеры решения задач
- •6.4. Задачи для самостоятельного решения
- •Контрольные вопросы
- •7. Химия металлов
- •7.1. Металлическая связь
- •7.2. Зонная теория кристаллов
- •7.3. Химические свойства металлов
- •7.4. Способы получения металлов
- •7.5. Способы очистки металлов
- •10.6. Сплавы металлов
- •7.6. Диаграммы состояния веществ, образующих
- •7.2. Диаграммы состояния веществ с неограниченной растворимостью
- •7.3. Диаграммы состояния веществ, образующих
- •7.7. Примеры решения задач
- •7.8. Задачи для самостоятельного решения
- •Контрольные вопросы
- •8. Химическая идентификация и анализ вещества
- •8.1. Качественный анализ
- •Кислотно-основная классификация катионов
- •Некоторые реагенты для идентификации катионов
- •8.2. Количественный анализ
- •8.3. Инструментальные методы анализа
- •8.4. Примеры решения задач
- •8.5. Задачи для самостоятельного решения
- •Контрольные вопросы
- •Библиографический Список Основная литература
- •Дополнительная литература
- •Перечень задач для выполнения контрольных работ
- •Список важнейших кислот
- •Константы диссоциации некоторых кислот и оснований
- •Приближенные значения коэффициентов активности ионов в водных растворах
- •Стандартные электродные потенциалы металлов
4.2.1. Равновесие в растворах электролитов
Равновесие между недиссоциированными молекулами и ионами описывается соответствующей константой, называемой константой диссоциации.
Константа диссоциации (Kд) – отношение произведения равновесных концентраций ионов в степени соответствующих стехиометрических коэффициентов к концентрации недиссоциированных молекул.
|
|
(11) |
где [А+], [В-], [АВ] – равновесные молярные концентрации ионов и недиссоциированных частиц.
Значения констант диссоциации слабых электролитов определены экспериментально и приведены в справочниках. Для сильных электролитов константы отсутствуют, т. к. их диссоциация необратима. Например, диссоциация уксусной кислоты и константа диссоциации выражаются уравнениями:
CH3COOH
⇄
CH3COO–
+ H+,
![]() .
.
Если молекула слабого электролита состоит более чем из двух ионов, то его диссоциация идет по ступеням, и каждая ступень характеризуется своей константой диссоциации. Например, диссоциация H2CO3 может протекать в 2 ступени:
1 ступень H2СO3 ⇄ H+ + HСO3–
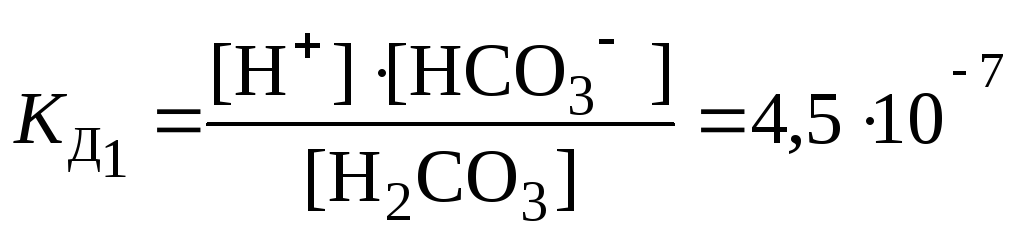
2 ступень: HСO3– ⇄ H+ + СO32–
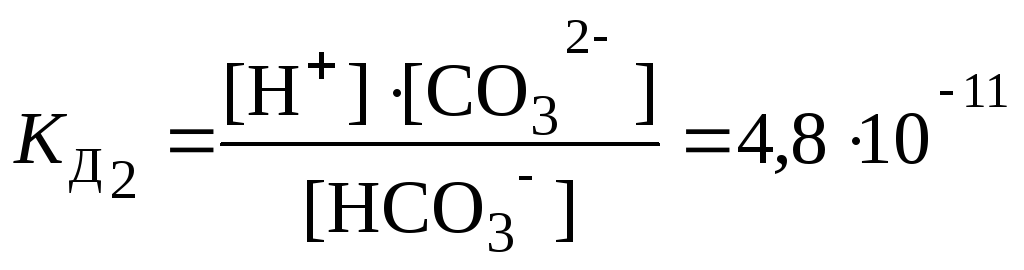
Исходя из значений константы диссоциации, можно оценивать и сравнивать силу электролитов: чем меньше КД тем слабее электролит, и наоборот.
Для разбавленных растворов слабых электролитов между константой диссоциации, концентрацией раствора и степенью диссоциации существует связь, которая выражается законом разбавления Оствальда: степень диссоциации возрастает с уменьшением концентрации раствора (т.е. при его разбавлении).
|
|
(12) |
Если степень диссоциации очень мала <<1, то (1–)1. Следовательно, закон разбавления Оствальда для слабых электролитов принимает вид:
|
|
(13) |
4.2.2. Ионно-обменные реакции в растворах электролитов
В разбавленных растворах электролитов (кислот, оснований, солей) между ионами могут протекать химические реакции, не сопровождающиеся изменениями степеней окисления. Они называются реакциями ионного обмена.
Ионно-обменные реакции протекают практически необратимо, если образуются малорастворимые вещества (они выпадают в осадок), легколетучие вещества (они выделяются в виде газа) или малодиссоциирующие вещества – слабые электролиты (в том числе вода), комплексные соединения.
Ионообменные реакции записывают обычно с помощью молекулярного, полного ионного и краткого ионного уравнений. Например, молекулярное уравнение:
Pb(NO3)2 + 2HI = PbI2↓ + 2HNO3;
ионное уравнение:
Pb2+
+
2NO3–
+ 2H+
+ 2I–
= PbI2↓
+ 2H+
+ 2NO3–;
сокращенное ионное уравнение:
Pb2+ + 2I– = PbI2↓.
4.2.3. Ионное произведение воды
Вода – очень слабый электролит, поэтому на ионы диссоциирует в незначительной степени:
Н2О ⇄ Н+ + ОН–.
Для данного равновесия на основе закона действия масс, можно записать константу равновесия – константу диссоциации воды (КД):
![]() илиКд
[ Н2О]
= [Н+]
[ ОН–].
илиКд
[ Н2О]
= [Н+]
[ ОН–].
Обозначая Кд [Н2О] через КВ, получим:
КВ = [Н+][ОН–]
КВ – называют ионным произведением воды. При 25 °С КВ = 1·10–14, тогда
|
[Н+][ОН–] = 1·10–14 |
(14) |
Полученное уравнение показывает, что для воды и разбавленных водных растворов при неизменной температуре произведение концентраций ионов водорода и гидроксид-ионов есть величина постоянная. В чистой воде при 25 оС
[H+] = [ОН–] = 1·10–7моль/л
Раствор, в котором концентрация ионов водорода равна концентрации гидроксид-ионов называют нейтральным. Если концентрация [Н+] > [ОН –], то такой раствор называют кислым. Если концентрация [Н+] < [ОН–], то раствор называют щелочным.
Кислотность или щелочность раствора выражают другим более удобным способом: вместо концентраций ионов водорода [H+] и гидроксид-ионов используют их десятичный логарифм, взятый с обратным знаком:
|
рН = – lg [Н+], рОН = – lg [ОН–]. |
(15) |
Соответственно,
|
рН + рОН = 14. |
(16) |
Величина рН называется водородным показателем и для характеристики среды раствора используется чаще:
рН > 7 – среда щелочная;
рН < 7 – среда кислая;
рН ≈ 7 – среда нейтральная.
При использовании величин концентраций часто наблюдается отклонение от закона действующих масс, в основном для сильных электролитов. Поэтому вместо концентраций пользуются активностями электролита (а). Отличие активности электролита от концентрации связано с частичной или полной диссоциацией его молекул на ионы, появлением сил электростатического взаимодействия этих ионов, взаимодействием ионов с молекулами растворителя. Активность связана с концентрацией через коэффициент активности (γ):
|
а = С∙ γ |
(17) |
Коэффициент активности – работа против сил, вызывающих отклонение свойств раствора от свойств идеальных растворов. Например, рН = –lg aH+.
Установлено, что в малоконцентрированных растворах коэффициент активности иона определяется только электростатическими взаимодействиями. Следовательно, γ зависит только от концентрации электролита и заряда иона и не зависит от природы электролита. Мерой электростатического взаимодействия является ионная сила раствора (I).
Связь коэффициента активности электролита с ионной силой раствора описывает предельный закон Дебая-Хюккеля:
|
|
18 |
где А – коэффициент, зависящий от температуры и диэлектрической постоянной растворителя Для воды при 298К А = 0,509. Обычно для приближенных расчетов рассчитывают ионную силу раствора и на основании этого определяют коэффициент активности по справочным данным:
|
|
(19) |
