
53fb59db0cf22f21c2f3100d
.pdf
31
яку ми шукали, можна обчислювати за наближеною формулою:
dN |
(1) |
|
|
f ( v,T )dv |
|
N |
|
|
Таке наближення відповідає тому, що на мал. 3 заштриховану площу можна прирівняти до площі прямокутника з основою v і висотою f v1T .
Отже, спочатку потрібно знайти значення функції Максвелла при v v1, v v2 і визначити, яку
похибку дає використання рівняння (1).
Функція Максвелла має вигляд: (2) де vім найбільш імовірна швидкість молекул,
|
|
vім |
|
|
|
|
|
|
|
|
|
|
|
(3) |
|
|
|
|
||||
|
|
|
2kT / m0 |
|
2RT / |
|
|
|
|
|
|
|||||||||||
|
Для того, щоб спростити підрахунки спочатку знайдемо найбільш імовірну швидкість з рівняння |
|||||||||||||||||||||
(3): v |
|
|
|
|
410м / с. |
|
|
|
|
|
|
|||||||||||
|
2RT / |
|
|
|
|
|
|
|
||||||||||||||
|
|
ім |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Тоді f |
v ,T 4,03 10 4 с / м; f v ,T 3,75 10 4 с / м. |
|
|
|
|
|
|
||||||||||||||
|
|
|
1 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|||
|
Це означає, що при використанні виразу (1) ми допустили відносну похибку |
|
|
|||||||||||||||||||
f |
|
f v1 ,T f |
v2 ,T |
|
0,07, |
тобто 7%. |
|
|
|
|
|
|
||||||||||
|
f v1 ,T |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Отже, рівність (1) можна використовувати з вказаною точністю. Тоді частка молекул, швидкість |
|||||||||||||||||||||
яких лежить в даному інтервалі |
|
|
|
|
|
|
||||||||||||||||
|
|
N / N f v1 ,Т v 4,0 10 3 , тобто 0,4%. |
|
|
|
|
|
|
||||||||||||||
|
Задача 9. Середня довжина вільного пробігу молекули вуглекислого газу CO за нормальних |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
умов дорівнює 40 км. Визначити середню арифметичну швидкість v молекули і число зіткнень, які |
||||||||||||||||||||||
має молекула за 1с. |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
Дано: |
|
|
|
|
|
|
|
|
|
|
|
|
|
Розв’язання |
|
|
|
|
|
|
|
|
Середня арифметична швидкість молекул визначається за формулою: v |
|
, де |
||||||||||||||||||
l 40км |
|
8RT / |
||||||||||||||||||||
t 1c |
– молекулярна маса речовини. Підставимо числові дані і отримаємо: |
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
362м / c, |
|
|
|
|
|
|
||||
CO2 |
|
|
|
|
v |
|
|
|
8 8,31 273 / 3,14 0,044 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
________ |
|
|
|
|
де МСО |
12 2 16 44г / моль 0,044кг / моль . |
|
|
|
|
|
|
||||||||||
v ? |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Отже, |
v 362м / с . |
|
|
|
|
|
|
|||||||||||
z ? |
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
Середнє число z зіткнень молекул за 1с визначається відношенням середньої |
||||||||||||||||||
швидкості |
|
v |
|
|
молекули до середньої довжини її вільного пробігу l |
: |
z |
v |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l |
|
|
||
Підставивши в цю формулу значення v 362м / с і l 40Hм 40 10 9 м отримаємо
z 362 / 40 10 9 9,05 109 c 1.
Задача 10. Зрівняти повне число молекул в атмосферному стовпі з підставою в 1 см2 із числом молекул у стовпі висотою 1000 м і тим же підставою.
Розв’язання.
Нехай число молекул в одиниці об'єму при h = 0 дорівнює N0 , тоді розподіл числа цих часток по
висоті буде визначатися наступним виразом:
N(h) N0e mgh/(kT) N0e gh/(RT ) .
Повне число молекул у стовпі з підставою в 1 см2 і заданою висотою
N(H ) H |
N(z)dz N |
|
H |
e gh /(RT )dz N |
|
RT |
(1 e gH /(RT )), |
|
0 |
0 |
g |
||||||
0 |
|
0 |
|
|
||||
|
|
|
|
|
|
де μ - молярна маса повітря.
Підставивши чисельні значення висоти, одержимо: N(H → ∞ ) = 2.1· 1025; N(H = 103) = 0.25· 1025.

32
Задача 11. На якій висоті перебувають центр мас вертикального стовпа повітря в атмосфері Землі, якщо температура повітря T не залежить від h. Уважати, що для повітря має місце розподіл Больцмана.
Розв’язання.
Нехай площа перетину стовпа повітря S. Виділимо на деякій висоті h шар повітря товщини dh, тоді його маса буде dm = ρ(h)·S·dh, де ρ(h)- густина повітря на висоті h. Оскільки ρ(h) = m·n(h), де m - маса молекули, а n(h)- концентрація молекул на висоті h, котра визначається з розплділу Больцмана: n(h) n0e mgh/(kT) .
З курсу механіки відомо, що центр мас тіла з безперервним розподілом маси визначається співвідношенням, що у нашому випадку має вигляд:
|
|
|
|
|
|
|
|
|
hdm |
|
|
H |
|
0 |
. |
||
C |
|
||||
|
|
|
|||
|
|
|
dm |
|
|
|
|
|
0 |
|
Обчислимо інтеграли: |
|
|
|
|
|||
|
dm mn S e |
|
|
|
0 |
0 |
|
|
0 |
|
|
|
|
|
|
mgh/(kT) |
dh |
mn S kT |
|
|
|
0 |
e |
|
|
|
|
mg |
|
|
|
|
|
|
|
mgh/(kT) |
|
n S kT |
. |
|
0 |
||
|
|
g |
|
0 |
|
|
|
|
|
|
mgh/(kT) |
|
n S (kT) |
2 |
|
|
|
|
|
|
||||||
mn S he |
dh |
. |
|||||||
hdm hmn(h)S dh |
|
0 |
|||||||
|
|
|
|
|
|
|
|
||
0 |
0 |
|
0 |
|
|
mg2 |
|
|
|
|
0 |
|
|
|
|
||||
|
|
|
|
|
|
|
|
||
Звідки знаходимо: HC |
kT . |
|
|
|
|
|
|||
|
|
|
mg |
|
|
|
|
|
|
Таким чином, центр мас вертикального стовпа повітря перебуває на висоті, на якій концентрація молекул n(h), а отже, потенційна енергія молекул і тиск газу зменшуються в e раз.
Задача 12. Обчислити середню потенційну енергію молекули газу в полі сили ваги.
Розв’язання.
Середнє значення потенційної енергії молекули газу на висоті z визначається вираженням:
U  mg zdW (z) , де d(z) - імовірність того, що потенційна енергія молекули укладена в інтервалі
mg zdW (z) , де d(z) - імовірність того, що потенційна енергія молекули укладена в інтервалі
|
0 |
|
|
|
|
|
|
|
|
|
|
від U до U + d у поле ваги Землі: dW (z) |
e mgz/(kT)dz . |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
e mgz/(kT)dz |
|
|||
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
mgz/(kT)dz |
|
|
|
|
|
|
||
Тоді |
U mg |
ze |
mg |
(kT /(mg)) |
2 |
kT |
, |
||||
0 |
|
|
|
|
|||||||
|
|
mgz/(kT) |
|
|
|
|
|||||
|
|
|
|
(kT /(mg)) |
|
||||||
|
|
e |
dz |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||
|
0 |
|
|
|
|
|
|
|
|
|
|
тобто потенційна енергія молекул у поле сили ваги залежить тільки від температури.
Задача 13. Проводяться спостереження за кулястими частками, що перебувають у зваженому стані в повітрі (у полі земного тяжіння). Радіус часток r = 2·10-7 м. Температура повітря t = 0оС, тиск p = 105 Па. Установлено, що на висоті h =10 м концентрація частинок зменшується вдвоє. Знайти масу зваженої частинки?
Розв’язання.
Позначимо масу частки m. Оскільки частки зважені в повітрі, те варто враховувати силу, що
виштовхує. Таким чином, сила, |
що діє на частку, F mg(1 |
0 |
/ ), де ρ0 - щільність повітря в |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
поверхні Землі; ρ - щільність частки. У цьому випадку закон Больцмана запишеться у вигляді |
||||||||||||
|
|
mg(1 |
0 |
/ ) |
|
|
|
|
|
|
|
|
n(z) n |
exp |
|
|
|
z . |
|
|
|
|
|
|
|
kT |
|
|
|
|
|
|
|
|
|
|||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Щільність частки радіусом r: |
|
m |
|
3m |
. |
|
|
|||||
|
|
|
||||||||||
|
|
|
|
|
|
|
V |
|
4 r3 |
|
|
|

33
За умовою завдання, на висоті h = 10 м n(h) = n0/2. Тоді відношення концентрації часток на двох різних висотах
n |
|
|
m(1 / ) |
|
2 , звідки |
ln 2 |
mgh |
|
4gh r3 / 3 |
. |
||
0 |
exp |
0 |
gh |
|
|
0 |
|
|||||
n(h) |
|
|
kT |
|
|
|
kT |
|
kT |
|
||
|
|
|
|
|
|
|
||||||
Отже, маса частки m |
kT ln 2 4gh r3 |
/ 3 |
. |
0 |
|
||
gh |
|
||
|
|
|
Підставивши в останню формулу чисельні значення величин, одержимо m = 5.4·10-21 кг.
Задача 14. Знайти силу, що діє на частку з боку однорідного поля, якщо концентрації цих часток на двох рівнях, що відстоять один від іншого на відстані h = 3 см (уздовж поля), відрізняються в η = 2 рази. Температура системи T = 280 К.
|
|
|
|
|
|
|
|
|
|
|
Розв’язання. |
|
Сила, що діє на частку з боку однорідного поля, визначається виразом |
||||||||||
|
F |
U (h2 ) U (h1) |
|
U2 U1 |
|
, |
|||||
|
|
|
h |
|
|
|
h |
|
|||
|
де h = h2 - h1 . Відповідно до розподілу Больцмана концентрації часток n1 та n2 на двох рівнях h1 |
||||||||||
й h2 |
визначаються відповідно |
|
|||||||||
|
n n0e |
U1 /(kT) |
и. n n0e |
U2 /(kT) |
|||||||
|
|
|
|
||||||||
|
1 |
|
|
|
2 |
|
|
|
|||
|
Оскільки частки розташовуються з більшою щільністю там, де менше їхня потенційна енергія, то |
||||||||||
n1/n2 = η. Отже, |
U1 |
|
|
U2 |
ln , |
||||||
kT |
|
|
|||||||||
|
|
|
|
|
|
kT |
|
||||
або U2 U1 kT ln .
Шукана сила F kTh ln 0.9 10 19 H.
Задача 15. У довгій вертикальній посудині перебуває газ, що складається із двох сортів молекул з масами m1 й m2 , причому m2 > m1. Концентрації цих молекул у дна посудини рівні відповідно n1 й n2, причому й n2 > n1. Уважаючи, що по всій висоті підтримується та сама температура T і прискорення вільного падіння дорівнює g, знайти висоту h, на якій концентрації цих сортів молекул будуть однакові.
Запишемо розподіл
n'1 n1e m1gh/(kT) і
Очевидно, що ln n'1
Розв’язання.
Больцмана для двох сортів молекул, що перебувають у полі сили ваги: n'2 n2e m2gh/(kT)
ln n1 m1gh /(kT) , ln n'2 ln n2 m2 gh /(kT) .
Шукану висоту h, де концентрації молекул будуть однакові, знайдемо, прирівнявши праві
частини цих рівнянь: |
ln n ln n (m m ) gh /(kT) . |
||||||||
|
|
|
2 |
|
1 |
2 |
1 |
||
|
|
|
|
|
|
||||
|
|
kT |
|
|
|
n |
|
|
|
Звідси h |
|
|
|
ln |
2 |
. |
|
|
|
|
|
|
|
|
|
||||
|
m ) g |
|
|
|
|||||
|
(m |
|
n |
|
|
||||
2 |
|
1 |
|
|
1 |
|
|
|
|
Задача 16. У циліндричній центрифузі перебуває емульсія, що складається з часток білка масою m і води. Щільність білка ρ. Центрифуга обертається з кутовою швидкістю ω. Визначити відношення числа часток, що перебувають на двох різних відстанях r1 й r2 (r2 > r1) від осі циліндра.
Розв’язання
Частинка білка, що перебуває у воді, в обертовій центрифузі відчуває дію відцентрової сили інерції (дією сили ваги зневажаємо):

|
|
|
|
|
|
34 |
|
|
|
, |
|||
|
F(r ) m 2r |
m 2r |
||||
|
|
|
|
|
B |
|
|
де r - радіус-вектор частки щодо осі циліндра; mВ - маса води витісненої об’ємом білка (сила |
|||||
mB 2r - |
аналог сили Архімеда). З огляду на, що mВ = ρ0m/ρ, де ρ0 - щільність води, одержуємо |
|||||
|
|
|
|
|
|
|
F(r ) m(1 |
0 |
/ ) 2r . |
|
|||
|
|
|
|
|
|
|
Зважаючи, що потенційна енергію частинки U(r) на осі циліндра рівна нулю, знаходимо:
r |
|
|
|
|
|
|
|
|
/ ) 2 |
r |
|
|
|
|
|
|
|
|
|
|
|
r'dr' |
|
|
|
||||||||
U (r) |
(F(r '),dr ') m(1 |
0 |
|
|
|
|||||||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
(1 |
|
/ ) 2r 2. |
|
|
|
|
|
|
|
|||
|
|
2 |
0 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Підставляючи цей вираз у формулу Больцмана, одержуємо |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
/ ) |
2 |
r |
2 |
|
|
|
|
|
|
|
|
|
|
m(1 |
|
|
|
, |
(1) |
|||||
n(r) n e U (r) /(kT) n exp |
|
|
0 |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||
0 |
|
|
|
0 |
|
|
2kT |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тобто число часток росте в міру віддалення від осі. З формули (1) матимемо шукане відношення
|
|
/ ) |
2 |
|
|
|
|
|
|
n(r ) |
m(1 |
|
|
2 |
|
2 |
. |
||
2 |
exp |
|
0 |
|
(r |
|
r |
|
) |
|
|
|
|
|
|
||||
n(r ) |
|
2kT |
2 |
1 |
|
||||
|
|
|
|
|
|
|
|||
1 |
|
|
|
|
|
|
|
|
|
Задача 17. Знайти найбільш імовірну швидкість молекул ідеального газу.
Розв’язання.
Припускаючи, що ідеальний газ перебуває в термодинамічній рівновазі, використаємо функцію розподілу молекул по швидкостях:
|
|
f (v ) 4 (a / )3 / 2 e av 2 v 2 , |
|
|
|
|
(1) |
||||||
|
|
де a = m/(2k). Похідна функції розподілу (1) по швидкості |
|
|
|
||||||||
|
|
f '(v ) 4 (a / )3 / 2 ( 2av 3 2v )e av 2 . |
|
|
|
|
|
||||||
|
|
Позначаючи найбільш імовірну швидкість через v |
B |
, знаходимо її з рівняння |
f '(v |
B |
) 0 , тобто |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
2v |
B |
( av 2 1) 0. |
|
|
|
|
|
||||||
|
B |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Звідси v |
|
|
|
|
|
. |
|
|
|
|
|
|
|
B |
1/ a |
2kT / m |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Задача 18. При якій температурі ідеального газу число молекул зі швидкостями в заданому інтервалі v, v + dv буде максимальним?
Розв’язання
Знайдемо максимум функції розподілу молекул по величині швидкості, розглядаючи її як
функцію температури або параметра a = m/(2k), тобто |
|
|||||||||||||||||||||
F(a) 4 (a / )3 / 2 e av 2 v 2 . |
|
|
|
|
|
|
|
|
|
|
(1) |
|||||||||||
Диференціюючи функцію (1) по параметрі a, одержуємо |
|
|||||||||||||||||||||
F'(a) 4 v 2e av |
2 |
|
3 ( a ) |
|
|
1 |
( a ) |
|
v |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
1 / 2 |
|
|
|
|
3 / 2 |
|
2 |
|
|
|||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
(2) |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 v |
2 |
|
av |
2 |
|
a |
1/ 2 |
|
3 |
|
|
a |
v |
2 |
|
|
|
|
|
|||
|
e |
|
|
|
( |
) |
|
( |
|
|
|
|
|
) |
|
|
|
|
||||
|
|
|
|
|
2 |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Похідна (2) буде рівна нулю при a = 0 та a =3/(2v2). Перший випадок відповідає T = ∞ і тому позбавлено фізичного змісту. Отже, шукана температура є T = mv2/(3k).
Задача 19. Визначити сумарну x-складову імпульсу всіх молекул ідеального газу, що проходять через плоский контур площі S за час t у позитивному напрямку осі x, перпендикулярної контуру. Температура газу T, тиск p.
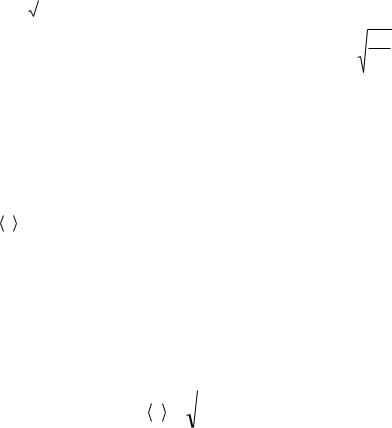
35
Розв’язання.
Число молекул, що проходять через площадку S за час t, швидкості яких перебувають в інтервалі від vx до vx + dvx, дорівнює:
|
|
m |
1 / 2 |
|
dN n St |
|
|||
|
||||
0 |
|
|
|
|
|
|
2 kT |
||
e |
mv 2 |
/(2kT) |
, |
x |
v x dv x |
||
|
|
|
де n0 - концентрація молекул, m - маса однієї молекули. Кожна з цих молекул переносить при цьому імпульс mvx. Тоді шукана складова імпульсу, через контур всіма молекулами, дорівнює:
|
|
|
3 / 2 |
|
2 |
|
|
|
|
|
||
p |
|
|
n0 Stm |
e |
mv x |
/(2kT) |
2 |
dv . |
|
|
||
x |
|
|
|
|
v |
|
|
|
||||
|
|
|
|
|
|
|
||||||
|
|
|
2 kT |
|
|
|
x |
x |
|
|
||
|
|
|
|
0 |
|
|
|
|
|
|
||
Використовуючи табличний інтеграл |
|
|
||||||||||
e x2 x2dx 1 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
0 |
4 |
px 12 n0kTSt 12 pSt.
, одержимо:
3
Задача 20. Знайти середню швидкість молекул ідеального газу.
Розв’язання
Середня швидкість молекул визначається виразом:
v |
|
|
|
|
|
|
|
|
|
a 3 / 2 |
|
av |
2 |
3 |
dv |
|
|
|
||||||
vf(v)dv |
4 |
|
e |
|
|
|
v |
|
|
|
|
|
||||||||||||
|
|
0 |
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
3 / 2 |
|
at |
|
|
|
|
|
|
3 / 2 |
|
|
|
|
|
|
at |
|
|
|
|||
2 |
a |
|
|
|
2 |
a |
|
d |
|
|
|
|
|
|||||||||||
|
|
e |
|
|
t dt |
|
|
|
|
|
|
e |
|
dt |
||||||||||
|
|
da |
|
|||||||||||||||||||||
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
a 3 / 2 |
d |
|
1 |
|
|
|
a |
3 / 2 |
|
1 |
|
|
|
|
2 |
|
|
|
|||||
2 |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
. |
|
||||
|
|
|
|
|
a2 |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
da |
|
a |
|
|
|
|
|
|
|
|
|
( a)1 / 2 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Оскільки a = m/(2k), то |
v |
8kT . |
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
|
|
|
|
|
|
|
|
Задача 21. Концентрація молекул ідеального газу n0 , температура газу T, маса молекул m. Газ перебуває в тепловій рівновазі. Визначити число молекул газу, що вдаряються в одиницю часу об одиницю поверхні посудини.
Розв’язання
Об обрану одиницю поверхні посудини вдаряються ті молекули, проекції швидкості яких на напрямок, перпендикулярний до поверхні, не рівний нулю. Нехай вісь x перпендикулярна до
розглянутої поверхні. Число молекул |
dnx в одиниці об'єму, проекція швидкості яких знаходиться в |
||||||||
інтервалі між vx й vx + dvx , дорівнює: |
|
|
|||||||
|
|
n |
|
m |
1 / 2 |
|
mv 2 / 2kT |
|
. |
dn |
|
|
|
e |
x |
dv |
|||
x |
|
||||||||
|
0 |
|
|
|
|
|
|
x |
|
|
|
|
|
2 kT |
|
|
|
|
|
з цього числа молекул тільки ті досягнуть за одиницю часу поверхні посудини, які розташовані від її не далі відстані, чисельно рівного vx . Число цих молекул визначається виразом
|
|
v |
|
|
|
m |
1 / 2 |
dn' |
x |
x |
n |
|
|
|
|
|
|||||||
|
|
0 |
|
|
|
||
|
|
|
|
|
|
2 kT |
|
e |
mv 2 |
/ 2kT |
dv |
. |
x |
|
|||
|
|
|
|
x |
Повне число молекул, які за одиницю часу досягнуть одиниці поверхні посудини, дорівнює
|
|
|
|
m |
2 |
/ 2kT |
|
|
|
|
|
mv x |
|
||||
|
|
|
1 / 2 |
|
|
. |
||
N v |
|
n |
|
|
e |
|
dv |
|
|
|
|
||||||
0 |
x |
0 |
|
2 kT |
|
|
x |
|
|
|
|
|
|
|
|
|
|
Вводимо позначення a = m/(2k). Тоді:

|
n |
|
|
|
|
av 2 |
|
n |
||
N |
0 |
|
a v e |
x dv |
0 |
|||||
|
|
|
|
|
||||||
|
|
|
0 |
|
x |
|
x |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
av |
2 |
|
1 |
|
|
|
|
|
|
x |
|||
|
|
|
|
|
d |
|
e |
|
||
|
|
|
|
|
||||||
|
2 |
|
|
|
|
|
|
|||
|
|
a |
|
|
|
|
||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
36
|
n |
|
|
|
|
|
|
|
|
|
2kT |
|
|
|
|
||
2 m . |
|
|
|
|
||||
|
0 |
|
|
|
|
|
|
|
|
|
, одержимо N |
n0 |
|
||||
Врахувавши, що середня швидкість молекул v |
8kT |
v . |
||||||
|
|
|
|
|
m |
4 |
|
|
Задача 22. Визначити частку молекул водню, модулі швидкостей яких при температурі 27ос лежать в інтервалі від v2 = 1898 м/с до v1 = 1903 м/с.
Розв’язання
Інтервал швидкостей v = v2 - v1 = 5 м/с досить малий у порівнянні із самими швидкостями. Тому для визначення шуканої частки молекул замість інтегрування можна записати розподіл Максвелла по модулях швидкостей у вигляді:
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
3 / 2 |
|
|
2 |
|
|
|
|
|
|
|
||||
|
|
N |
|
4 |
|
|
|
|
|
|
|
e mv |
|
/(2kT)v 2 v . |
(1) |
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
N |
|
|
|
|
|
|
2 kT |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
Найбільш імовірна швидкість молекул водню при заданій температурі (T = 300 К) дорівнює |
||||||||||||||||||||||||||
|
|
|
|
|
|
. З огляду на це, перетворимо формулу (1) до вигляду: |
|
|||||||||||||||||||||
v |
B |
2kT / m |
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
4 |
|
v 2 |
|
|
v |
2 /v 2 |
v . |
|
|||||||||||||||||
|
|
N |
|
|
|
|
v 3 e |
|
|
B |
(2) |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
B |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
Введемо позначення |
u |
|
v |
. Тоді вираз (2) прийме вигляд |
|
|||||||||||||||||||||
|
|
v B |
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
N |
|
|
4 |
|
|
u |
2 |
e |
u |
2 |
u . |
|
|
|
|
|
|
|
(3) |
|||||||
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
|
= 1.57·103 м/с. |
|||||||||||||||||||||
|
|
Для водню при T = 300 К v B |
|
|
2RT / |
|||||||||||||||||||||||
|
|
|
2kT / m |
|||||||||||||||||||||||||
Отже, u = 1.2, а u v = 3.16·10-3 .
v B
Підставивши ці значення у вираз (3), одержуємо N 2.45·10-3 = 0.245%.
N
Задача 23. Яка частина молекул водню, що перебуває при температурі T , має швидкості, що відрізняються від найбільш імовірної швидкості не більше, ніж на 5 м/с? Задачу розв’язати для двох значень T: 1) 400 K, 2) 900 K.
|
|
|
|
|
Розв’язання |
|
Оскільки в завданні мова йде про найбільш імовірну швидкість, треба вважати v v |
. Отже, |
|||||
|
|
|
|
|
|
B |
u v /v |
B |
= 1 і вираження (3) отримане при рішенні попереднього завдання прийме постій вид: |
||||
|
|
|
|
|||
N |
4 |
|
|
Перш ніж робити розрахунки, необхідно переконатися в тім, що виконується |
||
N |
|
|
|
u . |
||
|
|
e |
|
|
||
|
|
|
||||
умова u v u . v B
Знайдемо спочатку найбільш імовірну швидкість при T1 = 400 K й T2 = 900 K відповідно.
|
|
|
2 8.31 400 |
|
|
|
|
|
|
|
|
v |
|
|
|
м/с = 1.82·103 м/с; v |
|
|
2 8.31 900 |
|
м/с = 2.73·103 м/с. |
||
|
0.002 |
|
|||||||||
B1 |
|
B2 |
0.002 |
||||||||
|
|
|
|
|
|
|
|
||||

37
Оскільки за умовою v = 10 м/с, то одержимо u1=1/182, u 2 = 1/273.
Оскільки u = 1, то умова u u виконується для обох температур. Тепер обчислимо шукані величини:
N |
4 |
|
|
|
|
|
4 |
|
|||
1 |
|
|
u |
|
|
|
0.0046 |
||||
|
|
|
|
|
|||||||
|
|
|
|
1 |
|
|
|||||
|
|
|
|
|
|
||||||
N |
e |
|
|
|
3.14 2.7 182 |
|
|||||
|
|
|
|
|
|||||||
N |
2 |
|
4 |
|
u |
|
|
|
4 |
|
0.0030. |
||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
2 |
|
|
||||||
|
|
|
|
|
|
|
|
||||||
N |
|
|
e |
|
|
|
3.14 2.7 273 |
|
|||||
|
|
|
|
|
|
|
|||||||
Таким чином, при збільшенні температури найбільш імовірна швидкість молекул збільшується, а число молекул, швидкості яких лежать у тому самому інтервалі біля найбільш імовірної, зменшується. На графіку функції розподілу швидкостей (рис. 2.1), зі збільшенням температури максимум кривій зрушується вправо, а величина максимуму зменшується.
Задача 24. Яка частина молекул газу має швидкості, що перевищують найбільш імовірну швидкість?
Розв’язання
Розглянемо молекули, швидкості яких знаходяться в інтервалі від найбільш імовірної швидкості v B , тобто в нескінченно великому інтервалі швидкостей v . Скористаємося функцією
розподілу Максвелла у вигляді dN |
4 |
u2e u 2 du , |
де |
u v /v |
B |
. |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||||
Число молекул, відносні швидкості яких лежать у заданому інтервалі від u1 |
||||||||||||
інтегруючи праву частину (1) у вказаних межах: |
|
|
|
|
||||||||
|
|
|
u |
|
|
|
|
|
|
|
||
dN |
4 |
N 2 u2e u 2 du . |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||||
|
|
|
u1 |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|||
З огляду на те, що відносна швидкість u v /v B |
, |
то в нашому завданні u1 |
||||||||||
Отже, шукана частина молекул виразиться інтегралом:
|
4 |
|
2 |
||
N |
u2e u |
du . |
|||
|
|
||||
N |
1 |
|
|||
|
|
||||
(1)
до u2 знайдемо,
(2)
1 та u2 .
Скористаємося очевидним фактом, що швидкості всіх молекул лежать в інтервалі від 0 до ∞. Тому, якщо позначити через ΔN' число молекул, швидкості яких менше найбільш імовірної, тобто
лежать в інтервалі від 0 |
до 1, то можна записати |
N |
|
N' |
. Таким чином, замість того, щоб |
||||||||
|
|
|
|
|
|
|
|
|
|
N |
N |
1 |
|
шукати N , |
можна знайти N ' по формулі |
|
|
||||||||||
|
|
|
|
||||||||||
|
N |
|
|
|
|
|
|
|
N |
|
|
|
|
N' |
|
4 |
1 |
2 |
|
u 2 |
|
|
|
|
(3) |
||
N |
|
|
|
u |
|
e |
|
du , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
0 |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||
а потім обчислити N 1 N'.
N N
Оскільки інтеграл (3) все-таки в кінцевому вигляді не береться, скористаємося методом наближеного інтегрування. Для цього розкладемо підінтегральну функцію в ряд Маклорена:
u2e u 2 u2 |
u2 |
|
|
|
u6 |
|
|
u8 |
|
u10 |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
Отже, N' |
4 |
1 |
|
|
2 |
|
6 |
1 |
|
24 |
1 |
. |
|||||||||||
|
1 |
1 |
|
1 |
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
5 |
|
|
14 |
|
54 |
|
264 |
|||||||||||||||
|
3 |
|
|
|
|
|
|||||||||||||||||
Обмежуючись першими чотирма членами розкладання, знайдемо з погрішністю, що не

38
перевищує 0.01: |
N' 0.43 . |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
N |
N |
|
|
|
|
|
|
|
|
|
|
|
|
Звідси одержимо відповідь: |
1 0.43 |
0.57. |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|||||
Задача 25. Знайти найбільш імовірну енергію молекул ідеального газу. |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
Розв’язання |
|
|
|
|
|
|
|
Визначимо |
крапку максимуму |
функції |
розподілу молекул |
ідеального газу по енергіях: |
||||||||||||||
f (E) |
2 |
(kT) 3/ 2 e E /(kT) E1/ 2 . |
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
(kT) 3/ 2 e E /(kT) |
|
|
E |
1/ 2 |
|
1 |
|
||
Похідна цієї функції по Е |
f '(E) |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
. |
||||||||||||
|
|
|
|
|
|
|
|
|
|
2E1/ 2 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
kT |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Шукану енергію знайдемо з рівняння f '(E) 0 |
, тобто |
|
E1/ 2 |
|
1 |
0. |
Звідки треба |
|
|
kT |
2E1/ 2 |
|
E |
|
1 kT. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
B |
2 |
|
|
|
|
|
|
|
EB E(v B ) . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
Відзначимо, що |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
Задача 26. Знайти середню кінетичну енергію молекул ідеального газу. |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Розв’язання |
|
|
|
||||||
|
По визначенню середня кінетична енергія |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
E |
|
|
E f (E)dE |
|
2 |
|
|
(kT) 3/ 2 |
e E /(kT) E3 / 2dE . |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Уведемо позначення β = (k)-1 і нову змінну t = E1/2. Тоді |
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
2 |
|
||
|
|
E |
|
4 |
|
3/ 2 |
e t |
|
t |
4 dt |
|
4 |
3/ 2 |
d |
|
|
|
e t |
|
dt . |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
d 2 |
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
||
|
Інтеграл у дужках обчислюється за допомогою інтеграла Пуассона |
||||||||||||||||||||||||||||||||||||
|
|
|
t 2 |
|
|
t 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
/ . |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
e |
|
|
|
|
|
|
dt 2 e |
|
|
|
|
|
dt |
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Використовуючи цю формулу, одержуємо |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
d |
2 |
|
|
|
|
|
2 |
|
2 3/ 2 3 |
5/ 2 |
3 |
1. |
||||||||||||||||
|
|
E |
|
3/ 2 |
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
d 2 |
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
E |
2 kT. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
У такий спосіб |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Задача 27. Обчислити питомі теплоємності при постійному об’ємі cV та постійному тиску c P неону та водню, якщо вважати ці гази ідеальними.
Розв’язання
Питомі теплоємності ідеальних газів виражаються формулами:
cV |
|
i |
|
|
R |
|
, |
|
(1) |
||
|
|
|
|
|
|
|
|
|
|
||
cP |
2 |
|
|
M |
|
||||||
i |
2 |
|
R |
, |
(2) |
||||||
|
|
|
|
|
|
|
|
|
|||
|
|
|
2 |
|
|
|
M |
|
|||

39
де і – число ступенів вільності молекул газу; М – молярна маса. Для неону (одноатомний газ) і =
3; M 20 10 3 |
|
кг |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
моль |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Тоді |
c |
|
3 |
|
|
8.31 |
|
|
Дж |
6,24 |
10 |
2 |
|
|
Дж , |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
V |
|
|
|
2 20 10 3 |
кг К |
|
|
|
|
|
|
|
кг К |
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
c |
|
|
3 2 |
|
|
8.31 |
|
|
|
Дж |
1,04 10 |
3 |
Дж . |
|||||||||||||||||||||||||||
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
2 |
|
|
20 10 3 кг К |
|
|
кг К |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
Для водню (двоатомний газ) і = 5; |
М |
2 10 |
3 кг . |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
моль |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Тоді |
c |
|
5 |
|
|
|
|
8.31 |
|
|
|
Дж |
|
1,04 10 |
4 Дж , |
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
V |
|
|
2 2 |
10 3 кг К |
|
|
|
|
кг К |
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
c |
Р |
|
|
5 |
2 |
|
|
|
8,31 Дж |
1,46 10 |
4 Дж . |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
2 |
|
|
2 10 3 кг К |
|
кг К |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
Задача 28. Певний газ за нормальних фізичних умов має густину 0,0894 кг . Визначити його
м3
питомі теплоємності cV і cР , а також, який це газ?
Розв’язання
|
|
Нормальні фізичні умови: p 105 Па, |
Т 273К . |
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
Для визначення виду газу знайдемо |
його |
|
|
молярну |
масу |
M , скориставшись рівнянням |
||||||||||||||||||||||||||||||||||||||||
Менделєєва-Клапейрона: |
|
|
m |
|
|
, |
звідки |
|
|
|
|
|
|
|
m RT , але |
|
m |
|
густина газу. Тоді знаходимо |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
pV |
|
|
RT |
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
p V |
|
||||||||||||||||||||||
вираз для M |
RT |
. Обчислимо M 0,0894 |
8,31 273 |
|
2 г моль . |
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
p |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
105 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
Це значення молярної маси водню. Отже, |
|
цей газ – водень. Для водню Н2 число ступенів |
||||||||||||||||||||||||||||||||||||||||||||
вільності і = 5. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
Тоді |
|
|
i |
|
|
|
|
|
|
5 8,31 103 |
|
|
|
|
|
|
Дж |
, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
c |
|
|
|
R |
|
M |
|
|
|
|
|
|
10400 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
V |
|
2 |
|
|
|
|
|
|
|
|
|
|
2 2 |
|
|
|
|
|
кг К |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
cР |
i 2 |
R M |
5 2 8,31 103 |
14560 |
|
Дж . |
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
2 |
|
|
|
|
|
2 2 |
|
|
|
кг К |
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
Задача 29. |
|
Визначити кількість теплоти, |
що поглинається воднем масою m 0,2кг при його |
|||||||||||||||||||||||||||||||||||||||||||
нагріванні від температури t1 00 C |
до температури t2 1000 C при постійному тиску. Знайти також |
|||||||||||||||||||||||||||||||||||||||||||||||
зміну внутрішньої енергії газу та виконану роботу. |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
Дано: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Розв’язання |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
m 0.2кг |
|
|
|
|
|
|
|
|
Кількість теплоти |
Q , |
|
|
що поглинається воднем при ізобарному нагріванні |
|||||||||||||||||||||||||||||||||||
t |
|
00 C |
|
|
|
|
|
|
визначається за формулою: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
1 |
1000 C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
t |
2 |
|
|
|
|
|
|
|
Q cPm T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1) |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
H 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
m маса |
|
|
|
|
|
|
|
CP його питома |
|
|
|
|
|
|||||||||||||||||||||
p const |
|
|
|
|
|
|
|
|
де |
газу; |
|
|
теплоємність при постійному тиску; |
|||||||||||||||||||||||||||||||||||
_____________ |
|
|
T зміна температури газу. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
Q ? U ? A ? |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
i 2 R . |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Як |
відомо, |
c |
P |
|
|
|
Підставивши |
цей вираз cP у формулу (1), |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
i 2 |
|
|
|
R T |
|
|
|
|
|
|
|
|
|
2 |
|
|
M |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
отримаємо: Q m |
|
|
, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
M |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
Q |
0.2 5 2 |
8.31 372 273 |
291кДж |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
2 2 10 3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Внутрішня енергія U 2i Mm RT , отже, зміна внутрішньої енергії знаходиться з виразу

|
|
|
|
|
|
|
|
|
40 |
|
U |
i |
|
m |
R T . Підставимо сюди відповідні значення: |
||||||
2 M |
||||||||||
|
|
|
|
|||||||
U |
5 |
|
|
0.2 |
8.31 100 208кДж . |
|
||||
2 2 10 3 |
|
|||||||||
|
|
|
|
|
|
|||||
Роботу розширення газу визначимо за формулою І-го закону термодинаміки: Q A U , звідки |
||||||||||
A Q U . Обчислимо це значення: |
А=291 кДж – 208 кДж = 83кДж. |
|||||||||
Задача 30. Холодильна машина працює за оборотним циклом Карно в інтервалі температур t1 27 C і t2 3 C . Робоче тіло – азот, маса якого m = 0,2 кг. Знайти кількість теплоти, що
відбирається від охолодженого тіла та роботу зовнішніх сил за цикл, якщо відношення максимального об’єму до мінімального дорівнює b = 5.
Дано:
t1 27 C t2 3 C m 0,2кг b 5
Q2 ?
A ?
Розв’язання
Якщо холодильна машина працює за циклом Карно, то ізотермічне стиснення робочого тіла, що супроводжується роботою зовнішніх сил, відбувається при більш високій температурі T1 (дільниця 1–2). При цьому робоче тіло віддає в навколишнє
середовище, що виконує роль термостата, кількість теплоти Q1 . На дільниці 3–4 при більш низькій температурі T2 відбувається ізотермічне розширення робочого тіла, при цьому від тіла, що охолоджується, віднімається кількість теплоти Q2 .
Згідно з першим законом термодинаміки робота за цикл дорівнює повній кількості теплоти, що отримується та віддається за цикл: A Q1 Q2
Як бачимо із графіка, робота газу за цикл у вказаному напрямку від’ємна . Робота зовнішніх сил за цикл:
|
AЗ.С. A Q1 Q2 . |
|
|
|
|
|
|
|
(1) |
||||||||||||||||||
При ізотермічному розширенні |
|
|
|
|
|
|
|||||||||||||||||||||
|
Q2 |
|
m |
RT2 ln |
V4 |
. |
|
|
|
|
|
|
|
|
|
(2) |
|||||||||||
|
|
|
V3 |
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Як бачимо із графіка, мінімальний об’єм за цикл V |
2 |
, |
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
максимальний – |
V4 , а |
V3 |
|
b . |
|
|
|
|
(3) |
||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V2 |
|
|
|
|
|
|
|
|
|||
Другий та третій стан лежать на одній адіабаті, проведеній в інтервалі температур від T |
до T . |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Отже , |
V |
|
|
T |
або V |
T |
1 . (4) |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
2 |
|
|
|
|
2 |
|
2 |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
T1 |
|
|
|
V3 |
|
|
|
|
|
|||||||||
|
|
V3 |
|
|
|
|
|
|
|
|
|
T1 |
|
|
|
|
|||||||||||
Перемноживши почленно рівняння (3) та (4) , отримаємо: |
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
V4 |
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
(5) |
||||||||||
|
|
T2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
b |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
V3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
T1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Підставимо вираз (5) у (2)
|
|
m |
|
|
|
Q |
|
RT |
ln |
||
|
|||||
2 |
|
|
2 |
|
|
|
|
|
|
|
1 |
|
|
T2 |
|
b |
|
ln |
. |
||
|
|
|
|||
|
1 |
|
T1 |
|
|
|
|
|
|||
Азот – газ двохатомний, отже коефіцієнт Пуассона 1,4 тоді Q2 21,6 Дж . Для оборотного циклу справедливе співвідношення:
Q Q |
|
T T |
або |
Q |
|
T . |
(6) |
|
1 2 |
|
1 2 |
|
2 |
2 |
|
|
|
|
Q1 |
T1 |
|
|||||
Q1 |
T1 |
|
|
|||||
|
|
|
|
|||||
Щоб знайти роботу зовнішніх сил за цикл, виразимо Q1 з рівняння (6) та підставимо в рівняння
