
- •МОЛЕКУЛЫ
- •Механическая модель молекулы
- •Волновая функция стационарного состояния
- •Адиабатическое приближение
- •Гармоническое приближение
- •Методы построения Ψэлектр.
- •К какому «атому» принадлежит каждый из 10 электронов?
- •Построение волновой функции молекулы в методе ВС
- •Проблема оптимизации коэффициентов
- •б) пространственная симметрия — волновая функция должна принадлежать одному из неприводимых представлений (типов
- •2)Абсолютная величина коэффициентов при базисных волновых функциях конкретных РФ зависит от их энергий:
- •3)Волновая функция должна быть нормированной.
- •Энергия молекулы в методе ВС
- •J — межатомные кулоновские интегралы (энергии
- •Влияние межъядерного расстояния
- •Энергетическая диаграмма
- •ВЫВОДЫ
- •Теория резонанса
- •Максимальное
- •II. Метод МО (молекулярных орбиталей)
- •Одноядерная потенциальная яма (атом)
- •Электронная оболочка молекулы в методе МО
- •Одноэлектронное приближение
- •Глобальная волновая функция молекулы
- •То же самое можно записать в матрично-векторной форме:
- •Определение коэффициентов разложения Сij
- •Оставшеся после учета симметрии молекулы коэффициенты Сij определяются посредством процедуры самосогласования:
- •Уравнения Хартри-Фока-Рутана
- •Итерационная процедура
- •Варианты метода МО ЛКАО
- •Полная энергия молекулы
- •Орбитальные энергии
- •Энергетические диаграммы
- •Корреляционная диаграмма ± (
- •МО типа А1
- •МО типа В1
- •Корреляционная диаграмма молекулы воды
- •Формула Льюиса
- •Метод МО-КВ
- •КВ для молекулы водорода
- •Уравнения ХФР
- •Локальные характеристики молекул
- •Атомно-молекулярная матрица
- •Индекс свободной валентности
- •PQ-матрицы
- •Поляризуемости
- •Внешние возмущения
- •Возмущения атомов
- •Возмущения связей
- •Все поляризуемости могут быть вычислены через коэффициенты МО невозмущенной молекулы:

Метод МО-КВ
(конфигурационное взаимодействие)
Получаемые результаты можно улучшить, если использовать МНОГОДЕТЕРМИНАНТНЫЕ волновые функции, каждая из которых соответствует своей электронной конфигурации:
Е Е  Е
Е
|
|
φ3 |
|
|
|
|
φ3 |
|
|
φ3 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||||
|
|
φ2 |
|
|
|
|
φ2 |
φ2 |
||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||
|
|
φ1 |
|
|
|
|
φ1 |
|
|
φ1 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||||
ΦI |
|
ΦII |
ΦIII |
|
||||||
ΦМО КВ = CI ΦI + CII ΦII + CIII |
ΦIII |
|||||||||
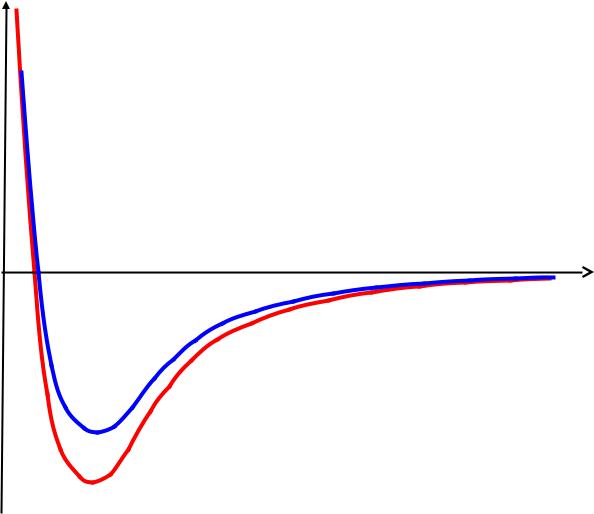
КВ для молекулы водорода
E
Фg = { C1(GG) + C2(UU) } [ – ]
Ф = GG
Rab
Фg = 0,87 GG – 0,50 UU

a |
a |
b |
изолированный |
"атом" в резонансной |
атом |
форме |
A = 1s |
A = 1s* |
МО: МО-КВ
G = A + B |
U = A – B |
|
||
G |
= |
(1s)a + (1s)b |
U = (1s)a – |
(1s)b |
G |
= |
(1s*)a + (1s*)b |
U = (1s*)a – (1s*)b |
|

Уравнения ХФР |
«Канонические МО» (КМО) |
Каждая КМО распространяется на всю молекулу в целом, что отражает тот факт, что любой электрон молекулы может быть найден в любой точке внутри молекулярного объема.
Узловая структура — совокупность узловых поверхностей, разделяющих объем молекулы на части.
Пространственная симметрия — неприводимое представление (тип симметрии) точечной группы молекулы (например, все КМО молекулы воды должны иметь один из четырех типов симметрии группы С2v)
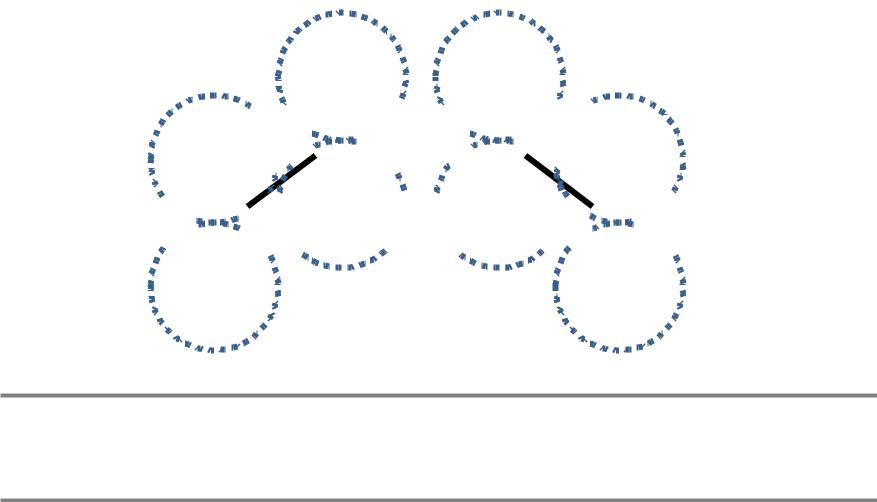
Пример: бутадиен H2C=CH–CH=CH2

 С
С

 С
С


 С
С




 С
С

(2рz)2 |
(2рz)3 |
(2рz)4 |
(2рz)1 |
|
i = Ci1 (2pz)1 + Ci2 (2pz)2 + Ci3 (2pz)3 + Ci4 (2pz)4
(Ci1)2 = (Ci4)2 |
(Ci2)2 = (Ci3)2 |

|
– |
+ |
|
+ |
+ |
– |
– |
– |
|
|
+ |
|
– |
– |
|
+ |
+ |
+ |
+ |
– |
|
|
– |
|
+ |
– |
|
+ |
– |
+ |
– |
– |
|
|
+ |
|
+ |
+ |
|
+ |
– |
– |
+ |
– |
|
|
– |
+ |
+ |
– |
– |
+ |
+ |
– |
– |
++
– –
+ + + +
EМО
4 = – 1,618
3 = – 0,618
2 = + 0,618
1 = + 1,618

|
– |
+ |
|
+ |
+ |
– |
– |
– |
|
|
+ |
|
– |
– |
|
+ |
+ |
+ |
+ |
– |
|
|
– |
|
+ |
– |
|
+ |
– |
+ |
– |
– |
|
|
+ |
|
+ |
+ |
|
+ |
– |
– |
+ |
– |
|
|
– |
A2
z 
B2
|
С2v |
A2 |
A1 |
A2 |
B1
B2
B2
xz
z y
E |
C2z |
xz |
yz |
1 |
1 |
1 |
1 |
1 |
1 |
–1 |
–1 |
1 |
–1 |
1 |
–1 |
1 |
–1 |
–1 |
1 |

Локальные характеристики молекул
Атомно-молекулярная матрица
1-я МО
2-я МО
…..
…..
N-я МО
C1a  C1b
C1b
C2a  C2b
C2b
… …
…
… …
…
CNa  CNb
CNb
атом  атом
атом
… C1N
C1N
… C2N
C2N
… …
…
… …
…
…  CNN
CNN
атом
а |
b |
N |
(Сik)2 = Рik
( вероятность нахождения электрона с номером i в окрестности атома с номером k, или, другими словами, электронная плотность на атоме с номером k, создаваемая электроном с номером i )
i (Сik)2 = Nk
(электронная плотность на атоме с номером k, создаваемая всеми электронами молекулы или среднее число электронов, принадлежащих этому атому )
Nk = –Qk
(электрический заряд той доли электронной оболочки, которая входит в состав атома с номером k )

+Z1  +Z2
+Z2 
 +Z3
+Z3 
 +Z4
+Z4
–Q1  –Q2
–Q2 
 –Q3
–Q3 
 –Q4
–Q4
Zk – Qk = qk
( локальный электрический заряд атома № k )

H2C |
– 0,092 |
фульвен |
– 0,073 |
+ 0,378

 – 0,047
– 0,047
 – 0,073
– 0,073
|
|
– |
– 0,092 |
|
H C |
||||
|
||||
2 |
+ |
|
|
|
