
- •Физические основы механики. Молекулярная физика и термодинамика
- •Оглавление
- •Предисловие
- •Пояснительная записка к тестовым заданиям для проверки качества знаний по физике
- •1. Физические основы механики
- •1.1. Основные понятия, определения и законы классической кинематики
- •1.2. Основные понятия, определения и законы классической динамики
- •1.3. Энергия, работа, мощность. Законы сохранения
- •1.4. Поле тяготения. Движение в поле центральных сил
- •1.5. Волновые процессы
- •1.6. Элементы механики жидкостей и газов
- •1.7. Основы релятивистской механики
- •2. Основы молекулярной физики и термодинамики
- •2.1. Основные понятия молекулярной физики и термодинамики
- •2.2. Основные представления и законы молекулярно-кинетической теории
- •2.3. Основные положения и законы термодинамики
- •2.4. Реальные газы. Фазовые равновесия и превращения
- •2.5. Кинетические явления (явления переноса)
- •Заключение
- •Библиографический список Основной
- •Дополнительный
- •Приложение 1 Физические основы механики. Основные понятия, определения и законы Кинематика и динамика
- •10) Среднее ускорение при неравномерном движении
- •1) В подвижной:
- •2) В неподвижной:
- •В случае переменной массы
- •Волновые процессы. Акустика
- •Энергия, работа, мощность. Законы сохранения в механике
- •Поле тяготения. Движение в поле центральных сил
- •Основы релятивистской механики
- •Приложение 2 Основы молекулярной физики и термодинамики. Основные понятия, определения и законы Конденсированное состояние. Кинематика и динамика жидкостей
- •Основные понятия, определения и законы молекулярной физики и термодинамики
- •Статистический метод исследования
- •Основы термодинамики
- •Реальные газы. Фазовые равновесия и превращения
- •Кинетические явления
- •Приложение 3 Физические величины
- •Приложение 4 Правильные ответы на тестовые задания Физические основы механики
- •Основы молекулярной физики и термодинамики
- •Физические основы механики. Молекулярная физика и термодинамика
- •305040, Г. Курск, ул. 50 лет Октября, 94.
Статистический метод исследования
Статистические закономерности – количественные закономерности, устанавливаемые статистическим методом, в котором рассматриваются лишь средние значения величин, характеризующих данную совокупность молекул (рассматривается конкретная молекулярная модель, и к ней применяются математические методы статистики, основанные на теории вероятностей).
Вероятность термодинамическая – число способов, которыми может быть реализовано данное состояние макроскопической физической системы (предел, к которому стремится относительная частота появления некоторого события при достаточно большом, стремящемся к бесконечности числе повторений опыта при неизменных внешних условиях):
w = n/N,
где N – число опытов;
n – число раз получено определенное событие.
Флуктуации – случайные отклонения физических величин от их среднего значения.
Средняя квадратичная скорость молекул (для газа массой m, находящегося в состоянии равновесия, при T = const) остаётся постоянной:
 или
или
 ,
,
где Ni – число молекул, обладающих скоростью vi;
N – число всех молекул.
Наиболее вероятная скорость – скорость движения молекул, которая характеризует положение максимума функции распределения Максвелла:

Средняя арифметическая скорость

Относительная скорость применяется для расчета числа молекул, движущихся со скоростями в интервале от v до v + dv:
u = v/vв.
Закон распределения молекул идеального газа по скоростям в стационарном состоянии (распределение Максвелла):

где dnv – среднее число молекул в единице объема со скоростями в интервале от v до v + dv;
n – число молекул в единице объема.
Функция распределения (доля молекул от их общего числа отнесена к некоторому интервалу скоростей):

или
![]()
где dnv/ndv – функция распределения.
Свободные пробеги молекул – прямолинейные участки траектории, проходимые молекулой между двумя последовательными соударениями.
Средняя длина свободного пробега молекулы – среднее расстояние, проходимое молекулой между двумя соударениями:

где Z – число соударений;
v – средняя скорость молекулы;
k – постоянная Больцмана;
d – диаметр молекулы;
p – давление;
T – абсолютная температура.
Среднее число соударений <z> – число соударений молекул, численно равное отношению средней скорости движения молекул <v> к средней длине свободного пробега:
 ,
или
,
или
![]()
Эффективный диаметр молекулы d – минимальное расстояние, на которое сближаются при столкновении центры 2–х молекул.
Эффективное сечение – величина равная
= d2.
Барометрическая формула показывает, что давление убывает с высотой тем быстрее, чем тяжелее газ и чем ниже его температура:
![]()
Закон распределения молекул газа по высоте в поле сил тяготения (распределение Больцмана):
![]() ,
,
![]() ,
,
где no – число молекул в единице объема в том месте, где потенциальная энергия молекул равна нулю;
n – число молекул в единице объема в тех точках пространства, где потенциальная энергия молекул равна Wp.
Распределение Максвелла–Больцмана – благодаря этому распределению можно определить долю молекул идеального газа, имеющих скорости в интервале от v до v + dv и обладающих потенциалом = gh во внешнем силовом поле:
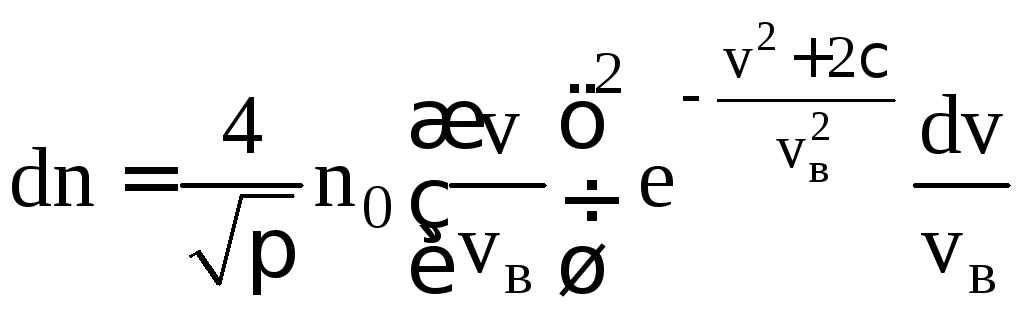 ,
,
где vв – наиболее вероятная скорость, значению которой соответствует максимум кривой Максвелла.
Зависимость плотности газа от высоты:
![]() ;
;
![]() ,
,
где mo – масса одной молекулы.
