
- •IV часть курса физики Молекулярная физика и термодинамика Введение
- •Лекция 1,2. Молекулярно - кинетическая теория газов
- •1.1. Основные понятия. Уравнение состояния
- •1.2. Вывод основного уравнения мокулярно-кинетической теории
- •1. 3. Молекулярно-кинетическое толкование температуры
- •1.4. Статистические распределения
- •1.5. Барометрическая формула. Классическое распределение Максвелла-Больцмана
- •1.6. Явления переноса
- •Лекция 3. 4. Основы термодинамики
- •3.1. Основные понятия
- •3.2. Работа в термодинамике
- •3.4. Количество теплоты. Первое начало термодинамики
- •Для бесконечно малых процессов
- •3.5. Теплоёмкость
- •3.6. Внутренняя энергия и теплоёмкость идеального газа
- •3.7. Адиабатный процесс
- •3.8 Обратимые и необратимые процессы. Второе начало термодинамики
- •1) (Формулировка Клазиуса) Невозможен процесс, единственным результатом которого является передача теплоты от холодного тела к горячему.
- •3.9. Циклы. Тепловая и холодильная машины
- •3.10. Цикл Карно
- •Энтропия
- •Статистический смысл энтропии и второго начала термодинамики
- •Лекция 5. Фазовые равновесия и фазовые превращения
- •Взаимодействие молекул реальных газов
- •Уравнение состояния Ван-дер-Ваальса
- •Изотермы реальных газов. Фазы. Фазовые переходы.
- •1. Участок ее` соответствует газообразному состоянию вещества. По мере сжатия газа давление растет до точки е.
- •Фазовые диаграммы р - т. Тройная точка
- •Поверхностное натяжение жидкости
- •Элементы физики твердого тела Лекция 6. Элементы квантовой статистики
- •6.1. Особенности квантовых статистик
- •6.2. Фазовое пространство. Ячейка фазового объема.
- •6.3. Принцип неразличимости тождественных частиц. Фермионы и бозоны
- •6.4. Функции распределения Ферми –Дирака и Бозе –Энштейна
- •6.5. Понятие о вырождении.
- •6.6. Вырожденный Ферми-газ в металлах
- •Лекция 7,8. Тепловые свойства кристаллов
- •7.1. Строение кристаллов. Дефекты
- •7.2. Классическая теплоемкость кристаллов по Дюлонгу и Пти
- •7.3. Квантовая теория теплоемкости Дебая
- •7.4. Теплоемкость электронного газа в металлах
- •9.3. Недостатки классической теории Друде-Лоренца
- •9.4. Понятие о квантовой теории электропроводности металлов
- •Элементы зонной теории кристаллов
- •9.6. Собственная проводимость проводников. Электроны проводимости и дырки
- •9.7. Примесная проводимость п/п. Электронный и дырочный п/п.
- •9.8. Р / n переход.
- •9.10. Понятие о сверхпроводимости
- •Лекция 11. Атомное ядро
- •11.1. Строение атомных ядер
- •Свойства ядер
- •11.3 Ядерные силы.
- •Законы радиоактивного распада
- •Ядерные реакции
- •Лекция12. Элементарные частицы и современная физическая картина мира
- •Элементарные частицы
- •Элементарные частицы
- •Свойства элементарных частиц
- •Классы элементарных частиц.
- •Физическая картина мира
- •Основные формулы
- •Вопросы для подготовки к зачету
Статистический смысл энтропии и второго начала термодинамики
Рассмотрим 3 молекулы, находящиеся в сосуде, условно разделённым на 2 части (см. рис.3.8).
М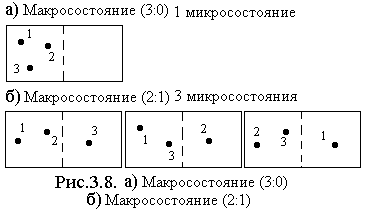 акросостоянием
назовём описание всей системы, а
микросостоянием
- описание
положения каждой молекулы.
акросостоянием
назовём описание всей системы, а
микросостоянием
- описание
положения каждой молекулы.
Макросостоянию (3:0) соответствует всего =1 возможное микросостояние (см. рис.3.8.а). Макросостоянию (2:1) соответствуют =3 возможных микросостояния (см. рис.3.8.б). - называют статистическим весом данного макросостояния системы. равно числу возможных микросостояний, соответствующих данному макросостоянию.
В нашем примере 2-е макросостояние (2:1) более вероятно, чем 1-е (3:0).
Больцман
доказал, что статистический вес
и энтропия S
связаны соотношением: ![]() (3.23)
(3.23)
где k - постоянная Больцмана.
Следовательно, закон неубывания энтропии (2-е начало термодинамики) означает, что изолированная термодинамическая система должна последовательно переходить в состояние со все большим статистическим весом. А после того, как достигнет = max, может оставаться в этом равновесном состоянии бесконечно долго.
По 2-му началу термодинамики обратный процесс уменьшения энтропии в изолированной системе (и уменьшения статистического веса ) запрещён. (Молекулы не могут самопроизвольно собраться в одной половине сосуда).
В этом заключается статистический смысл энтропии и 2-го начала термодинамики. В теории флуктуаций такое возможно. Там 2-е начало не выполняется.
Лекция 5. Фазовые равновесия и фазовые превращения
Взаимодействие молекул реальных газов
В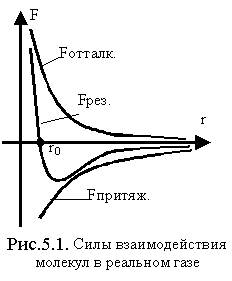 отличие от идеального газа в реальном
газе молекулы взаимодействуют друг с
другом. Силы отталкивания
отличие от идеального газа в реальном
газе молекулы взаимодействуют друг с
другом. Силы отталкивания![]() очень
быстро возрастают, начиная с некоторыхr0- расстояний между
центрами молекул (см. рис.5.1).
очень
быстро возрастают, начиная с некоторыхr0- расстояний между
центрами молекул (см. рис.5.1).
Силы
притяжения
![]() изменяются
с расстоянием медленнее (см. рис.5.1).
Поэтому на расстояниях
изменяются
с расстоянием медленнее (см. рис.5.1).
Поэтому на расстояниях![]()
![]() и молекулы притягиваются другу
(Ван-дер-Ваальсовы силы притяжения).
и молекулы притягиваются другу
(Ван-дер-Ваальсовы силы притяжения).
Потенциальная
энергия взаимодействия
![]() представлена на рис. 5.2..
представлена на рис. 5.2..
С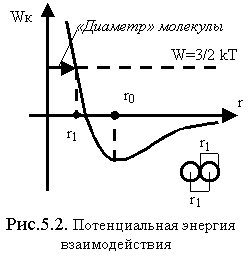 редняя
кинетическая энергия теплового
поступательного движения молекул
редняя
кинетическая энергия теплового
поступательного движения молекул![]() .
При этом молекулы могут сблизиться до
расстояния
.
При этом молекулы могут сблизиться до
расстояния![]() .
(С повышением температуры
.
(С повышением температуры![]() убывает очень слабо, см. рис. 5.2).
убывает очень слабо, см. рис. 5.2).
Расстояние
![]() называют
эффективным
диаметром
молекул.
называют
эффективным
диаметром
молекул.
Т.
к.
![]() ,
то молекулы в потенциальной яме не
остаются, и (за счет теплого движения)
вблизи друг от друга (приr
= r0)
не задерживаются.
,
то молекулы в потенциальной яме не
остаются, и (за счет теплого движения)
вблизи друг от друга (приr
= r0)
не задерживаются.
Итак, реальные молекулы имеют конечный размер и при обычных условиях испытывают некоторое притяжение.
Уравнение состояния Ван-дер-Ваальса
К чему приводит конечный размер молекул и их взаимное притяжение?
Т. к. молекулы имеют конечный объем, то в сосуде свободным останется не весь объем сосуда V, а объем (V - в), где в - поправка, определяемая объемом молекул.
П
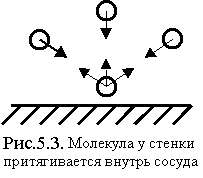 ритяжение
молекул между собой приводит к тому,
что молекулы, находящиеся у стенки,
испытывают притяжение внутрь сосуда
иударяют
по стенкам слабее, чем в случае идеального
газа (как бы тормозятся пружиной) (см.
рис.5.3)
ритяжение
молекул между собой приводит к тому,
что молекулы, находящиеся у стенки,
испытывают притяжение внутрь сосуда
иударяют
по стенкам слабее, чем в случае идеального
газа (как бы тормозятся пружиной) (см.
рис.5.3)
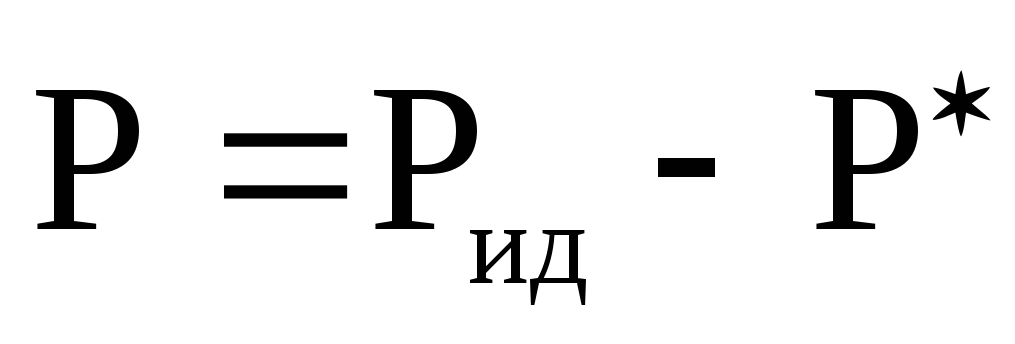 ,
,
где Р- давление в реальном газе, Рид – давление идеального газа. Поправка Р* пропорциональна:
n концентрации оттягивающих молекул,
n числу молекул в пограничном слое
В
итоге
![]() (т. к.
(т. к.![]() концентрация обратно пропорциональна
объему данного газа). Получаем давление
идеального газа:
концентрация обратно пропорциональна
объему данного газа). Получаем давление
идеального газа:![]()
Вводя эти поправки в уравнение Менделеева-Клапейрона, Ван-дер-Ваальс получил уравнение состояния для 1 моля реального газа:
![]() (уравнение
состояния для 1 моля реального газа)
(5.1.)
(уравнение
состояния для 1 моля реального газа)
(5.1.)
где V - объем, занимаемый одним молем газа, а,b - константы, зависящие только от вида газа.
Для произвольного числа молей =m/μ объем V=Vμ m/μ, и уравнение состояния принимает вид:
![]() (для
=m/μ
молей реального
газа) (5.2)
(для
=m/μ
молей реального
газа) (5.2)
