
- •1.Кинематика материальной точки
- •2. Три закона Ньютона Первый закон Ньютона
- •Третьей закон Ньютона
- •Законы изменения и сохранения момента импульса системы
- •5. Поступательное и вращательное движение твердого тела
- •6. Момент инерции
- •8. Гидромеханика. Уравнение Навье - Стокса
- •[Править]Уравнения Навье — Стокса
- •9. Гармонические колебания
- •10. Волны и уравнение гельмгольца Уравнения Гельмгольца. Волновой характер электромагнитного поля
- •11. Интерференция
- •Расчет результата сложения двух сферических волн [править]
- •Когерентность волн [править]
- •12. Дифракция
- •13. Поляризация
- •Поляризация монохроматических волн [править]
- •14. Формула Планка
- •15. Атом Бора
- •Полуклассическая теория Бора[править]
- •Формула Зоммерфельда — Дирака[править]
14. Формула Планка
Формула
Планка —
выражение для спектральной плотности
мощности (Спектральной Плотности
Энергетической Светимости) излучения
абсолютно чёрного тела, которое было
получено Максом
Планком.
Для плотности энергии излучения ![]() :
:![]()
Формула Планка
(«форма» зависимости ![]() от
частоты и температуры) первоначально
была «выведена» эмпирически. Формула
Планка была получена после того, как
стало ясно, что формулаРэлея—Джинса,
которая следует из классической теории
электромагнитного поля, удовлетворительно
описывает излучение только в области
длинных волн. С убыванием длин волн
формула Рэлея—Джинса сильно
расходится с эмпирическими данными.
Более того, в пределе она даёт расхождение —
бесконечную энергию излучения
(ультрафиолетовая
катастрофа).
В связи с этим Планк в 1900 году сделал
предположение, противоречащее классической
физике, о том, что электромагнитное
излучение испускается в виде отдельных
порций энергии (квантов), величина
которых связана с частотой излучения
выражением:
от
частоты и температуры) первоначально
была «выведена» эмпирически. Формула
Планка была получена после того, как
стало ясно, что формулаРэлея—Джинса,
которая следует из классической теории
электромагнитного поля, удовлетворительно
описывает излучение только в области
длинных волн. С убыванием длин волн
формула Рэлея—Джинса сильно
расходится с эмпирическими данными.
Более того, в пределе она даёт расхождение —
бесконечную энергию излучения
(ультрафиолетовая
катастрофа).
В связи с этим Планк в 1900 году сделал
предположение, противоречащее классической
физике, о том, что электромагнитное
излучение испускается в виде отдельных
порций энергии (квантов), величина
которых связана с частотой излучения
выражением:
![]()
Коэффициент
пропорциональности ![]() впоследствии
назвалипостоянной
Планка,
впоследствии
назвалипостоянной
Планка, ![]() =
1.054 · 10−27 эрг·с.
Это предположение позволило объяснить
наблюдаемый спектр излучения теоретически.
=
1.054 · 10−27 эрг·с.
Это предположение позволило объяснить
наблюдаемый спектр излучения теоретически.
Правильность формулы Планка подтверждается не только непосредственной эмпирической проверкой, но и следствиями из данной формулы, в частности из неё следует закон Стефана-Больцмана, также эмпирически подтверждённый. Кроме того, из неё выводятся также и приблизительные формулы, полученные до формулы Планка, — формула Вина и формула Рэлея-Джинса.
ЭТО НЕ ВСЕ ЧТО НУЖНО !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
15. Атом Бора
Бо́ровская
моде́ль а́тома (Моде́ль Бо́ра) —
полуклассическая модель атома,
предложенная Нильсом
Бором в
1913 г. За основу он взял планетарную
модель атома, выдвинутую Резерфордом.
Однако, с точки зрения классической
электродинамики, электрон в модели
Резерфорда, двигаясь вокруг ядра, должен
был бы излучать непрерывно
и очень быстро, потеряв энергию, упасть
на ядро. Чтобы преодолеть эту проблему
Бор ввел допущение, суть которого
заключается в том, что электроны в атоме
могут двигаться только по определенным
(стационарным) орбитам, находясь на
которых они не излучают, а излучение
или поглощение происходит только в
момент перехода с одной орбиты на другую.
Причем стационарными являются лишь те
орбиты, при движении по которым момент
количества движения электрона равен
целому числу постоянных
Планка[1]: ![]() .
.
Используя
это допущение и законы классической
механики, а именно равенство силы
притяжения электрона со стороны ядра
и центробежной силы, действующей на
вращающийся электрон, он получил
следующие значения для радиуса
стационарной орбиты ![]() и
энергии
и
энергии![]() находящегося
на этой орбите электрона:
находящегося
на этой орбите электрона:
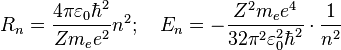
Здесь ![]() —
масса электрона, Z — количество
протонов в ядре,
—
масса электрона, Z — количество
протонов в ядре,![]() —диэлектрическая
постоянная,
e — заряд электрона.
—диэлектрическая
постоянная,
e — заряд электрона.
Именно такое выражение для энергии можно получить, применяя уравнение Шрёдингера, решая задачу о движении электрона в центральном кулоновском поле.
Радиус первой
орбиты в атоме водорода R0=5,2917720859(36)·10−11 м[2],
ныне называется боровским
радиусом,
либо атомной
единицей длины и
широко используется в современной
физике. Энергия первой орбиты ![]() эВ представляет
собой энергию
ионизации атома
водорода.
эВ представляет
собой энергию
ионизации атома
водорода.
