
- •Министерство сельского хозяйства Российской Федерации
- •Введение.
- •Лекция 1 механика
- •1.1 Предмет физики.
- •1.2. Основные математические понятия
- •Приращение функции – изменение функции.
- •Основные свойства производной:
- •Градиент функции.
- •Международная система единиц «си»
- •1.3. Основы теории погрешности
- •1.4. Кинематика. Основные параметры простейших видов движения
- •Параметры вращательного движения:
- •Характеристики колебательного движения
- •1.5.Основные динамические характеристики
- •Физическая природа сил.
- •1.6.Основные законы динамики.
- •Закон сохранения импульса
- •Закон изменения импульса
- •Работа. Мощность. Энергия.
- •Закон сохранения энергии (для изолированной системы).
- •Полная энергия гармонических колебаний.
- •Вопросы для самоконтроля.
- •Список литературы Основная
- •Лекция 2 гидростатика. Гидродинамика
- •1.1.Основные законы гидростатики
- •1.2. Основные понятия и законы гидродинамики.
- •Закон Ньютона для внутреннего трения.
- •Закон Стокса.
- •Закон Пуазейля.
- •Принцип аэрации почвы.
- •1.3. Свойства жидкости.
- •Поверхностное натяжение.
- •Поверхностно активные вещества
- •1.4. Жидкость в капиллярах.
- •Вопросы для самоконтроля
- •Список литературы
- •Основные уравнения мкт.
- •Основные процессы и понятия.
- •Экспериментальные газовые законы.
- •Понятие идеального газа
- •Изотермы Ван-дер-Ваальса.
- •1.4.Диффузия
- •1.5.Теплопроводность
- •1.6.Внутреннее трение
- •Уравнение Ньютона.
- •1.7.Уравнение переноса в общем виде.
- •Лекция 4 термодинамика
- •1.1.Понятие числа степеней свободы
- •1.2.Основные понятия термодинамики
- •Уравнение Майера
- •Показатель адиабаты
- •1.3.Основные законы термодинамики
- •1.4.Работа при термодинамических процессах.
- •Работа при изотермическом процессе.
- •Работа при изобарическом процессе.
- •Работа при адиабатическом процессе.
- •1.5.Тепловая машина. Цикл Карно.
- •Свойства энтропии.
- •Вопросы для самоконтроля.
- •Список литературы Основная
- •Лекция 5
- •Теорема Остроградского – Гаусса.
- •Принцип суперпозиции.
- •1.2.Работа электрического поля. Потенциал электрического поля.
- •Связь напряженности и потенциала.
- •Теорема Ирншоу.
- •1.3.Проводники и диэлектрики в электрическом поле.
- •Диэлектрики в электрическом поле.
- •1.4.Электрическая емкость. Конденсатор.
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Лекция 6 электрический ток
- •1.1.Понятие электрического тока и условия его существования.
- •1.2.Параметры электрического тока.
- •1.3.Основные законы
- •Электрический ток в электролитах
- •Зависимость сопротивления электролитов от температуры.
- •1.5..Электрический ток в полупроводниках. Полупроводниковые приборы.
- •Полупроводниковый диод p-n переход.
- •Полупроводниковый триод
- •1.6.Электрический ток в газах.
- •Вольт-амперная характеристика газового разряда.
- •1.7. Термоэлектронная эмиссия. Электровакуумные приборы.
- •Полупроводниковый триод.
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Лекция 7 Магнетизм и электромагнетизм
- •1.1.Параметры магнитного поля.
- •1.2.Основные формулы и законы.
- •Закон Ампера.
- •1.3. Действие магнитного поля на проводник с током.
- •1.4 Виды магнетиков. Гистерезис.
- •1.5. Явление электромагнитной индукции. Закон Фарадея.
- •Закон Фарадея.
- •Правило Ленца.
- •1.6.Получение переменного тока
- •1.7.Явление взаимной индукции и самоиндукции.
- •Резистор в цепи переменного тока:
- •Конденсатор в цепи переменного тока:
- •Сопротивление конденсатора в цепи переменного тока.
- •Катушка индуктивности в цепи переменного тока.
- •Зависимость индуктивного и емкостного сопротивления от частоты тока.
- •Обобщенный закон Ома
- •1.9.Резонанс в цепи переменного тока.
- •1.10.Колебательный контур
- •1.11.Электромагнитные волны
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Лекция 8 Оптика
- •1.1. Природа света.
- •1.2.Геометрическая оптика.
- •Закон отражения.
- •1.3.Элементы волновой оптики Дисперсия
- •Интерференция.
- •Дифракция.
- •Условия интерференционного максимума и минимума.
- •Поляризация.
- •Основные фотометрические характеристики.
- •1.4.Фотоэффект и законы внешнего фотоэффекта
- •1.5.Люминесценция
- •Правило Стокса.
- •1.6.Световое давление
- •1.7. Излучение и поглощение света веществом.
- •1.8.Законы излучения абсолютно черного тела.
- •Вопросы для самоконтроля
- •Список литературы
- •1.2.Виды радиоактивного излучения
- •1.3.Энергия связи. Дефект массы атомного ядра.
- •1.4.Виды ядерных реакций
- •Применение ядерной энергии.
- •Вопросы для самоконтроля
- •Список литературы Основная
- •Содержание
Лекция 4 термодинамика
1.1.Понятие числа степеней свободы
Понятие числа степеней свободы. Числом степеней свободы называется число независимых координат, определяющих положение молекулы или тела в пространстве. Молекулы в газах движутся беспорядочно, при этом они совершают поступательный и вращательный вид движения.
Максимальное число степеней свободы молекул = 6 (3 поступательных и 3 вращательных степеней свободы).
Одноатомная молекула имеет три поступательных степени свободы. При вращении одноатомной молекулы относительно ее центра, ее положение в пространстве не изменяется, значит, вращательные степени свободы у одноатомных молекул = 0.
Двухатомные молекулы имеют пять степеней свободы: 3 поступательных и 2 вращательных, вращается относительно осей одной линии связи атомов.
Трех и более атомные молекулы имеют все шесть степеней свободы.
Число степеней свободы молекулы – j.
1.2.Основные понятия термодинамики
Внутренняя энергия вещества называется суммарная кинетическая энергия всех молекул этого тела.
Внутренняя энергия определяется температурой, а так же от рода вещества.
Внутренняя
энергия вещества -
![]() .
.
Внутренняя энергия вещества распределяется по степеням свободы равномерно.
Внутренняя энергия зависит от удельной теплоемкости вещества.
Теплоемкость – это способность вещества накапливать или принимать тепло. Удельная теплоемкость – определяется количеством теплоты, которую нужно сообщить единицы массы, чтобы увеличить его температуру на один Кельвин.
![]()
![]()
Удельная теплоемкость газов зависит от условий, при которых газ нагревается.
Газ можно нагревать при двух условиях:
при постоянном давлении (в этом случае, рассматривается теплоемкость газа при постоянном давлении (Ср.));
при постоянном объеме (удельная теплоемкость газа при постоянном объеме (СV)).
Ср больше, чем СV на величину работы, которую совершает газ при нагревании постоянном давлении.
Физический смысл универсальной газовой постоянной. Универсальная газовая постоянная численно равна работе, совершаемой одним молем газа при нагревании его на один Кельвин.
Уравнение Майера
![]()
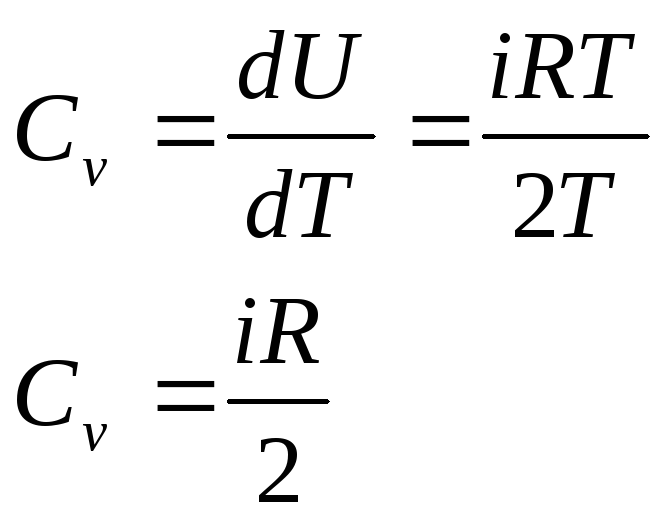
![]()
Получим
отношения
![]() к
к![]() через число степеней свободы:
через число степеней свободы:
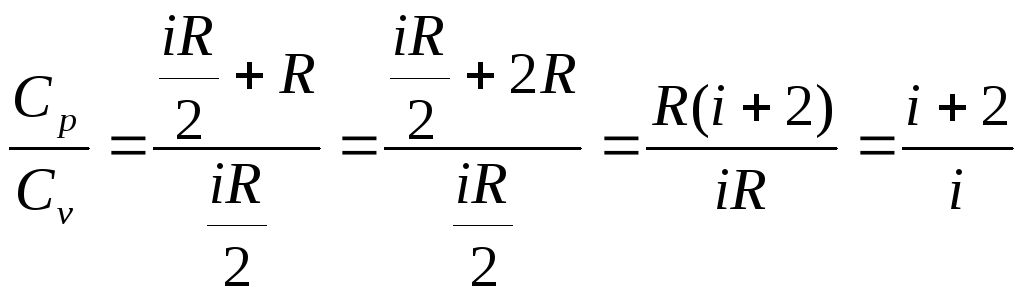
Показатель адиабаты
Состояние газа характеризуется тремя параметрами: Т, P, V.
Термодинамический процесс – это переход системы из одного состояния в другое, в результате которого изменяются параметры P, V, T.
Термодинамика базируется на двух основных законах, называемых началами термодинамики.
1.3.Основные законы термодинамики
Первое начало термодинамики – это все количество теплоты, переданное системе, расходуется на изменение ее внутренней энергии и совершение работы.
![]()
Изобразим PV диаграмму циклического (периодического) процесса (рис.30), при котором система, проходя ряд термодинамических состояний, возвращается в исходное состояние.
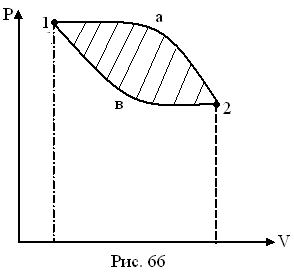
Рисунок 30.
![]()
Система не может совершать работу большую, чем переданное ей тепло.
Термодинамические процессы бывают обратимыми и необратимыми. Обратимый (идеализированный) процесс, при котором система, пройдя ряд термодинамических состояний, возвращается в исходное и при этом никаких изменений не происходит.
Все термодинамические процессы необратимы.
Адиабатический процесс – это процесс, протекающий без теплообмена между системой и окружающей средой.
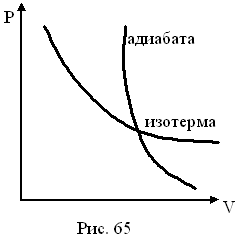
Рисунок 31.
На PV- диаграммах адиабата изображается круче изотермы (рис31).
Изменение давления при адиабатическом процессе происходит не только за счет изменения объема, как это происходит при изотермическом процессе, но и за счет изменения температуры.
