
- •Лекційний курс з дисципліни
- •2. Становлення та розвиток мікробіології.
- •2.1. Морфологічний період розвитку мікробіології
- •2.2. Еколого-фізюлогічний період розвитку мікробіології.Відкриття луї пастера.
- •2.3. Відкриття роберта коха. Розробка методів досліджень
- •2.4. Внесок у розвиток мікробіології вітчизняних учених
- •2.5. Розвиток мікробіології у XX ст.
- •3.Положення мікроорганизмів у природі.
- •3.1. Прокаріоти та еукаріоти.
- •3.2. Загальні властивості мікроорганізмів
- •Тема 2: морфологія та будова прокаріотної клітини.
- •2. Будова мікробної клітини.
- •2.1. Клітинна стінка мікроорганізмів та її поверхневі структури.
- •2.2. Мембрани мікробних клітин. Цитоплазматична мембрана.
- •2.3. Мембранні утворення у прокаріот.
- •2.4. Внутрішньоклітинні структури.
- •3. Ендоспори та інші форми спокою у бактерій.
- •3.1. Характеристика спороутворювальних бактерій.
- •3.2. Спороутворення (споруляція)
- •3.3. Інші форми спокою (цисти, екзоспори, міксоспори)
- •4. Відмінності прокаріот та еукаріот.
- •1. 1. Фізичні фактори.
- •1.2. Хімічні фактори.
- •1.3. Методи стерилізації.
- •2. Адаптивні реакції мікроорганізмів на стресові дії.
- •3.Хімічний склад бактеріальної клітини.
- •4. Живлення мікроорганізмів.
- •5. Фізіологія росту та розмноження бактерій.
- •Тема 4: систематика прокаріот.
- •1.1. Термінологія, що використовується в систематиці.
- •1.2. Концепція виду в бактеріології.
- •1.3. Історичні аспекти систематики бактерій.
- •3.1. Фенотипова систематика.
- •3.2.Геносистематика бактерій.
- •3.3. Філогенетична класифікація.
- •Тема 5: генетика мікроорганізмів.
- •1.Організація генетичного матеріалу бактерії.
- •2.Мінливість мікроорганізмів.
- •3.Генетичні рекомбінації.
- •4.Практичне значення генетики бактерій.
- •Тема 6: механізми обміну речовин і перетворення енергії у мікроорганізмів.
- •2. Біосинтетичні процеси у мікроорганізмів
- •3.Типи бродіння.
- •4. Перенесення електронів в анаеробних умовах (анаеробне дихання).
- •5. Використання неорганічних донорів водню: аеробні хемолітотрофні бактерії
- •6. Фіксація молекулярного азоту
- •7. Фототрофні бактерії та фотосинтез.
- •Тема 7: мікроорганізми і навколишнє середовище.
- •2. Типи взаємовідносин між організмами в природі.
- •3. Екологія мікроорганізмів.
- •4. Мікрофлора організму людини. Патогенні мікроби. Токсини. Інфекція.
- •5. Еволюція мікроорганізмів.
7. Фототрофні бактерії та фотосинтез.
Здатність використовувати світло як джерело енергії, необхідної для росту, притаманна двом групам бактерій, які принципово відрізняються одна від одної.
Перша група включає пурпурові та зелені бактерії. Згідно з дев'ятим виданням Керівництва Бергі з систематики бактерій ці бактерії належать до класу Anoxyphotobacteria. Вони не можуть використовувати воду як донор водню (як це роблять зелені рослини), їм потрібні донори з більш високим ступенем відновлення (сірководень, водень або органічні сполуки). У зв'язку з цим фотосинтез у них проходить без виділення кисню (аноксигенний фотосинтез). Бактерії цієї групи — типові водні організми, які існують як у прісній, так і морській воді. їх червоне, оранжеве чи зелене забарвлення зумовлене наявністю хлорофілів і каротиноїдів.
Друга група включає ціанобактерії. Вони використовують воду як донор водню і виділяють кисень, тобто здійснюють оксигенний фотосинтез. Процес фотосинтезу у ціанобактерій не відрізняється від фотосинтезу у зелених рослин. Пігментна система ціанобактерій містить хлорофіл а, каротиноїди та фікобілілротеїни.
ХАРАКТЕРИСТИКА ПУРПУРОВИХ І ЗЕЛЕНИХ БАКТЕРІЙ
Згідно з дев'ятим виданням Керівництва Бергі з систематики бактерій клас Anoxyphotobacteria складається з двох порядків . Перший порядок Rhodospirillales (пурпурові бактерії) об'єднує родини Rhodospirillaceae (несіркові пурпурові бактерії) та Chroraatiaceae (сіркові пурпурові бактерії). Другий порядок Chlorobiales (зелені бактерії) об'єднує родини Chloro-biaceae (зелені сіркові бактерії) та Chloroflexaceae. Морфологіячно різноманітна група — коки, палички, вигнуті форми (спірили, вібріони), рухливі та нерухливі.
Після проведеного в середині 80-х років XX ст. аналізу 16S рРНК у прокаріот зелені фотобактерії увійшли до складу групи 9 (Chloroflexus) і групи 10 (Chlorobium), а пурпурові бактерії — до групи 11, яка була виділена у 1988 р. в окремий клас Proteobacteria.
У книзі "Prokaryotes" (1999 p.) зелені фототрофні бактерії родини Chlorobiaceae розміщені в розділі 5, представники родини Chloroflexaceae — у розділі 7. Пурпурові фототрофні бактерії входять до складу частини С: Proteobacteria.
Пурпурові бактерії. Спільним для представників порядку Rhodospirillales є те, що їх фотосинтетичний апарат (світлозбирні системи та реакційні центри) міститься на внутрішніх мембранах (тилакоїдах), які утворюються з інвагінацій плазматичної мембрани. Тилакоїдні структури можуть бути везикулярні, трубчасті та пластинчасті (ламелярні). Типовим хлорофілом для цих бактерій є хлорофіл а. Фіксація СО2 відбувається у циклі Кальвіна. Пурпурові бактерії здатні використовувати органічні сполуки як донори водню та/або джерела вуглецю.
За здатністю використовувати як донор електронів елементну сірку пурпурові бактерії поділяються на сіркові та несіркові. Типовим видом пурпурових сіркових бактерій є Chromatium vinosum, несіркових — Rhodospirillum rubrum. Сіркові бактерії можна легко розпізнати за внутрішньоклітинними включеннями сірки (мають вигляд кульок, які сильно заломлюють світло).
Зелені бактерії. Для цих бактерій характерна наявність хлоросом — органел, які прилягають до цитоплазматичної мембрани та містять характерний світлозбирний пігмент — бактеріохлорофіл (с, d або е). Крім того, вони містять невелику кількість і бактеріохлорофілу а, який прямо пов'язаний з фотосинтетичними реакційними центрами і локалізований у цитоплазматичній мембрані. Зелені бактерії не здатні фіксувати вуглекислий газ у циклі Кальвіна (у них немає ферменту рибулозодифосфаткарбоксилази). Асиміляція СО2 відбувається через відновлювальний цикл трикарбонових кислот.
Типовим видом зелених сіркових бактерій є Chlorobium limicola, несіркових бактерій — Chloroflexus aurantiacus.
Особливості метаболізму пурпурових і зелених бактерій. Цим бактеріям притаманний різнобічний метаболізм. Так, багато які пурпурові несіркові бактерії здатні як до анаеробного росту на світлі, так і до аеробного в темноті (за рахунок органічних субстратів). Інші групи представлені строгими анаеробами і облігатними фототрофами. Багато які види використовують як донор водню молекулярний водень (представники родів Rhodobacter, Chromatium, а також родоспірили та Chlorobium ростуть на світлі, використовуючи Н2 і СО2). Деякі види цих бактерій здатні використовувати як донор водню (електронів) сірководень, елементну сірку. Спостерігається асиміляція СО2 та органічних субстратів. Переважна більшість цих фототрофних бактерій здатна до фіксації молекулярного азоту. Як запасні речовини накопичуються полі-Р-гідроксибутират, полісахариди та поліфосфати.
Пігменти фотосинтетичного апарату. Завдяки фотосинтетичним пігментам достатньо густі суспензії фототрофних бактерій мають зелене, зелено-синє, пурпурово-фіолетове, червоне, коричневе та рожеве забарвлення. Колір залежить від природи та кількісного співвідношення пігментів. Окремі пігменти можна визначити за спектрами поглинання інтактних клітин. Хлорофіли, наприклад, є відповідальними за максимуми поглинання в синій (< 450 нм), червоній та інфрачервоній (650-1100 нм) областях спектра. Поглинання в області 400-550 нм зумовлене каротиноїдами, а у ціанобактерій в області 550-650 нм — фікобіліпротеїнами.
Каротиноїди виконують дві функції: беруть участь у фотосинтезі як світлозбирні пігменти, тобто поглинають світлову енергію та передають її хлорофілу; захищають хлорофіл від фото-окиснення. Синьо-зелені мутантні форми пурпурових бактерій, позбавлені каротиноїдів, здатні рости тільки на слабкому світлі, а за високої інтенсивності світла гинуть.
Поширення фототрофних бактерій. Фототрофні пурпурові та зелені бактерії існують в анаеробних зонах багатьох водойм, у неглибоких ставках, у водах, які повільно течуть, в озерах і морських бухтах. Пурпурові сіркобактерії нерідко утворюють нальоти, забарвлені у різноманітні відтінки червоного кольору (від ніжнорожевого до темно-червоного), на поверхні мулу чи на якомусь органічному матеріалі, що розкладається. Іноді вони рояться над поверхнею мулу, утворюючи шар завтовшки близько 10 см ("цвітіння" води). Інтенсивне розмноження пурпурових сіркобактерій спостерігається і в мілководних ставках, поверхня яких вкрита щільним шаром ряски або листям водних лілій.
Цей своєрідний біологічний фільтр поглинає ті спектральні компоненти світла, які можуть використовуватись зеленими водоростями та ціанобактеріями, але пропускають світло, що поглинається бактеріохлорофілами та темно-червоними каротиноїдами. Тому під таким зеленим покривом ростуть анаеробні фототрофні бактерії.
Сезонний масовий розвиток пурпурових сіркобактерій спостерігається також в анаеробних зонах озер нижче межі температурного стрибка (термоклин, глибина 10-30 м). Бактерії знаходять тут необхідні їм речовини — сірководень, СО2 та органічні сполуки. Інфрачервоне сонячне випромінювання, яке поглинається бактеріохлорофілами, не проникає на таку глибину. У цих умовах максимум енергії припадає на область спектра 450—500 нм, тобто якраз ту область, в якій поглинають каротиноїди. Високий вміст каротиноїдів у клітинах пурпурових бактерій забезпечує можливість фотосинтетичного метаболізму цих бактерій на великих глибинах. Відповідно на таких глибинах і серед зелених сіркобактерій переважають багаті на каротиноїди коричневі форми.
ПРОЦЕСИ ФОТОСИНТЕЗУ
Фотосинтез — перетворення світлової енергії у біохімічно доступну енергію (АТФ) та відновлювальні еквіваленти [НАД{Ф)Н], а також зв'язаний з цим синтез клітинних компонентів.
Рівняння фотосинтезу у зелених рослин має вигляд
СО2 + 2Н2О—><СН2О + Н2О + 2О.
Рівняння фотосинтезу у фототрофних бактерій має вигляд
СО2 + 2H2S-—><CH2O> + Н2О + 2S.
Загальне рівняння фотосинтезу можна навести у вигляді
СО2 + 2Н2А——><СН2О> + Н2О + 2А.
Основою будь-якого фотосинтезу є один і той самий первинний процес, а різні типи фотосинтезу відрізняються один від одного тільки природою донора водню (вода, сірководень, органічні сполуки). Для того, щоб донором водню могла бути вода, необхідним є здійснення двох послідовних фотореакцій. При використанні донорів з більш негативним окисно-відновним потенціалом (сірководень) достатньо однієї фотореакції.
Оксигєнним фотосинтез
Первинні процеси фотосинтезу проходять у тилакоїдах — плоских замкнених мембранних бульбашках, що містяться в клітинах ціанобактерій і хлоропластах водоростей і зелених рослин.
Тилакоїдні мембрани і світлозбирні пігменти (пігменти антен). Тилакоїдна мембрана містить пігментні молекули (хлорофіл а, хлорофіл b і каротиноїди), переносники електронів і ферменти. Переважна більшість молекул хлорофілу (понад 99 %), а також додаткові пігменти (каротиноїди, фікобіліпротеїни) є відповідальними за поглинання світла і розподіл енергії; вони утворюють систему антен. Лише незначна частина хлорофілу а виконує роль фотохімічного реакційного центру, в якому і проходить фотохімічна окисно-відновна реакція.
Пігменти антен (світлозбирні пігменти) уловлюють світло і передають енергію хлорофілу реакційного центру:
Каротиноїд -> Каротиноїд *; Хлорофіл + Каротиноїд * -> Хлорофіл * + Каротиноїд.
Фотореакції. Фотореакції належать до первинних процесів фотосинтезу. Вони здійснюються в реакційних центрах. Реакційний центр складається з ряду компонентів, найважливішими з яких є первинний донор електронів (комплекс хлорофілу та білка) і первинний акцептор електронів. Ці два компоненти являють собою окисно-відновні системи. Система донора (Р/Р+) має позитивний потенціал, а система акцептора (Х/Х -) — негативний. Під дією енергії світла відбувається перенесення одного електрона
Відновлений
донор + Окиснений акцептор.....--—
>
—> Окиснений донор + Відновлений акцептор.
У результаті фотореакції донор втрачає один електрон — виникає "дірка" (електронний ефект). Такі дірки повинні заповнюватись електронами, які можуть надходити шляхом циклічного або нециклічного перенесення електронів. У разі нециклічного перенесення електрони надходять від екзогенного зовнішнього донора, а у разі циклічного — повертаються від відновленого акцептора (X ) до окисненого донора. Циклічне перенесення електронів приводить до зміни заряду мембрани, а нециклічне — й до відновлення НАДФ.
Дві фотореакції в двох фотосистемах. У оксигенному фотосинтезі працюють дві фотосистеми (ФС) — І і II (рисунок 6.21). Фотосистема І збуджується світлом з довжиною хвилі більше 730 нм, а фотосистема II — короткохвильовим світлом (менше 700 нм).
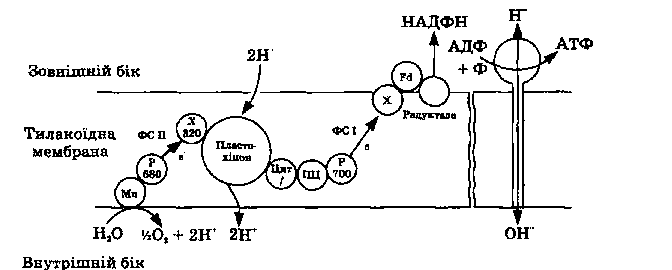
Рис. 6.21 Схема просторової орієнтації електрон-транспортної системи на тилакоїдиій мембрані: Мп — марганцевий комплекс; ПЦ — пластоціанін; цит / — цитохром f; Fd — фередоксин; X — залізосірковий білок
Фотохімічно активний центр фотосистеми і містить хлорофіл а (Р700), який є первинним донором електронів у першій фотореакції. Окисно-відновний потенціал Р700 становить близько +0,5 В. Світлова енергія, що поглинається світлозбирними пігментами першої фотосистеми, передається в реакційний центр і переводить у збуджений стан Р700, який окиснюється і віддає один електрон. Акцептором відданого електрона є X — залізосірковий білок з окисно-відновним потенціалом близько -0,5 В. Цей акцептор у свою чергу передає електрон фередоксину, а з відновленого фередоксину — на НАДФ та інші акцептори, в тому числі і на Р700 (нециклічне перенесення електронів). У разі циклічного перенесення електрон від X передається через пласто-хінон, цитохроми та пластоціанін (ПЦ) знову на Р700.
Реакційний центр фотосистеми II містить хлорофіл а11. (Р680), який є первинним донором електронів у другій фотореакції. Його окисно-відновний потенціал становить близько +0,9 В. Акцептором електрона є пластохінон Х320 з окисно-відновним потенціалом близько 0 В. Пластохінон при цьому відновлюється до семихінону. Донором електронів для цієї фотосистеми є вода: дірка, що утворилася в Р680 внаслідок втрати електрона, заповнюється електроном, який вивільнюється при утворенні О2 з води. Розклад води відбувається за участю марганцю.
Дві описані фотосистеми зв'язані між собою електрон-транспортним ланцюгом, важливою ланкою якого є пластохінон. Подібно до убіхінону в дихальному ланцюгу, пластохінон міститься в надлишку і є своєрідним "депо" електронів.
Як видно з рисунка, перенесення одного електрона через дві фотосистеми супроводжується надходженням двох протонів у внутрішній простір тилакоїдів. Дві фотосистеми разом з електрон-транспортним ланцюгом забезпечують спрямований потік електронів від води (із внутрішнього боку) до НАДФ (із зовнішнього боку). Отже, фотореакції приводять до відновлення НАДФ і утворення заряду на мембрані. Тобто світлові реакції виступають у ролі протонного насоса, який працює за рахунок енергії світла і створює позитивний заряд всередині тилакоїда. В результаті цього мембрана акумулює енергію у формі протонного потенціалу, і ця енергія використовується для синтезу АТФ.
Аноксигенний фотосинтез
В аноксигенному фотосинтезі бере участь одна фотореакція, вона підтримує циклічний транспорт електронів. Для поповнення циклу електронами потрібні зовнішні донори електронів. Ними є сірководень, сірка, тіосульфат, органічні сполуки (малат, сукцинат та ін.), молекулярний водень. Фотореакція, хоча й аналогічна першій фотореакції у зелених рослин, приводить тільки до створення протонного потенціалу і синтезу АТФ, але не до відновлення НАД (у цьому разі відсутнє нециклічне перенесення електронів, у результаті якого відновлюється НАД). НАДН у клітинах анаеробних фототрофів утворюється за рахунок зворотного транспорту електронів, який відбувається з витратами АТФ (за аналогією з аеробними хемолітоавтотрофами). Такий процес фотосинтезу є характерним для пурпурових фототрофних бактерій.
При фотореакції у зелених бактерій первинний акцептор електронів має окисно-відновний потенціал близько -0,5 В (у пурпурових бактерій — всього -0,1 В!). За такого високого негативного потенціалу є можливим перенесення електронів від первинного акцептора для відновлення фередоксину та відновлення НАД. Отже, відновлювальні еквіваленти у зелених фотобактерій утворюються не за рахунок зворотного транспорту електронів, який потребує витрат АТФ (як у пурпурових фотобактерій), а в результаті фотореакції. З еволюційного погляду фотосинтез зелених бактерій міг би бути ланкою, яка зв'язує фотосинтез пурпурових бактерій і фотосинтез ціанобактерій і зелених рослин.
ВИКОРИСТАННЯ СВІТЛОВОЇ ЕНЕРГІЇ ГАЛОБАКТЕРІЯМИ
Галобактерії, які належать до архебактерій, існують у високо-концентрованих або насичених розчинах солей. Оптимальний ріст галобактерій відбувається у 3,0-3,5 М розчині хлористого натрію. Можливість існування цих бактерій у таких екстремальних умовах зумовлена тим, що концентрація солі всередині клітин є такою ж високою, як і в навколишньому середовищі.
Паличкоподібні рухливі клітини Halobacterium halobium забарвлені у червоний, оранжевий і жовтий кольори завдяки наявності каротиноїдів. У клітинах галобактерій міститься також і бактеріородопсин — пігмент, який утворює в клітинах так звану пурпурову мембрану — темно-червоні плями діаметром 0,5 мкм у плазматичній мембрані. Ці пурпурові мембрани займають близько половини поверхні клітини. Завдяки бактеріородопсину на світлі створюється протонний потенціал між зовнішнім і внутрішнім боками мембрани. Отже, пурпурова мембрана виконує роль протонного насоса, який приводиться в дію світлом, що й спричиняє утворення електрохімічного мембранного потенціалу. Вирівнювання зарядів (розрядка потенціалу) може супроводжуватися синтезом АТФ: пурпурова мембрана уможливлює функціонування особливого типу фосфорилювання. Крім енергії, одержаної за допомогою світла, галобактерії можуть отримувати енергію за рахунок аеробного окиснення субстрату.
