
- •Введение
- •ГЛАВА 1. Генетическая токсикология, предмет и задачи
- •ГЛАВА 2. Изменчивость
- •2.1. Типы изменчивости
- •Рис. 2.1.1. Типы изменчивости
- •2.2. Основные положения теории мутаций
- •2.3. Новые положения теории мутаций
- •2.4. Классификация мутаций
- •2.5. Генные мутации
- •2.5.1. Типы генных мутаций
- •2.6. Хромосомные мутации
- •Рис. 2.6.1. Классификация хромосомных аберраций
- •Рис. 2.6.6. Выявление делеций во время мейоза и на политенных хромосомах
- •Рис. 2.6.7. Эффект положения гена: изменение числа фасеток в зависимости от положения генов в хромосоме
- •Рис. 2.6.8. Выявление дупликаций во время мейоза
- •Рис. 2.6.9. Образование инверсионной петли в мейозе
- •Рис. 2.6.13. Участок метафазной пластики. Транслокация: транслокоционный крест (слева – фотография, справа – реконструкция)
- •2.7. Геномные мутации
- •Рис. 2.7.1. Классификация геномных мутаций
- •2.8. Уровни защиты организмов от мутагенов
- •ГЛАВА 3. Методы оценки мутагенов
- •3.1. Проблемы оценки мутагенов
- •Рис. 3.1.1. Принципиальная схема поэтапного тестирования (B.A. Bridges, 1974): “+” – положительный ответ тестирования, “–” – отрицательный ответ тестирования
- •3.2. Бактериальные тест-системы для выявления мутагенов
- •3.4. Цитогенетические методы
- •3.4.1. Метафазный анализ
- •3.4.2. Ана-телофазный анализ
- •3.4.3. Микроядерный тест
- •Рис. 3.4.1. Образование микроядра из ацентрического фрагмента
- •3.4.4. Сестринские хроматидные обмены
- •Рис.3.4.2. Метафазная пластинка (сестринские хроматидные обмены обозначены стрелками)
- •3.4.5. Политенные хромосомы
- •ГЛАВА 5. Методы выявления и оценки генотоксикантов
- •5.1. Отбор и подготовка проб для проведения токсикогенетического анализа
- •5.2. Chlorella vulgaris как тест-объект для оценки генотоксичности факторов окружающей среды
- •Рис. 5.2.1. Жизненный цикл хлореллы
- •Рис. 5.2.2. Метод последовательного разведения культуры клеток хлореллы
- •Таблица полученных в ходе работы результатов
- •Сравнение данных по выживаемости и частоте мутаций у хлореллы
- •Рис. 5.2.5. Соотношение типов мутаций у Chlorella vulgaris
- •Таблица полученных в ходе работы результатов
- •5.3.1. Клеточный (митотический) цикл
- •Рис. 5.3.1 Клеточный (митотический цикл)
- •Рис. 5.3.2. Митотическое деление растительной клетки: 1 – ядро, 2 – хромосомы, 3 – цитоплазма, 4 – кариолемма, 5 – кариоплазма, 6 – глыбки хромтина, 7 – веретено деления, 8 – фрагмопласт, 9 – ядра дочерних клеток
- •Рис. 5.3.3. Морфология хромосом в течение клеточного цикла
- •5.3.2. Ход выполнения лабораторной работы
- •Определение митотического индекса в меристеме корешка Allium cepa*
- •5.3.3. Определение митотоксической активности тканей
- •Сводная таблица учета митотического и фазных индексов в меристеме проростков корешков Allium cepa*
- •5.3.4. Статистическая обработка результатов
- •Рис. 5.3.5. Соотношение фазных индексов
- •Рис. 5.4.1. Типы хромосомных аберраций (схема)
- •5.4.2. Определение мутагенного эффекта химического соединения
- •Рис. 5.4.2. Картины хромосомных аберраций на стадии ана-телофазы
- •Рис. 5.4.3. Частота хромосомных аберраций в меристеме проростков корешков Allium cepa
- •Рис. 5.4.4. Соотношение типов хромосомных аберраций
- •5.5.1. Жизненный цикл дрозофилы
- •5.5.2. Методы культивирования дрозофилы
- •Частота летальных культур у Drosophila melanogaster
- •Рис. 5.5.2. Половой диморфизм у Drosophila melanogaster
- •Рис. 5.5.3. Мутации у Drosophila melanogaster
- •Приложение
- •Генетический код
- •Словарь терминов
- •Список использованной литературы
- •Прохорова Инна Мечиславовна

Генетическая токсикология
ГЛАВА 3. Методы оценки мутагенов
ГЛАВА 3. Методы оценки мутагенов
3.1. Проблемы оценки мутагенов
а первом этапе главной задачей генетической токси- Нкологии была разработка методов оценки мутагенного эффекта различных факторов и выявление среди
них наиболее чувствительных и экономичных тестов.
Можно назвать основные требования, применяемые к современным токсикогенетическим методам:
-высокая чувствительность (чтобы не пропустить потенциальный мутаген, не дать ложноотрицательного ответа);
-специфичность (чтобы регистрировать только истинные мутагены, не давать ложноположительного ответа);
-способность выявлять все типы мутаций;
-возможность выявлять как прямые мутагены, так и косвенные мутагены (промутагены), приобретающие мутагенную активность в процессе метаболизма в организме;
-возможность выявлять как универсальные мутагены, индуцирующие мутации у всех организмов, так и мутагены, активные
вограниченном наборе биологических систем;
-экономичность, краткосрочность, простота в выполнении;
-воспроизводимость результатов (возможность получения аналогичных результатов на той же тест-системе);
-возможность экстраполяции данных, полученных при исследованиях in vitro на условиях in vivo (Дмитриева, Парфёнов,
1991);
-возможность экстраполяции полученных данных на челове-
ка.
-регистрация как нарушений структуры ДНК, так и генетических процессов (генетическая репарация, кроссинговер, протекание митоза, нарушение центромеры, митотического аппарата,
идр.
40

ГЛАВА 3. Методы оценки мутагенов
К настоящему времени разработано более 200 методов оценки генотоксикантов, в которых используются различные тестобъекты, от вирусов до высших животных и клеток человека, и регистрируется самые различные генетические повреждения. Однако существующее многообразие методов свидетельствует о том, что ни один из них не является универсальным, удовлетворяющим всех исследователей. Причины этого следующие:
1.Тесты на мутагенность являются видоспецифичными, так как есть мутагены, повреждающие геном только у определенных видов. Таким образом, мутаген, опасный, например, для человека, может быть не выявлен на используемом исследователем тест-объекте. Поэтому необходимо использовать несколько тестобъектов.
2.Методы являются тест-специфичными, то есть выявляют немного видов наследственных нарушений, чаще один тип мутаций. Поэтому, если тест, регистрирующий хромосомные мутации, дал отрицательный ответ, это не означает, что фактор не вызывает генных мутаций. Следовательно, чтобы не получить ложноотрицательных ответов, необходимо использовать несколько тестов.
3.Исследование одним методом и на одном тест-объекте может дать различный ответ из-за тканеспецифичного действия фактора. В тесте рецессивных летальных мутаций у Dr. melanogaster.
Так, у дрозофилы ответ зависит от того, в какие органы вводилось химическое соединение. Тканеспецифичность отмечается и при использовании микроядерного теста (Л.Н. Сычева, 2004).
4. Косвенные мутагены (промутагены) сами не обладают мутагенной активностью, но их метаболиты генотоксичны. Таким образом, даже проверка фактора несколькими методами на нескольких тест-объектах ещё не гарантирует, что его генетическая безопасность окончательно установлена.
По этим причинам для уменьшения количества возможных ложноотрицательных и ложноположительных ответов необходимо использовать широкий набор методов с применением широкого круга объектов. Это сильно усложняет и удорожает исследование.
Для уменьшения возникших затрат Б. Бриджесом и Фламмом (Bridges, 1976; Flamm, 1974) была предложена этапность тестирования, когда на первом этапе факторы отбираются по степени индуцируемого генотоксического эффекта. Дальнейшее тестиро-
41
Генетическая токсикология
вание требует больших затрат и проводится с учетом результатов первого этапа.
Традиционно процедура тестирования делится на три этапа: Первый этап. Первичный скрининг. Задача его – выявить, может ли в принципе данный фактор взаимодействовать с ДНК. Требования к методам этого этапа: высокая чувствительность, краткосрочность и экономичность. На данном этапе в качестве тест-объектов используются микроорганизмы, особенно часто –
бактерия Salmonella typhimurium.
Второй этап. Определяется, может ли данный фактор повреждать ДНК в эукариотических клетках. В качестве тест-объек- тов используются культуры клеток млекопитающих и человека.
Третий этап. Выясняется, может ли фактор вызывать генетические нарушения в целостном организме. Используются тесты, учитывающие эффект в соматических и половых клетках in vivo (Тарасов, 1994).
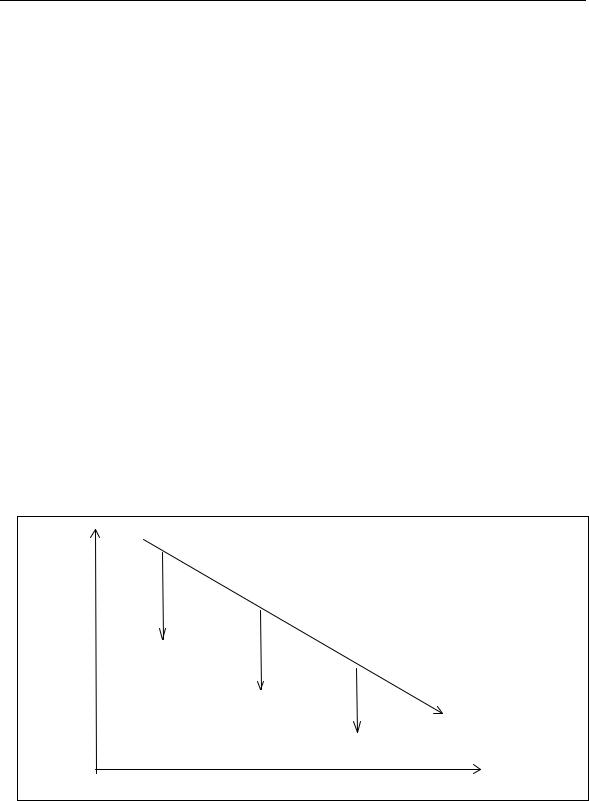
На рисунке 3.1.1 представлена схема поэтапного тестирования факторов на мутагенность. С увеличением стоимости тестирования происходит значительное снижение количества факторов, генотоксичность которых предстоит оценить.
число |
- + |
веществ |
- +
- +
принятие
решения
прекращение тестирования
увеличение стоимости
Рис. 3.1.1. Принципиальная схема поэтапного тестирования (B.A. Bridges, 1974): “+” – положительный ответ тестирования, “–” – отрицательный ответ тестирования
42
