
метода п.ф №1
.pdf21
существенно влияет на метаболические процессы в клетке (см. раздел 4.2.4.); б) к нарушению микросомального окисления и способности клеток к детоксикации вредных и
чужеродных, в том числе и лекарственных веществ; в) к нарушению деятельности рибосом, фиксированных на ЭПР и снижению синтеза белка.
Повреждение лизосом приводит к выходу в цитоплазму гидролитических ферментов (протеаз, липаз, нуклеаз и т. д.), наиболее активных в кислой среде и способных расщеплять практически любую структуру клетки. При их активации в клетке начинают преобладать катаболические процессы. В результате дело может закончиться аутолизом (самоперевариванием) клетки.
Повреждение ядра приводит к изменению деятельности внутриядерных ферментов, принимающих участие в синтезе нуклеиновых кислот, нарушению структуры ДНК и РНК, синтеза ферментов, участвующих в процессах метаболизма в клетке. Наиболее уязвимым местом ядра является РНК-полимераза. Значительные нарушения в ядре могут происходить при митотическом делении и заключаться в разрыве хромосом, отрыве части хромосом (делеции), переносе этого участка хромосомы на другую (транслокация) или в неправильном расхождении хромосом с неравномерным распределением их между двумя дочерними клетками. Как правило, эти нарушения приводят к снижению жизнеспособности или гибели клеток.
4.2.3. Механизмы, определяющие клеточную реактивность, и ее изменения.
При оценке действия патогенного фактора на клетку необходимо учитывать как силу, продолжительность и характер его влияния, так и функциональное состояние клетки, проявляющееся ее пониженной или повышенной чувствительностью. Эта чувствительность на протяжении индивидуальной жизни претерпевает значительные изменения, что связано с проблемой возрастной резистентности, но также и с сезонными, суточными и другими ритмами, которым подвластны не только организм, но и клетки.
На поверхности клетки существует высокореактивная среда - гликокаликс. Состояние этой среды, содержащей мембранные рецепторы, определяет способность клетки отвечать на раздражение. Следует подчеркнуть, что поверхностные белки мембран отражают генетическую информацию, заложенную в ядре, и что как виды белковых молекул, так и их взаимное расположение на мембране специфичны для данного вида индивидуума, что и определяет как видовую, так и индивидуальную реактивность.
Первым информатором о патогенном факторе являются мембранные рецепторы. Именно через них запускается механизм молекулярного ответа. В передаче информации участвуют три компонента: расположенный на внешней поверхности мембраны рецептор; трансдюсер фосфолипидной природы и каталитический компонент, находящийся на внутренней поверхности мембраны, например, аденилатциклаза.
Нарушение или изменение ответа на молекулярном уровне может быть связано:
1.С отсутствием или уменьшением количества клеточных рецепторов в результате генетического дефекта.
2.С повреждением рецепторов. Оно может быть следствием денатурации белков под действием термических или химических факторов; повреждения гликопротеидов рецептора, например, под
22
действием опухолевых вирусов, продуктами перекисного окисления липидов, например, при стрессе. 3.С конфирмационными изменениями структуры рецепторов. Это может быть следствием
гормональных влияний или изменения электростатических сил между молекулами белков при сдвигах реакции внеклеточной среды в кислую или щелочную сторону. Например, при связывании
молекулы гормонаглюкагона со своим рецептором на поверхности печеночной клетки утрачивается структурное сродство к гормону рецептора, реагирующего на инсулин, расположенного на поверхности этой же клетки; в условиях ацидоза снижается чувствительность гладкомышечных клеток артериол к вазопрессорному действию катехоламинов. Эти изменения реактивности обратимы.
4.С повреждением внутримембранных фосфолипидов-трансдюсеров (передатчиков). Это происходит при активации фосфолипаз или накоплении липидных перекисей. Такие процессы могут наблюдаться, например, в опухолевых клетках. В результате нарушается передача на субмембранный каталитический компонент.
5.С изменением концентрации в клетке вторичных "посредников": цАМФ, цГМФ, ионов кальция, инозитолтрифосфата, диацилглицерола, участвующих в реализации физиологического ответа клетки.
6.С включением приспособительных механизмов, обеспечивающих адаптацию клетки к действию патогенных факторов. Например, при интенсивном ультрафиолетовом облучении в клетках кожи откладывается меланин, защищающий их от повреждения. При хроническом действии ядов уменьшается проницаемость клеточных мембран для них и активируются ферменты, их разрушающие. Благодаря этим механизмам изменяется реактивность клетки - она и организм в целом становятся более резистентными.
4.2.4. Патогенез повреждения клетки
При действии самых разнообразных патогенных факторов в первую очередь происходит повреждение плазматической мембраны. Функциональные мембраны клетки представляют собой барьеры для заряженных частиц (ионов) и молекул с молекулярной массой выше 100-150. Эти вещества активно или пассивно накапливаются в пространствах, ограниченных мембранами и обусловливают возникновение концентрационных (химических) или электрохимических (ионных) градиентов на границах клетка - среда. Транспорт веществ происходит с участием систем активного и пассивного транспорта. Системы пассивного переноса облегчают перемещение веществ в направления градиента их концентраций через мембрану клеток. Деятельность этих систем не требует затрат энергии, однако и не является в полном смысле слова пассивной. Гидрофобный липидный слой представляет определенный барьер для прохождения растворимых в воде веществ. Предполагается наличие в мембране специальных мембранных каналов, деятельность которых определяется величиной и видом заряда их поверхности и связана с механизмом активного транспорта. Система активного транспорта осуществляет перемещение веществ против градиента их концентрации с расходом энергии макроэргических фосфатов. Так работает, например, система калий - натриевого насоса. Эта система локализована в клеточной мембране и за счет энергии, высвобождаемой при гидролизе АТФ выводит натрий из клеток и накапливает в ней калий. Разница в концентрации натрия и калия поддерживается, пока существует живая клетка. Прекращение работы этой системы ведет к
23
гибели клетки.
Причины нарушения активного транспорта могут быть связаны; 1.С недостатком синтеза АТФ в клетке. Например, при повреждении митохондрий, дефиците
кислорода, глюкозы и т.д.
2.С блокадой мембранных АТФ-аз. Например, сердечные гликозиды, блокируя калий-натриевую АТФ-азу, могут провоцировать возникновение аритмий.
3.С повреждением мембран липидными перекисями, свободными радикалами. Например, клеток миокарда при стрессе.
Нарушение работы активного транспорта приводит к изменению деятельности мембранных каналов, т. е. к нарушению механизма пассивного транспорта. В результате изменяется поступление веществ в клетку и выведение метаболитов, накопление натрия и кальция в ней. Избыток кальция в цитоплазме поглощается митохондриями и ЭПР. При повреждении клетки ее способность удалять кальций через плазматическую мембрану снижается. Буферная емкость митохондрий ограничена и слишком большой поток кальция может ее превысить. Митохондрии набухают, в матриксе их появляются преципитаты, в состав которых входит кальций, окислительное фосфорилирования угнетается. Повышение содержания кальция в цитоплазме приводит к увеличению содержания белкакальмодулина. Он активирует гликолиз, снижает ресинтез гликогена, увеличивает расход АТФ и потребность клетки в кислороде. Активация гликолиза приводит к снижению рН в клетке и активации лизосомальных ферментов. В результате катаболические процессы в клетке начинают преобладать над анаболическими и способствуют дальнейшему прогрессированию ацидоза и повышению осмотического давления. Это вызывает перемещение воды из внеклеточного пространства и развитие отека. Развитие отека клетки усугубляет дистрофические процессы в ней. На определенном этапе ацидоз начинает угнетать гликолиз, что приводит к значительному снижению содержания АТФ в клетке и еще более выраженной активации лизосомальных ферментов. Дефицит АТФ и активация лизосомальных ферментов (липаз и фосфолипаз) усугубляет повреждение мембран митохондрий и ЭПР, что приводит к нарушению процессов аккумуляции кальция в них и выходу его в цитоплазму. В этом случае кальций, который в нормальных условиях является жизненно важным регулятором клеточного метаболизма, становится для клетки настоящим "убийцей". Реакции, обычно регулируемые кальцием, протекают непрерывно, неконтролируемо. Активация липаз и фосфолипаз, накопление продуктов липидного обмена (жирных кислот, перекисей) усугубляет повреждение клеточной мембраны, мембран лизосом и митохондрий, блокирует мембранные АТФ-азы, рецепторы и каналы ионной проницаемости.
Так формируется ряд порочных кругов, приводящих к некробиозу клетки. Продукты перекисного окисления липидов вызывают повреждение спирали ДНК. Накопление ошибок генетического кода становится одной из причин быстрого старения клетки. Процесс повреждения может быть остановлен включением саногенетических механизмов. Следует диалектически оценивать значение изменений, возникающих при повреждении. Некоторые звенья этого процесса имеют как патогенное, так и саногенное значение.
4.2.5. Саногенетические механизмы в процессе повреждения клетки. Исходы повреждения
24
1.Переключение энергетического обмена на менее выгодный анаэробный гликолиз возникает при действий на клетку самых разнообразных повреждающих факторов. В результате резко снижается содержание макроэргических соединений (креатинфосфата, АТФ).
2.Использование жиров и белков в процессе глюконеогенеза приводит к формированию дистрофии. Ацидоз и активация лизосомальных ферментов может привести к лизису клетки. Однако переключение на анаэробный гликолиз имеет и приспособительное значение, так как делает клетку более автономной, независимой от поступления кислорода. Позволяет пережить неблагоприятный период, связанный, например, с временными нарушениями кровообращения. Переключение на анаэробный гликолиз защищает мембрану ЭПР от разрушения. Так, в эксперименте было показано, что ингибирование гликолиза при сохранении окислительного фосфорилирования на фоне гипоксии усиливает повреждение мембранных структур миокарда.
3.Снижение ресинтеза АТФ увеличивает потребность клетки в кислороде и вместе с тем продукты распада АТФ (аденозин, аденозин-монофосфат) обладают мощным вазодилятирующим действием, способствуют раскрытию анастомозов. Когда митохондрии еще не перенасыщены кальцием, они поглощают его избыток, что позволяет клетке выиграть время. После того как кальциевая буря утихнет, они начинают выделять в цитоплазму кальций с небольшой скоростью, не нарушая метаболизма клетки. Образующийся при распаде АТФ неорганический фосфор играет роль "ловушки" для кальция, связывая его.
4.Увеличение содержания кальмодулина способствует удалению кальция в везикулы ЭПР. Умеренное повышение продуктов перекисного окисления липидов разобщает мембранный компонент и защищает клетку от избыточного действия раздражающего агента.
5.Накопление продуктов перекисного окисления жирных кислот приводит к образованию простагландинов, обладающих мощным мембрано-стабилизирующим действием (простагландины группы Е, простациклин и др.).
6.Антиоксиданты (токоферол) и антиоксидантные ферментные системы (супероксиддисмутаза, глутатионпероксидаза и др.) сглаживают последствия нарушений липидного обмена.
7.Экспрессия определенных генов и как следствие - накопление в клетках специальных так называемых "стресс-белков", которые предотвращают денатурацию белков и т.о. защищают клеточные структуры от повреждения.
8.Система ферментов - репараз восстанавливает нарушения структуры ДНК (если повреждена одна спираль).
Таким образом, исход повреждения зависит от равновесия между процессами повреждения и приспособления. При чрезмерном или длительном, хроническом действии патогенных факторов повреждение из обратимого переходит в необратимое. Это заканчивается гибелью клетки, ее некрозом.
Включение адаптивных механизмов может привести к полному сохранению функции и жизнедеятельности клетки.
Однако, чаще всего, особенно при хроническом действии раздражителей, в клетке возникают и накапливаются определенные структурные, функциональные и биохимические нарушения,
25
приводящие в конечном итоге к более быстрому изнашиванию и старению клеток. При длительном действии экстремальных факторов внешней среды, большая часть энергии, образующейся в клетках, расходуется на адаптацию и приспособление к неблагоприятным условиям внешней среды, и меньше ее остается на осуществление процессов самообновления, в то время как в норме большая часть энергии тратится на восстановительные процессы. В результате длительное действие неблагоприятных факторов внешней среды приводит к более быстрому изнашиванию и старению клетки, а значит и ограничению активной жизни индивида в целом.
5. КОНСТИТУЦИЯ ЧЕЛОВЕКА.
МЕХАНИЗМЫ ФОРМИРОВАНИЯ НАСЛЕДСТВЕННОЙ ПАТОЛОГИИ
5.1. Контрольные вопросы 1. Конституция человека, роль наследственности и внешней среды в ее формировании. Значение
для организма и его патологии. 2. Некоторые механизмы формирования наследственной патологии. 3. Проявления конституциональной патологии. 4. Особенности людей нормальных конституциональных типов и заболеваемость. 5. Принципы профилактики и терапии конституциональной патологии.
5.2. Рекомендации к ответам 5.2.1. Конституция человека, роль наследственности и внешней среды в ее формировании
Конституция человека - это совокупность стойких морфологических, биохимических и функциональных, в том числе психических особенностей человека, формирующихся на генетической основе в рамках нормы реакции.
Конституция - основа реактивности организма.
Норма реакции - это диапазон изменчивости наследственного признака в различных условиях внешней среды. Наиболее изменчивые признаки, которые наследуются полигенно, то есть формирование которых зависит не от одной, а от нескольких пар генов. Доминантные аллели каждой пары как бы суммируют свое влияние (аддитивное действие генов). В совокупности получается большая или меньшая выраженность признака. Полигенным наследованием определяются количественные признаки, такие как рост, масса тела, артериальное давление, содержание в крови тех или иных веществ, уровень интеллекта и другие психологические особенности.
В формировании конституциональной патологии большое значение имеет аддитивнополигенное наследование с пороговым эффектом. В достижении порога, то есть того критического уровня, за которым возникает патология, кроме наследственных могут иметь значение и различные средовые влияния. Последние нередко социально обусловлены. Например, питание людей, уровень физических и эмоциональных нагрузок, воздействие экологических нарушений, занятость женщин вне семьи, в результате чего уменьшено общение ребенка с матерью. До недавнего времени последний фактор не принимали во внимание, хотя известно, что недостаток ласки, то есть недостаток у ребенка положительных эмоций, вызываемых лаской, нарушает формирование эмоциональной сферы. Это отражается на характере, личностных особенностях человека. Такую же роль играют равнодушие и жестокость по отношению к ребенку в семье или в детском учреждении. Формированию аномалий характера (акцентуаций и психопатий) способствует алкоголизация в детском и подростковом возрасте, а тем более в период утробного развития.
26
Фактором, очень неблагоприятным для формирования конституции, является также позднее прикладывание новорожденного к груди матери и недостаточно продолжительный период грудного вскармливания. С молозивом, а затем с молоком ребенок должен получать гормонально активные полипептиды. Без них страдает формирование иммунологической и эндокринной систем организма. Иммунодефицит проявляется в дальнейшем не только пониженной устойчивостью к инфекциям, но и повышением частоты опухолевых и аутоаллергических заболеваний. Высказывается суждение о том, что иммунологические нарушения у женщин являются одной из причин многократных выкидышей и преждевременных родов. Отклонения же формирования эндокринной системы приводят к нарушениям обмена, проявляющимся ожирением - часто уже в детском возрасте, повышением опасности сахарного диабета, более ранним формированием атеросклероза.
5.2.2. Значение конституции для организма и его патологии
Конституция определяет реактивность организма (см. главу 6). От нее зависят индивидуальные возможности биологической и социальной адаптации. Конституция имеет огромное значение в этиологии, так как генетические дефекты могут выступать как в роли этиологического фактора, так и 8 роли условия (см. главу 2). Кроме того, в конституции человека могут быть аномалии, которые сами по себе нарушают жизнедеятельность, причиняют страдания, то есть определяют патологическое состояние организма.
5.2.3.Некоторые механизмы формирования наследственной патологии
Отправным пунктом формирования наследственной патологии является кодируемый геном белок или полипептид с аномальной структурой. С определенной долей условности белки можно подразделить на ферментные и неферментные.
5.2.3.1. Формирование патологии на почве нарушений ферментативных процессов
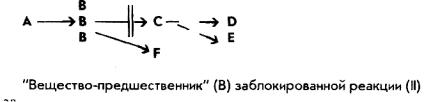
Генетически обусловленным может быть отсутствие фермента, его дефект или нарушение регуляции его функции. В результате определенное звено обмена может быть усилено или, чаще, наоборот, будет ослаблено. Перерыв в цепи биохимических превращений называют "блокадой метаболизма". Она может быть полной или частичной.
"Вещества-продукта" (С) становится недостаточно, следовательно, и всех тех веществ, для синтеза которых оно необходимо (D, Е). Организм может страдать как из-за избытка предшественника, так и от недостатка продукта заблокированной реакции. И то, и другое может вести к формированию самых разнообразных дистрофических процессов.
Ферменты обеспечивают синтез и разрушение всех гуморальных регуляторов (гормонов, простагландинов, кининов, компонентов ренин-ангиотензинной системы, регуляторов гемопоэза и лимфопоэза и многих других). Поэтому нарушение ферментативной активности может лежать в основе нарушения регуляции любой системы организма.
27
Некоторые метаболиты обладают канцерогенным влиянием, например, образующиеся в процессе обмена триптофана и тирозина. В результате недостаточной активности обезвреживающих их ферментов возрастает концентрация канцерогенов в крови и моче. У таких людей имеется предрасположенность к опухолевым заболеваниям, особенно мочевыводящей системы и системы кроветворения.
Недостаток миелопероксидазы и др. ферментов в лейкоцитах снижает их защитную функцию. Нарушения обмена в эритроцитах в результате дефекта различных ферментов может быть
причиной гемолиза.
Дефект ферментов свертывающей системы крови лежит в основе ряда форм повышенной кровоточивости (гемофилии).
Дефект фермента может быть причиной и других патологических проявлений, примеры которых изложены в разделе 5.2.4.
5.2.3.2. Формирование патологии на почве дефекта неферментных белков
Специальные белки осуществляют связывание веществ в крови, транспорт их через мембраны клеток, входят в состав мембран клеток и их рецепторов, обеспечивают структуру соединительной ткани и т. п. Дефект такого белка может быть следствием как нарушения матрицы ДНК, то есть синтеза аномального полипептида, так и следствием дефекта фермента, участвующего в синтезе специального белка из полипептидов.
Дефект связывающего белка крови изменяет активность связываемого им объекта (гормона, биологически активного вещества и т. п.). Это клинически проявляется аналогично избытку или недостатку соответствующего фактора и лежит в основе многих случаев эндокринной патологии, а также заболеваний, имеющих в основе расстройство других гуморальных механизмов регуляции. Этот механизм может давать и другие разнообразные патологические проявления. Например, нарушение связывания в крови катионов кальция приводит к расстройству регуляции сосудистого тонуса; железа - к уменьшению синтеза гемоглобина или отложению железа в тканях с развитием там дистрофических процессов (первичный гемохроматоз). В результате недостаточного связывания в крови катиона меди он откладывается в ядрах мозга, в печени, в роговице, вызывая дистрофические изменения (болезнь Вильсона-Коновалова). Недостаточное связывание гистамина специальным белком крови проявляется необычно ярким течением воспалительных и аллергических процессов (одна из причин так называемого экссудативного диатеза).
Дефект транспортных белков, осуществляющих перенос веществ через мембраны клеток, может иметь следствием снижение или, наоборот, усиление всасывания вещества из кишечника или первичной мочи. В результате организм теряет что-то необходимое (аминокислоту, витамин, микроэлемент и т. п.) или, наоборот, создается его избыток, и это определяет специфичность формирующегося повреждения. Например, из-за дефекта транспортного белка апоферритина снижается всасывание железа в кишечнике, создается его дефицит и возникает одна из многочисленных наследственных форм анемии. В случае нарушения транспорта через мембраны других клеток вещество остается неиспользованным в крови, а обмен нарушается так же, как при дефиците этого вещества.
28
Генетические особенности структуры клеточных рецепторов определяют чувствительность организма к воздействию вирусов, микробных токсинов, химических веществ, в том числе фармакологических, а также к разнообразным регулирующим влияниям на клетку, в частности, эндокринным. Последнее, в свою очередь, может проявиться изменениями формирования органов, роста скелета, обменными расстройствами (ожирением, атеросклерозом, диабетом и др.). Например, в случае дефекта рецепторов клеток к соматотропному и фолликулостимулирующему гормонам при моносомии по Х-хромосоме, несмотря на высокое их содержание в крови формируется синдром Шерешевского-Тернера: аплазия яичников, низкий рост, характерная форма шеи, часто снижение интеллекта.
Следствием нарушения структуры специфических белков могут быть и другие очень разнообразные патологические проявления. Например, недостаточное образование иммуноглобулинов (гипо- и агаммаглобулинемия) является одной из причин конституциональной несостоятельности гуморального иммунитета.
Дефекты или недостаток неферментных белков свертывающей системы крови (афибриногенемия) может быть основой конституциональной кровоточивости. В случае различных отклонений в синтезе коллагена, из-за изменения свойств соединительной ткани возникают нарушения опорно-двигательного аппарата: искривления позвоночника, деформации грудной клетки, тугоподвижность суставов или, наоборот, склонность к возникновению вывихов. Примером может служить синдром Марфана: у человека высокий рост за счет удлинения конечностей, длинные гибкие "паучьи" пальцы, деформации грудной клетки, нарушение зрения из-за вывиха хрусталика, расстройства гемодинамики из-за несмыкания створок клапанов сердца.
5.2.4. Проявления конституциональной патологии
Первую группу составляют аномалии строения органов (уродства), формирующиеся на основе генетического дефекта.
Конституциональные дефекты развития чрезвычайно разнообразны и часто бывают множественными. Это различные отклонения строения скелета, нервной системы, почек и мочевыводящих путей, сердца и т. п. Они могут быть следствием генных дефектов и хромосомных аномалий.
В эту же группу могут быть отнесены и аномалии личности, возникающие на генетической основе - акцентуации характера и психопатии, или "личностные уродства", как их образно называли раньше. Они очень разнообразны. Широко распространена, например, так называемая эмоциональная тупость. Это люди с обедненной эмоциональной сферой, а именно - у них снижена способность испытывать радость, сострадание, стыд, жалость, чувство дружбы. Они крайне самоуверенны, равнодушны как к порицанию, так и к похвале, эгоистичны, жестоки и даже агрессивны не только к посторонним, но и к своим близким. Для таких людей характерно потребительское отношение к людям, природе, обществу. Вместе с тем у них очень низки духовные потребности. Не желая трудиться,- они часто стремятся жить за чужой счет, что приводит к правонарушениям, проституции, алкоголизму, наркомании. Этим людям недоступны человеческие отношения, которые называются нормами морали. Поэтому они легко разрушают семьи, взрослые дети не заботятся о престарелых
29
родителях, мать может бросить ребенка. Равнодушие и даже жестокость таких людей к своим детям способствуют формированию аномалий характера и в следующем поколении.
Порок развития может иметь место уже при рождении ребенка, но может формироваться позже, например, деформации позвоночника и грудной клетки, психопатии. После того как уродство сформировалось, оно не нарастает, а даже в некоторых случаях может отчасти компенсироваться. Так, проявления патологических личностных особенностей (психопатий), максимальные в подростковом возрасте, в зрелом отчасти сглаживаются.
Однако на почве некоторых морфологических отклонений может возникнуть типовой патологический процесс, что ляжет в основу болезни. Например, в случае стеноза мочеточников, из-за повышения давления в лоханках может возникнуть атрофия почечной ткани - гидронефроз. На почве аневризм сосудов мозга могут возникать расстройства функции нервной системы и кровоизлияния. Аномалии сердца или сосудов могут приводить к нарушениям гемодинамики и возникновению новых болезненных проявлений. В таких случаях своевременная хирургическая коррекция морфологического дефекта может предотвратить формирование болезни.
Вторую группу проявлений конституциональной патологии составляют строго наследственные болезни, то есть такие, в основе которых лежит повреждение, возникновение и специфичность которого полностью определяется генетическим дефектом. Например, гемолиз при гомозиготности по S-гeмоглобину. Формируется патология вне зависимости от влияний внешней среды. Начало строго наследственных заболеваний приурочено к определенному возрасту. Повреждение, как правило, неуклонно прогрессирует. Это редкие заболевания, но их много и суммарно в заболеваемости современных людей они занимают значительное место.
Третью группу проявлений конституциональной патологии составляют заболевания, при которых повреждение возникает только в случае, если организм, имеющий определенный дефект, взаимодействует со строго определенным средовым фактором, безвредным для других людей.
Так, в случае недостаточной активности фермента, расщепляющего какой-либо дисахарид в тонком кишечнике, последний частично всасывается нерасщепленным, или подвергается в толстом кишечнике бактериальной ферментации. Поэтому у человека, например с алактазией, употребление свежего молока (лактозы) вызывает метеоризм, диарею, рвоту. Последние могут приводить к обезвоживанию, исхуданию. В результате выведения дисахарида с мочой могут поражаться почки человека. Возникает отвращение к продуктам питания, содержащим нерасщепляемое вещество. Исключение из рациона питания этих продуктов предотвращает возникновение патологии.
При дефекте фермента, участвующего в метаболизме определенного вещества в ткани, поступление его с пищей приводит к хроническому заболеванию в результате формирования дистрофического процесса. Так, поступление галактозы может приводить к поражению печени, хрусталика (галактоземия); фенилаланина - к слабоумию и неврологическим нарушениям (фенилпировиноградная олигофрения); наличие в пище значительного количества пуринов способствует отложению солей мочевой кислоты в суставах и формированию артритов (подагра). Такие заболевания часто тоже называют наследственными, т. к. они возникают только у лиц с определенной генетической особенностью. Однако здесь, в отличие от строго наследственных

30
заболеваний, формирование повреждения может быть предотвращено, то есть эффективна профилактика путем устранения из пищи нежелательного вещества.
Четвертую группу проявлений аномалий конституции составляют такие особенности, которые сами по себе не ведут к формированию повреждения, но обусловливают повышенную ранимость человека при воздействии нескольких разных средовых факторов, не опасных для других людей, а не одного конкретного, как в третьей группе. Например, дефекты некоторых ферментов в эритроцитах могут приводить к анемии или клинически не проявляться. Такие люди повышенно устойчивы к малярии. Поэтому эти гены широко распространены в тех районах земного шара, где малярия веками была фактором естественного отбора.
Надо иметь в виду, что люди с дефектами ферментов эритроцитов не переносят сульфаниламидов, салицилатов, барбитуратов, противомалярийных препаратов и многих других лекарств и химических веществ с прооксидантным действием, т. к. они в относительно малых дозах вызывают у этих людей гемолиз. Гемолиз может возникнуть у них при употреблении в пищу некоторых бобовых растений, красной смородины.
Лица гетерозиготные но S-Hb (AS) имеют в эритроцитах приблизительно 15% этой аномальной формы. Они в 13 раз устойчивее к малярии, чем люди гомозиготные по А гемоглобину (АА). Они здоровы, однако если у такого человека по любой причине возникнет ацидоз, присутствие S- гемоглобина обнаружит себя тем, что эритроциты примут серповидную форму, в связи с чем нарушится микроциркуляция и произойдет гемолиз.
Улюдей, имеющих пониженную активность а 1-антитрипсина в легких (что само по себе повреждения не вызывает), очень неблагоприятно, с преобладанием альтерации, текут воспалительные процессы в легких. Поэтому они плохо переносят любую запыленность воздуха. При работе в условиях запыленности прежде всего у них возникает хроническая пневмония, пневмосклероз, эмфизема, бронхоэктатическая болезнь. Злокачественно, с массивным распадом ткани течет у них туберкулез легких.
Улюдей, имеющих конституциональную недостаточность иммунологической системы или системы фагоцитов, повышена восприимчивость к микроорганизмам. Инфекционный процесс часто принимает у них характер сепсиса.
Улиц с конституциональными дефектами свертывающей системы крови (гемофилии А, В, С, афибриногенемия) в результате любых, даже минимальных, травмирующих воздействий возникают опасные кровотечения, кровоизлияния с последующим формированием анемии, тугоподвижности суставов и т.п.
Здесь тоже возможна профилактика путем устранения всех опасных для данного человека воздействий внешней среды.
Пятую группу проявлений конституциональной патологии составляют заболевания, которые называют и полигенными, и наследственно-обусловленными, и мультифакториальными. Последним подчеркивают роль многих факторов наследственных и средовых в возникновении патологии, а также то, что это гетерогенные, неоднозначные понятия, хотя и именуемые пока что "нозологическими единицами". Это болезни - генокопии, формирующиеся по принципу аддитивно-полигенного
