
- •Оглавление
- •Раздел I. Общие сведения о высокомолекулярных соединениях
- •1.1. Особенности полимерного состояния вещества Введение
- •1.1.1. Полимеры, общие определения
- •1.1.2. Различия в свойствах высоко- и низкомолекулярных соединений
- •1.2. Образование, получение и распространение полимеров
- •Содержание различных веществ в теле человека
- •Некоторые аминокислоты, входящие в состав белков
- •Содержание различных оксидов в базальтовых породах, мас. %
- •1.3. Классификация полимеров
- •1.3.1. Принципы классификации полимеров
- •Типичные конденсационные полимеры
- •Типичные полимеризационные полимеры
- •Классификация, молекулярно-массовые характеристики и стереохимия полимеров
- •1.3.2. Тривиальная, рациональная и систематическая номенклатура полимеров
- •Названия некоторых линейных полимеров
- •1.3.3. Классификация и номенклатура сополимеров
- •Названия некоторых элементорганических и неорганических полимеров
- •Название основных типов сополимеров
- •1.4. Молекулярно-массовые характеристики полимеров
- •1.4.1. Распределение макромолекул по молекулярным массам
- •1.4.2. Моменты распределения и средние молекулярные массы
- •1.4.3. Параметр полидисперсности
- •1.4.4. Методы определения молекулярной массы полимеров
- •1.5. Стереохимия полимеров
- •1.5.1. Химическая изомерия звеньев
- •1.5.3. Стереоизомерия
- •Температуры кристаллизации и плавления полидиенов
- •Вопросы и упражнения к лекциям 1-2
- •Раздел II. Синтез полимеров методами цепной и ступенчатой полимеризации
- •2.1. Радикальная полимеризации
- •2.1.1. Инициирование радикальной полимеризации
- •Важнейшие инициаторы радикальной полимеризации
- •2.1.2. Элементарные реакции и кинетика полимеризации
- •1. Инициирование.
- •2. Рост цепи.
- •3. Обрыв цепи.
- •Вклад диспропорционирования в реакциях обрыва (λ) для различных мономеров
- •Относительные константы передачи цепи на инициатор Син при 60ºС
- •Относительные константы передачи цепи на мономер См
- •Значения относительных констант передачи цепи Сs·104 на некоторые соединения при 60-70ºС
- •Значения относительных констант передачи цепи на полимер Ср
- •Ингибиторы радикальной полимеризации.
- •Константы ингибирования Сz, 50-60ºС
- •Константы скоростей элементарных реакций роста и обрыва при радикальной полимеризации некоторых мономеров, 20-25ºС
- •2.1.3. Молекулярно-массовое распределение при радикальной полимеризации
- •2.1.4. Влияние температуры и давления на радикальную полимеризацию
- •2.1.5. Диффузионная модель обрыва цепи. Гель-эффект
- •Влияние степени превращения мономера q на полимеризацию метилметакрилата, 22,5ºС
- •2.1.6. Каталитическая передача цепи
- •2.1.7. Псевдоживая радикальная полимеризация
- •Константы обратимого ингибирования псевдоживой полимеризации стирола в присутствии темпо
- •2.1.8. Эмульсионная полимеризация
- •Эмульсионная полимеризация смеси стирола и бутадиена
- •Вопросы и упражнения к лекциям 3-5
- •2.2. Катионная полимеризация
- •2.2.1. Элементарные реакции. Кинетика
- •Константы скорости роста в катионной полимеризации
- •Константы передачи цепи на мономер при катионной полимеризации стирола
- •Константы передачи цепи на мономер при катионной полимеризации изобутилена в различных растворителях
- •Контсанты передачи цепи при катионной полимеризации стирола
- •2.2.2. Псевдокатионная и псевдоживая катионная полимеризация
- •2.2.3. Влияние реакционной среды
- •Влияние растворителя на катионную полимеризацию стирола, инициированную hClO4
- •2.3. Анионная полимеризация
- •2.3.1. Основные реакции инициирования
- •2.3.2. Кинетика анионной полимеризации с обрывом цепи
- •2.3.3. Живая полимеризация. Блок-сополимеры
- •2.3.4. Полимеризация с переносом группы
- •2.3.5. Влияние температуры, растворителя и противоиона
- •Влияние растворителя на анионную «живую» полимеризацию стирола, 25ºС, натрий-нафталиновый комплекс 3·10-3 моль/л
- •Кинетические и термодинамические характеристики реакции роста цепи при живой полимеризации стирола, инициируемой натрий-нафталином, 20ºС, тетрагидрофуран
- •2.3.6. Ассоциация
- •2.4. Ионно-координационная полимеризация
- •Примеры стереоспецифической полимеризации
- •2.4.1. Катализаторы Циглера-Натта. Исторический аспект
- •Компоненты катализаторов Циглера-Натта
- •2.4.2. Полимеризация на гетерогенных катализаторах Циглера-Натта
- •Влияние растворителя на анионную полимеризацию 1,3-диенов, инициируемую н-бутиллитием
- •2.5. Синтез гетероцепных полимеров ионной полимеризацией
- •2.5.1. Карбонилсодержащие соединения
- •Предельные температуры и концентрации мономеров при полимеризации альдегидов
- •2.5.2. Полимеризация эфиров и эпоксидов с раскрытием цикла
- •2.5.3. Полимеризация лактамов и лактонов
- •2.5.4. Другие гетероциклы
- •2.6. Общие вопросы синтеза полимеров
- •2.6.1. Термодинамика синтеза
- •Энтальпии и энтропии полимеризации некоторых мономеров, 25ºС
- •Энтальпии δн0, энтропии δs0, функции Гиббса δg0 и предельные температуры полимеризации Тп альдегидов, 25ºС
- •Энтальпии δн0, энтропии δs0, функции Гиббса δg0 полимеризации циклоалканов при 25ºС
- •2.6.2. Сопоставление ионной и радикальной полимеризации
- •2.6.3. Об общности процессов псевдоживой полимеризации
- •2.7. Ступенчатая полимеризация
- •2.7.1. Равновесная и неравновесная поликонденсация
- •Влияние константы равновесия к на степень завершенности реакции поликонденсации х и среднечисловую степень полимеризации
- •Влияние воды на степень полимеризации при поликонденсации
- •2.7.2. Кинетика поликонденсации
- •Константы скорости реакции этерификации в гомолитических рядах одно- и двухосновных кислот, 25ºС
- •2.7.3. Молекулярно-массовое распределение полимера при поликонденсации
- •2.7.4. Разветвленные и сшитые полимеры
- •2.7.5. Фенопласты, аминопласты
- •2.7.6. Полиамиды, полиэфиры, поликарбонаты
- •2.7.7. Полиуретаны. Полисилоксаны
- •2.7.8. Жесткоцепные ароматические полимеры
- •Свойства полиариленэфирсульфонов
- •2.7.9. Сверхразветвленные полимеры
- •Очистка — б — очистка — а — очистка и т. Д.
- •Вопросы и упражнения к лекциям 9-10
- •Раздел 3. Цепная сополимеризация
- •3.1. Количественная теория сополимеризации
- •3.1.1. Кривые состава сополимера и относительные активности мономеров
- •3.1.2. Состав и микроструктура сополимера. Статистический подход
- •Доля последовательностей различной длины из мономера 1 (q1n) в эквимолярных сополимерах различных типов
- •3.1.3. Многокомпонентная сополимеризация
- •Предсказанные и определенные экспериментально составы сополимеров, полученных радикальной тер- и тетраполимеризацией
- •3.1.4. Сополимеризации до глубоких конверсии
- •3.2. Радикальная сополимеризация
- •3.2.1. Скорость сополимеризации
- •Корреляция между и r1 · r2 при радикальной сополимеризации
- •3.2.2. Природа эффекта предконцевого звена
- •Относительные активности мономеров при сополимеризации стирола (1) с акрилонитрилом (2), определенные в рамках моделей концевого и предконцевого звена, 60°с
- •3.2.3. Влияние температуры и давления на радикальную сополимеризацию
- •Значения относительных активностей мономеров при разных температурах и отношения частотных факторов
- •Влияние давления на сополимеризацию некоторых мономеров
- •3.2.4. Чередующаяся сополимеризация
- •1 Бутилметакрилат - диметилбутадиен, 2 - бутилметакрилат - (с2н5)3АlСl - диме-тилбутадиен; f1 мольная доля бутилметакрилата в исходной мономерной смеси
- •3.2.5. Влияние реакционной среды
- •3.2.6. Связь строения мономера и радикала с реакционной способностью.
- •Сополимеризация винилацетата (1) с хлорзамещенными этилена (2)
- •Влияние резонансного фактора на величину константы скорости роста, 20-30°с
- •Эмпирические и расчетные квантово-химические резонансные параметры строения мономеров и радикалов
- •Значения константы скорости реакции роста и параметра е некоторых мономеров, 25-30°с
- •Значения константы скорости реакции роста и параметра е пара-замещенных стирола, 60°с
- •Значения параметров реакционной способности мономеров схемы q-e
- •Относительные активности при сополимеризации некоторых мономеров
- •3.3. Ионная сополимеризация
- •3.3.1. Катионная сополимеризация
- •Катионная сополимеризация некоторых мономеров
- •3.3.2. Анионная сополимеризация
- •Анионная сополимеризация стирола (1) с бутадиеном-1,3 (2), инициатор н-с4н9Li
- •Влияние растворителя и противоиона на состав сополимера при сополимеризации стирола с изопреном
- •3.3.3. Сополимеризация на катализаторах Циглера-Натта
- •Реакционная способность различных мономеров в сополимеризации Циглера-Натта
- •Раздел 4. Химические превращения полимеров
- •4.1. Характерные особенности макромолекул как реагентов
- •4.1.1. Влияние соседних звеньев
- •4.1.2. Макромолекулярные и надмолекулярные эффекты
- •4.1.3. Кооперативные взаимодействия7
- •4.2. Сшивание полимеров
- •4.2.1. Высыхание красок
- •4.2.2. Вулканизация каучуков
- •4.2.3. Отверждение эпоксидных смол
- •4.3. Деструкция полимеров
- •4.3.1. Термическая деструкция. Циклизация
- •Температуры начала разложения и энергии активации термического распада некоторых полимеров
- •Продукты термического распада некоторых полимеров
- •Выход мономера при термическом распаде различных полимеров
- •4.3.2. Термоокислительная деструкция. Горение
- •Ограниченный кислородный показатель для некоторых полимеров
- •4.3.3. Фотодеструкция. Фотоокисление
- •4.4 Полимераналогичные превращения
- •4.4.1. Поливиниловый спирт
- •4.4.2. Химические превращения целлюлозы
- •4.4.3. Структурная модификация целлюлозы
- •Вопросы и упражнения к лекциям 11-15
Ограниченный кислородный показатель для некоторых полимеров
|
Полимер |
ОКП, мол.% |
Полимер |
ОКП, мол.% |
|
Полиоксиметилен Полиметилметакрилат Полиэтилен Полипропилен Полистирол Поливиниловый спирт |
16 17 17 17 18 22 |
Нейлон Полифениленоксид Поливинилхлорид Поливинилиденхлорид Политетрафторэтилен |
25 30 47 60 95 |
4.3.3. Фотодеструкция. Фотоокисление
Фотохимические превращения происходят в полимере под действием ультрафиолетового (180 < λ < 400нм) и видимого света (400 < λ < 800 нм), если полимер содержит химические связи или группы, поглощающие свет в этих областях спектра (так называемые хромофорные группы). При поглощении фотона хромофорные группы переходят в возбужденное состояние, энергия которого может превысить энергию диссоциации химической связи. В этом случае связь диссоциирует с образованием радикалов, которые вызывают вторичные, так называемые темновые, фотохимические реакции распада, деполимеризации, изомеризации, передачи цепи и т.д. Следует иметь в виду, что возбужденные хромофорные группы могут дезактивироваться, поэтому квантовый выход (отношение числа квантов, вызвавших реакцию, к общему числу поглощенных квантов) обычно очень мал, порядка 10-4.
Солнечный свет, достигший поверхности Земли, содержит ультрафиолетовый участок спектра с λ ≥ 270 нм. Казалось бы, что интенсивной фотодеструкции должны подвергаться лишь полимеры, содержащие в макромолекулах хромофорные группы, поглощающие свет в близкой области, карбонильные (λ = 279; 285нм), ароматические (λ ≥ 193; 260нм). Однако фотостарению под действием естественного освещения подвергаются практически все полимеры. Это обусловлено содержанием хромофорных групп в составе случайных примесей (пластификаторов, стабилизаторов) и в продуктах окисления полимера. Такие неконтролируемые хромофорные группы могут инициировать фотостарение полимера, выступая в качестве фотосенсибилизаторов или фотоинициаторов. Молекулы сенсибилизатора, поглотившие квант света, передают энергию возбуждения макромолекулам, что приводит к диссоциации химических связей. Фотоинициатор под действием света распадается на радикалы, которые инициируют цепные реакции с участием макромолекул.
Первичные процессы, в полимерах проходящие под действием света, зависят от природы хромофорной группы. Как уже указывалось, наиболее часто встречаются карбонильные и ароматические хромофорные группы. Карбонильные группы при облучении светом с длиной волны 270-330 нм легко переходят в возбужденное синглетное (антипараллельная ориентация спинов -связи) и триплетное (параллельная ориентация спинов) состояния. Затем идут процессы по механизму Норриша первого или второго типа. Ниже приведена схема реакций I и II типа сополимера этилена с оксидом углерода:
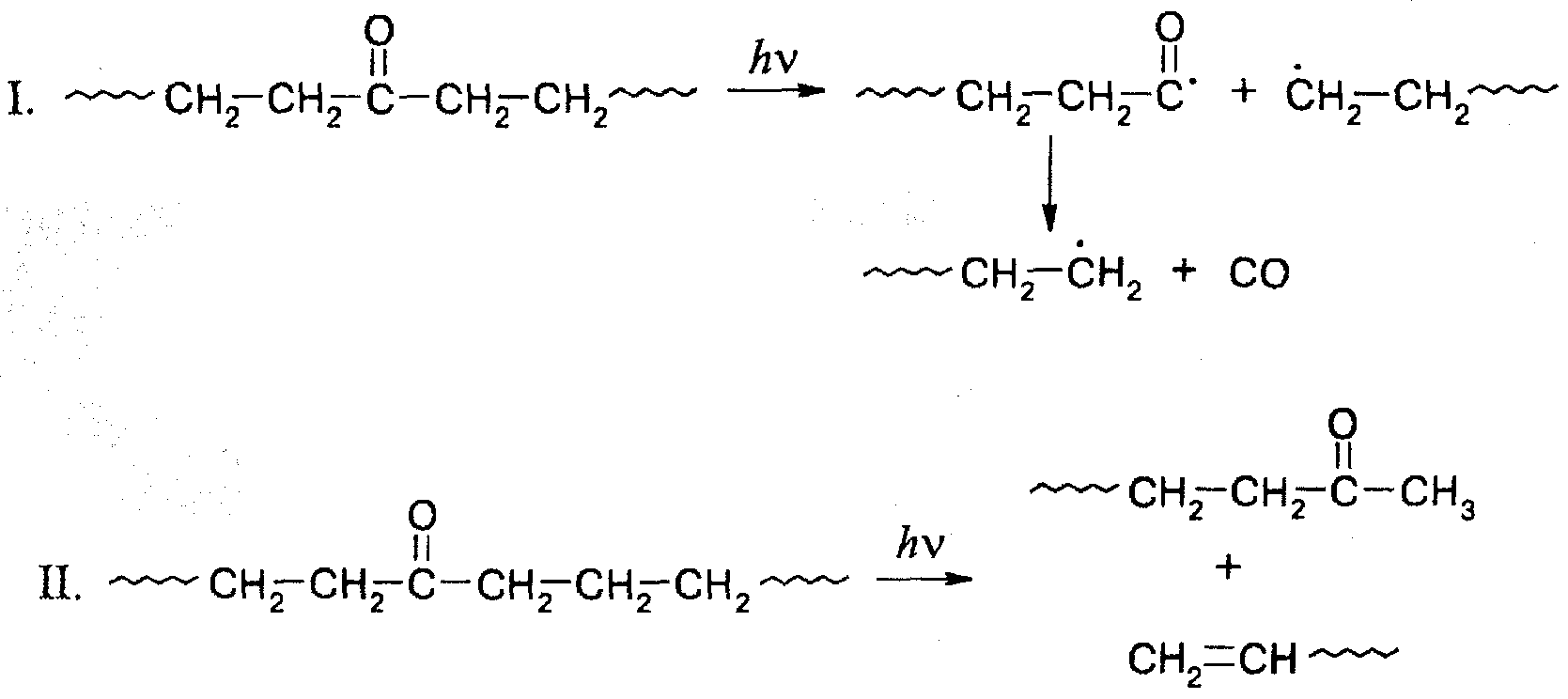
Как видно, реакция Норриша II типа протекает по радикальному, а реакция Норриша I типа по скрыторадикальному механизму. Обе реакции приводят к разрыву цепи. Свободные радикалы, образующиеся в реакции I типа, могут вызвать в дальнейшем превращения в полимере.
Реакция Норриша I типа играет важную роль в фотолизе полиуретанов (1), поликарбонатов (2), полиамидов (3):
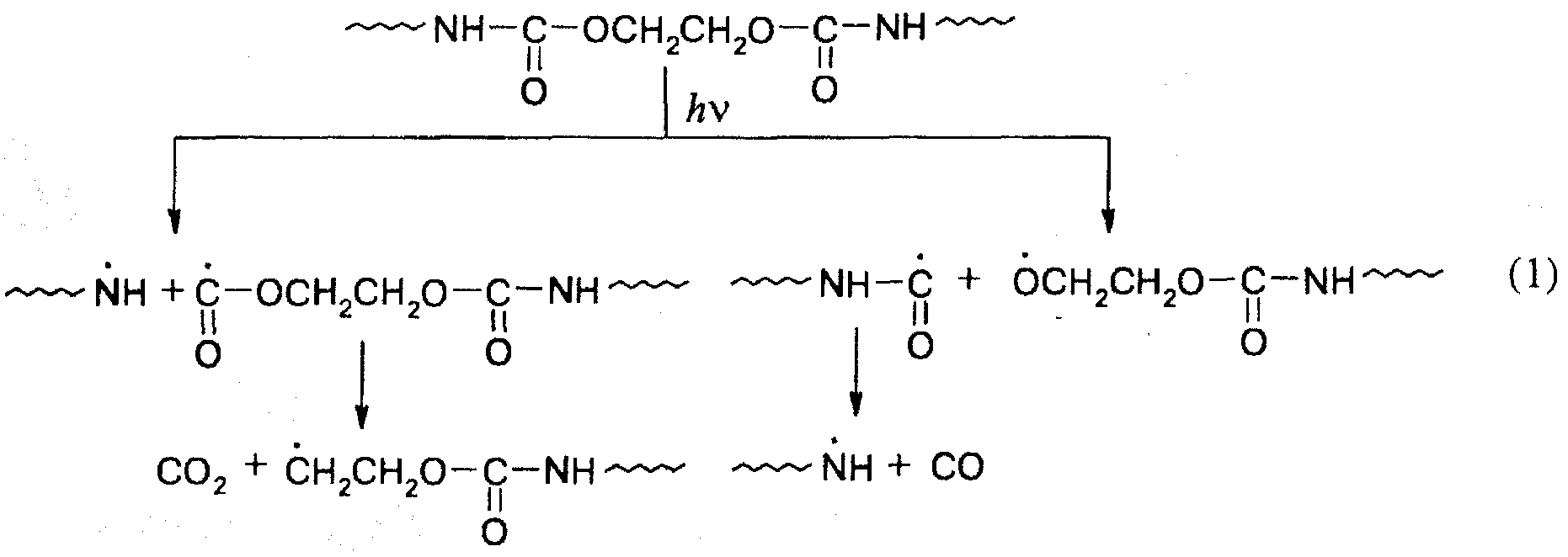
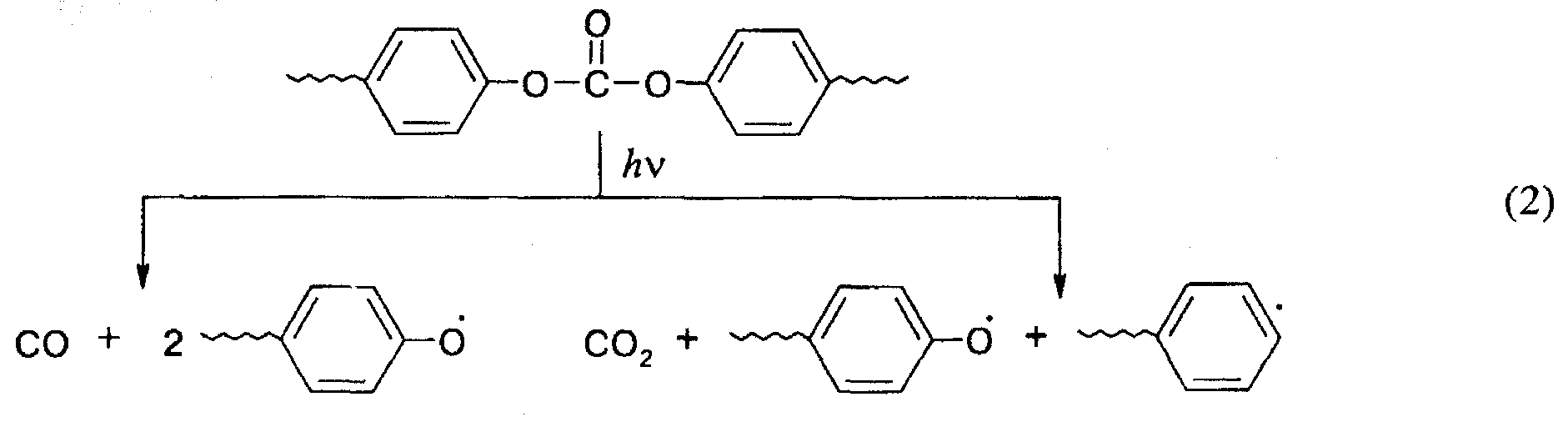
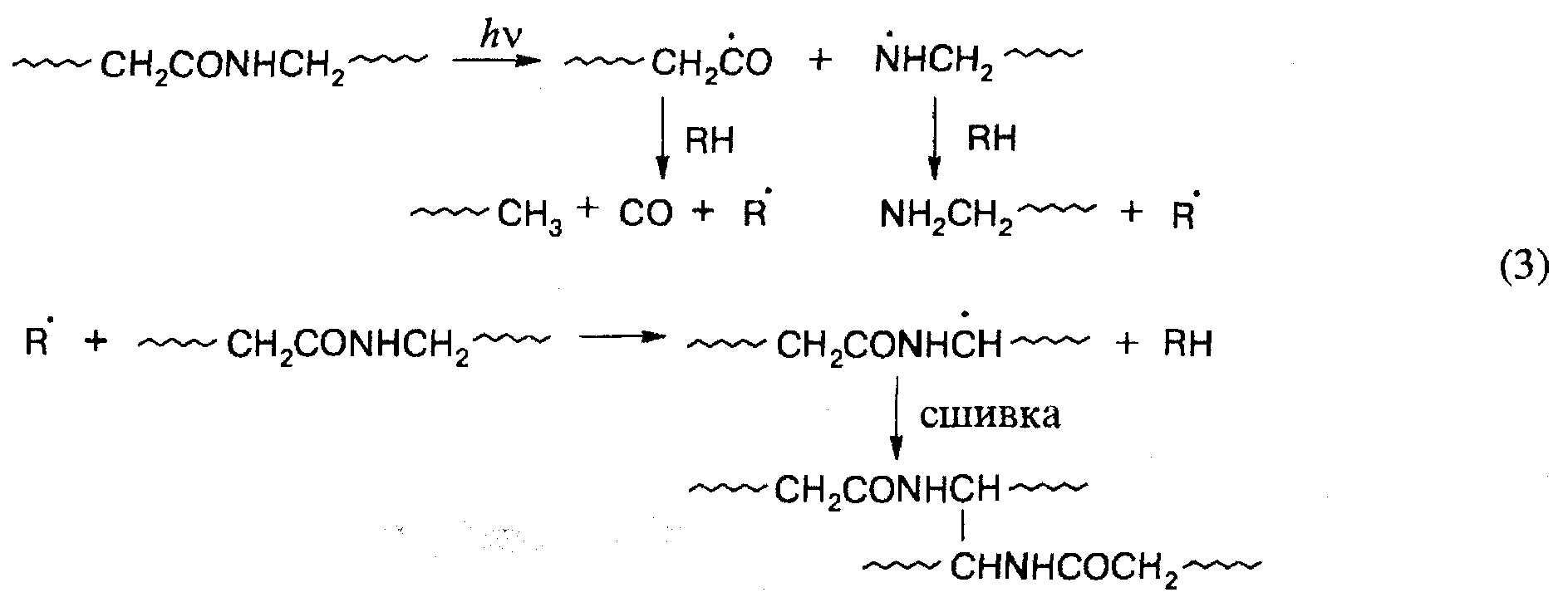
В качестве примера полимера, содержащего ароматические хромофорные группы, рассмотрим полистирол. Процесс фотолиза сопровождается выделением небольшого количества водорода, результатом фотолиза является пожелтение полимера и потеря им растворимости. Ниже представлена схема процесса, приводящего к этим изменениям:
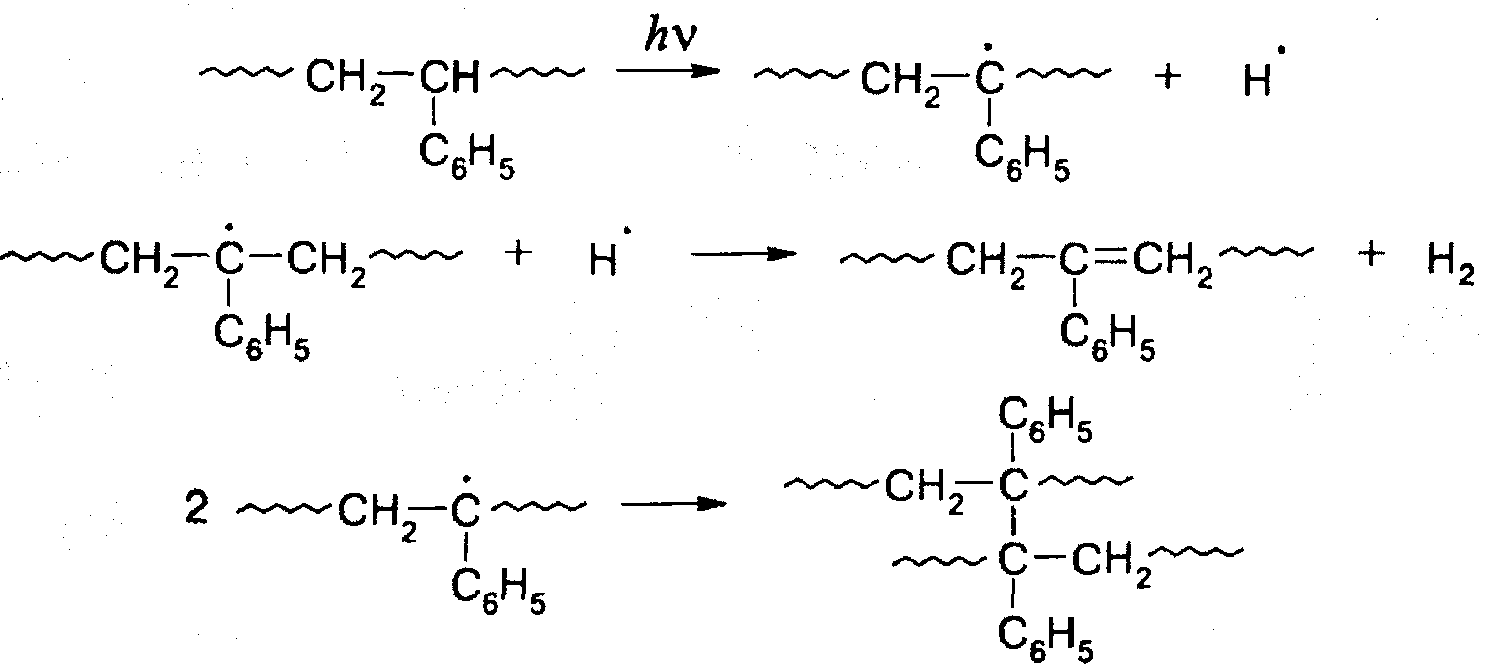
Первичным
актом является образование радикалов![]() врезультате
отрыва атомарного водорода от
возбужденного мономерного звена,
поглотившего квант света. Молекулярный
водород образуется в результате
рекомбинации атомов водорода, либо в
результате отрыва атома водорода от
соседнего атома углерода, что приводит
к образованию двойной связи.
Последовательное распространение этой
реакции вдоль цепи приводит к возникновению
«островков» сопряженных связей,
придающих окраску полимеру. Соединение
«срединных» радикалов приводит к сшивке
и потере растворимости полимером.
врезультате
отрыва атомарного водорода от
возбужденного мономерного звена,
поглотившего квант света. Молекулярный
водород образуется в результате
рекомбинации атомов водорода, либо в
результате отрыва атома водорода от
соседнего атома углерода, что приводит
к образованию двойной связи.
Последовательное распространение этой
реакции вдоль цепи приводит к возникновению
«островков» сопряженных связей,
придающих окраску полимеру. Соединение
«срединных» радикалов приводит к сшивке
и потере растворимости полимером.
Фотолиз полиметилметакрилата протекает с заметной скоростью при облучении полимера ультрафиолетовым излучением с λ ≤ 250нм. Поглощение полимером квантов света вызывает одновременное протекание реакций трех типов:
Разрыв основной цепи по закону случая:
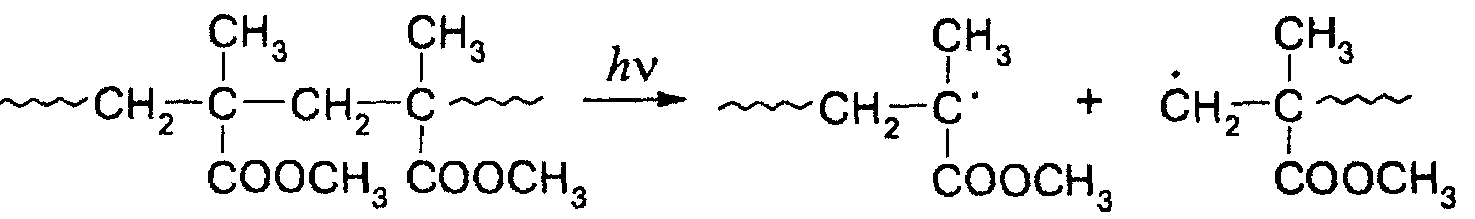
Распад эфирных групп:

Отщепление метильных заместителей:
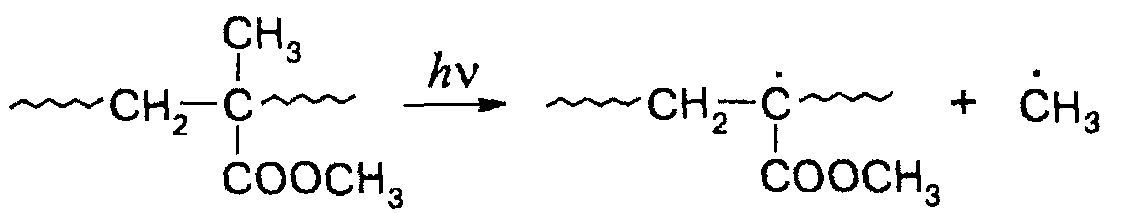
Из темновых реакций, вызываемых образовавшимися при фотолизе радикалами, наибольшее значение имеет деполимеризация. При комнатной температуре длина цепи деполимеризации незначительна и составляет пятьшесть мономерных звеньев на один разрыв цепи. С повышением температуры эта величина возрастает и при 160°С достигает 220 единиц.
Считается,
что при фотолизе полимеров метакриловых
и акриловых эфиров наиболее общей
реакцией является отрыв сложноэфирных
групп и образование «срединных»
радикалов
![]() .
Однако, если в случае полиметилметакрилата
эти радикалы приводят к разрыву цепи
посредством-распада,
то в случае полиметилакрилата они
рекомбинируют (соединяются), что
приводит к сшивке полимера. В обоих
случаях среди летучих преобладают
формальдегид, метанол, метан, оксид и
диоксид углерода. Их происхождение
ясно из приведенных выше схем.
.
Однако, если в случае полиметилметакрилата
эти радикалы приводят к разрыву цепи
посредством-распада,
то в случае полиметилакрилата они
рекомбинируют (соединяются), что
приводит к сшивке полимера. В обоих
случаях среди летучих преобладают
формальдегид, метанол, метан, оксид и
диоксид углерода. Их происхождение
ясно из приведенных выше схем.
Фотодеструкция полиэтилена и полипропилена вызывается хромофорными группами, находящимися в составе примесей, добавок, продуктов окисления полимера, а также дефектами макромолекулярной структуры. При поглощении ими квантов света образуются «первичные» радикалы, отрывающие атомы водорода от макромолекул. Образующиеся «срединные» макрорадикалы ответственны за сшивку и разрыв макромолекул, являющиеся основными результатами фотодеструкции полиолефинов:
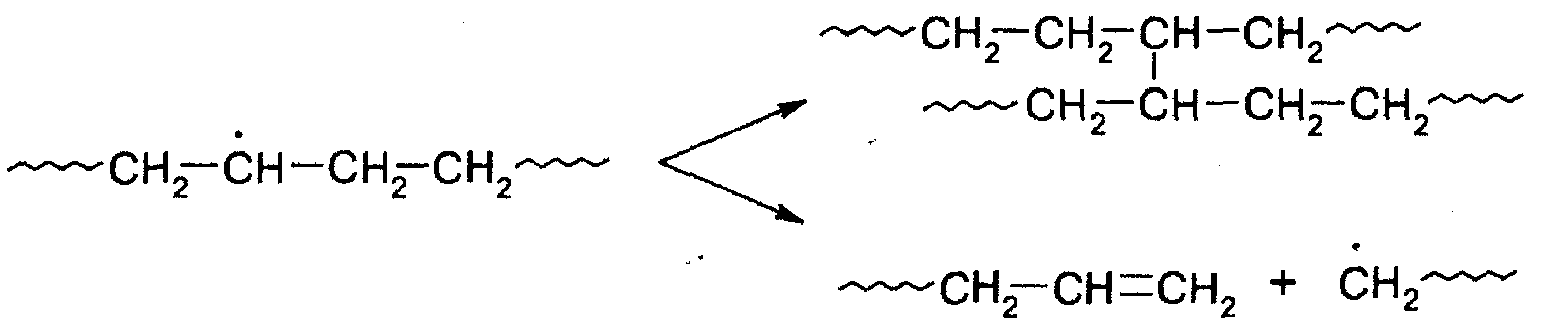
Фотоокисление. Хорошо известно, что полиэтиленовая пленка, используемая в парниках, не служит больше сезона. Причиной ее разрушения является фотоокислительная деструкция. Роль света в этом процессе заключается в инициировании процесса окисления.
Радикалы, инициирующие процесс окисления, возникают в результате поглощения света хромофорными группами. Они могут находиться в составе полимера, целевых добавок, например пластификатора, а также в виде примесей. Как правило, различные кислородсодержащие группы образуются в полимерах при их переработке через расплав. В частности, в полиэтилене были обнаружены карбонильные группы по возникновению полосы поглощения в области 1710-1735см-1 ИК-спектра. Поглощение кванта света карбонильной группой может приводить к возникновению радикалов по реакции Норриша I типа, а также по реакции:
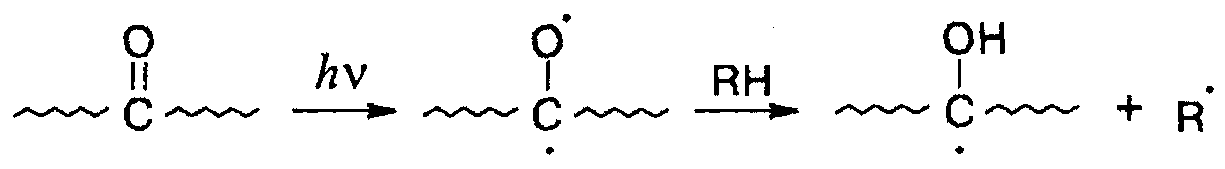
Выше упоминалось, что при окислении полимеров накапливаются гидропероксидные группы. Свет инициирует распад этих групп и, тем самым, инициирует автокаталитический цепной процесс окисления полимеров. В качестве характерного примера ниже приведена схема фотоокисления стирола:
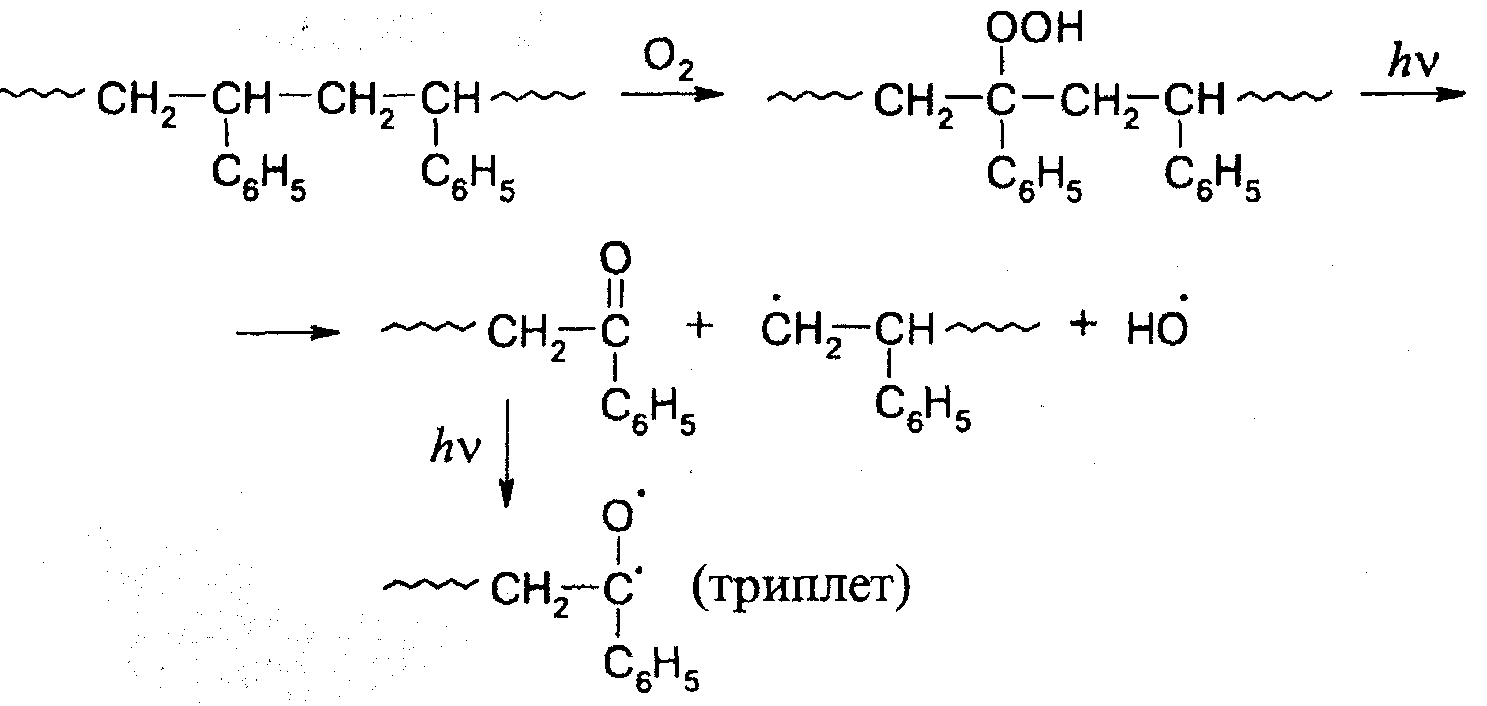
Для предотвращения фото- и фотоокислительной деструкции используют фотостабилизаторы, отражающие или поглощающие ультрафиолетовое излучение. К ним относятся сажа, оксиды металлов, салицилаты, о-оксибензофеноны, оксибензотриазолы и др.
