
- •Г. Б. Смирнов Механизмы приобретения и потери генетической информации бактериальными геномами гу нии эпидемиологии и микробиологии им. Н.Ф. Гамалеи рамн, 123098 Москва, ул. Гамалеи, 18.
- •(Успехи современной биологии, 2007)
- •I. Потеря и приобретение генетического материала.
- •I.1. Примеры редукции геномов.
- •I.2. Общепринятое объяснение редукции геномов.
- •I.3. Факты, которые трудно объяснить с помощью общепринятой концепции.
- •II. Молекулярные механизмы потери и приобретения генетического материала
- •II.1. Нуклеотидные последовательности в точках рекомбинации при интеграциях и делециях.
- •II.2. Сайты интеграции (tРнк, интегроны, is-элементы, короткие повторы).
- •II.3. Распределение is-элементов и повторяющихся последовательностей в геномах.
- •II.4. Образование повторов.
- •II.5. Молекулярные события, приводящие к геномным перестройкам.
- •III. Полинуклеотидный (Пн) выбор
- •III.1. Вклад Пн-выбора и фенотипического отбора в приобретение и потерю фенотипически значимых генов.
- •IV. Выбор пути эволюции генома. Гипотеза пульсации генома.
- •V. Заключение
- •Литература
II.4. Образование повторов.
Как возникают повторы, каковы их основные свойства и что определяет их распределение по геномам?
Геномы бактерий содержат преимущественно короткие тандемные повторы, такие как семейство"variable number of tandem repeats» (VNTR) и семейство «short sequence repeats» (SSR). Они могут образовываться как в результате рекомбинации, так и ошибок репликации при редактировании (slipped strand mispairing) или репарации [см. 104]. Установлено, что близко расположенные прямые повторы (close direct repeats — СDR) находятся в избытке по сравнению с повторами другимх типов во всех геномах. В наибольшей степени это характерно для одного из самых маленьких геномов M.genitalium. (Табл.4). Вцелом, динамика образования повторов в бактериальной ДНК выглядит следующим образом: короткие повторы служат праймерами для образования тандемных дупликаций (повторов), которые в свою очередь преобразуются в разбросанные (по геному) повторы [7] (Рис.5). Увеличение расстояния между повторами приводит к их стабилизации и достигается за счёт транспозиций (внедрения между повторами) и других геномных перестроек. Частота делеций частей повтора прямо пропорциональна размеру повторяющихся последовательностей и обратно пропорциональна длине спейсера, поэтому, чем длиннее повторы, тем больше должно быть расстояние между ними, чтобы обеспечить их стабильность [32, 61, 22, 78]. Перечисленные данные свидетельствуют о том, что размер, ориентация и взаимное расположение повторов определяет судьбу участков ДНК, находящихся между ними, или прилежащих к ним. Кроме того, перечисленные свойства повторов определяют вероятность внедрения в сайт, содержащий повторы, любых фрагментов ДНК, от IS-элементов до геномных островов.
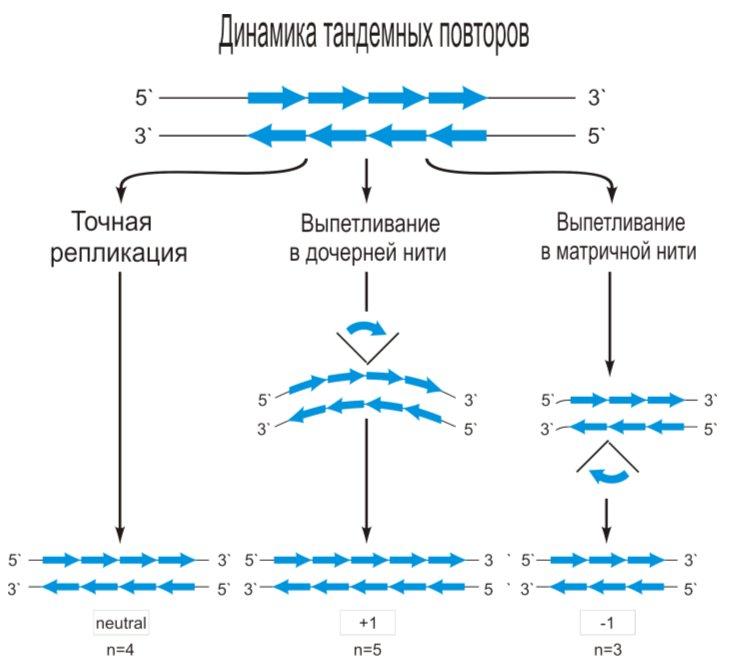
Рис. 5. Динамика тандемных повторов: экспансия и редукция.
II.5. Молекулярные события, приводящие к геномным перестройкам.
Таким образом, наиболее вероятная последовательность эволюционно важных событий в геномах представляется следующим образом. Сначала за счёт ошибок (проскальзывания) репликации возникают близко расположенные короткие тандемные повторы, которые могут дуплицироваться и за счёт геномных перестроек распространяются по геному. Уже эти повторы могут генерировать делеции. Повторы могут служить сайтами интеграции для IS-элементов. IS-элементы и другие МГЭ также являются горячими точками для рекомбинаций, приводящих к делециям (прямая ориентация) или другим геномным перестройкам: инсерциям и инверсиям (инвертированные повторы). Инвертированные повторы составляют основу специализированных сайтов интеграции в составе интегронов и генов тРНК, куда внедряются генные кассеты и геномные острова из других геномов. Все перечисленные генетические элементы распределены в геномах неслучайно и в той или иной степени видоспецифично. Соответственно неслучайными и видоспецифичными являются геномные перестройки, стимулируемые повторами и различными МГЭ. Таким образом, структура генома направляет его эволюционное развитие. К таким же выводам о роли структуры генома в его эволюции пришла Линн Хелена Капорале [см. 29, 30].
