
- •Кафедра химии
- •Содержание
- •Общие правила работы в лаборатории
- •Правила техники безопасности
- •Оказание первой помощи
- •Порядок оформления работ
- •Общая химия
- •Тема 1. Растворы
- •Работа 1. Приготовление рабочего 0,1n раствора hCl
- •Плотность растворов соляной кислоты
- •Работа 2. Определение нормальности рабочего раствора hCl по 0,1n раствору NaOh
- •Работа 3. Древовидные образования
- •Работа 4. Рост искусственной «клетки» Траубе
- •Тема 2. Гетерогенные равновесия и процессы
- •Работа 5. Определение хлоридов мочи по Мору
- •Тема 3. Комплексонометрия
- •Работа 6. Определение общей жесткости воды трилонометрическим методом.
- •Тема 4. Протолитические равновесия и процессы
- •Работа 7. Приготовление буферных растворов
- •Тема 5. Электрохимия
- •Работа 10. Потенциометрический метод определения рН растворов при помощи стеклянного электрода
- •Тема 6. Поверхностные явления. Хроматография
- •Работа 11. Разделение минеральных солей на колонках с твердым адсорбентом
- •Работа 12. Радиальная распределительная хроматография
- •Тема 7. Дисперсные системы
- •Работа 13. Метод замены растворителя
- •Работа 14. Получение золя гидроксида железа (III)
- •Работа 15. Получение золя гексацианоферрата (II) меди
- •Работа 16. Изучение процесса коагуляции коллоидных растворов
- •Тема 8. Растворы вмс
- •Работа 17. Изучение процесса денатурации белка
- •Работа 18. Изучение процесса высаливания белка
- •Биоорганическая химия
- •Тема 1. Спирты, фенолы
- •Тема 2. Тиолы, амины
- •Тема 3. Альдегиды и кетоны
- •Тема 4. Карбоновые кислоты
- •Работа 16. Обнаружение фенольного гидроксила в карбоновых кислотах
- •Тема 5. Аминокислоты. Белки
- •Работа 20. Нингидриновая реакция на α-аминокислоты
- •Тема 6. Липиды
- •Тема 7. Углеводы
- •Дисахариды. Полисахариды
- •Тема 8. Нуклеиновые кислоты
- •Литература
Работа 20. Нингидриновая реакция на α-аминокислоты
Выполнение работы: в пробирку наливают 2 мл 1%-ного раствора яичного белка и прибавляют 2-3 капли 0,1% -ного раствора нингидрина. Смесь кипятят в течение 1-2 минут. Появляется розовато-фиолетовое или сине-фиолетовое окрашивание. При стоянии раствор синеет. Окрашивание указывает на наличие a - аминогруппы.
.
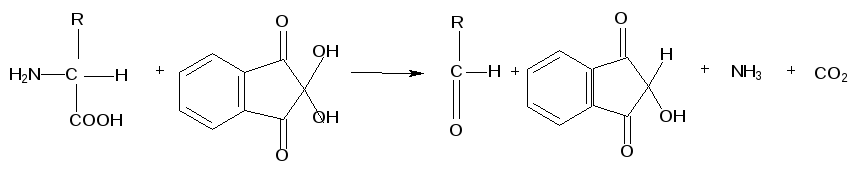
|
a‑аминокислота |
нингидрин |
альдегид |
восстановленная форма нингидрина (гидриндантин) |

продукт конденсации сине-фиолетового цвета
Аминокислоты, входящие в состав белковых молекул, являются L-α- аминокислотами. Для них характерна реакция с нингидрином. Для пролина и гидроксипролина нингидриновая реакция не характерна, так как это иминокислоты.
Работа 21. Реакция Адамкевича на наличие триптофана в белке
Выполнение работы: в первую пробирку наливают 5 капель 1% раствора яичного белка, во вторую – 5 капель 1% раствора желатина. В обе пробирки добавляют по 5 капель концентрированной уксусной кислоты, слегка нагревают, затем охлаждают и по стенке пробирки (осторожно), чтобы жидкости не смешивались, приливают 10 капель концентрированной серной кислоты. В первой пробирке на границе двух слоев наблюдается красно-фиолетовое окрашивание в виде кольца, постепенно распространяющееся на всю жидкость. В пробирке с раствором желатина реакция отрицательна, так как в желатине нет триптофана.
Тема 6. Липиды
В этом разделе представлены работы по изучению химических свойств жиров (масел). Липиды – большая группа органических соединений. Их роль в организме многогранна. Чаще они являются сложными эфирами спиртов (глицерин, холестерин и др.) и высших жирных карбоновых кислот. Триацилглицерины (нейтральные жиры) являются сложными эфирами глицерина и высших жирных кислот. Наиболее распространенными кислотами, входящими в состав липидов, являются пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая и арахидоновая. Весьма важными группами липидов, входящих в организм человека, являются фосфолипиды (лецитины, кефалины и др.), сфинголипиды, гликолипиды. Наиболее распространенными из глицеролфосфатидов являются лецитины, состоящие из глицерина, высших жирных кислот, фосфорной кислоты и холина. Отличаются лецитины друг от друга жирными кислотами, как и другие фосфатидилглицерины.
Задача работы: научиться экспериментально доказывать наличие в липидах основных структурных компонентов; определять степень насыщенности высших жирных кислот; осуществлять омыление жиров.
Оборудование, материалы: растительное масло, 35 %-ный и 10% -ный раствор NaOH, кристаллический гидросульфат калия, 1%-ный раствор перманганата калия, 10%- ный раствор карбоната натрия, лецитин, 10%-ный раствор соляной кислоты, насыщенный раствор молибдата аммония, аскорбиновая кислота, фарфоровая чашка, стеклянные палочки, плитка, дистиллированная вода, пипетки, пробирки, спиртовка.
Работа 22 . Омыление жиров.
Выполнение работы: В небольшую фарфоровую чашку поместите 0,5 мл растительного масла и 4 капли 35 %-ного раствора NaOH. Стеклянной палочкой размешайте щелочь с маслом до получения однородной эмульсии. Затем поставьте чашку на электрическую плитку и при незначительном нагревании продолжайте помешивать, пока не получится однородная прозрачная слегка желтоватая жидкость. Затем добавьте 2 мл дистиллированной воды и вновь нагрейте, тщательно перемешивая до полного упаривания воды. Снимите чашку с электрической плитки. Получится кусочек твердого белого мыла.
Работа 23 . Открытие глицерина в жире
Выполнение работы: В пробирку наливают 2 - 3 капли жира, добавляют несколько кристалликов гидросульфата калия. Содержимое нагревают, образуется акролеин, который легко узнается по резкому удушливому запаху.
акролеин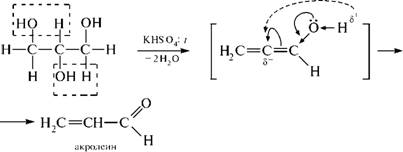
Работа 24. Гидролиз лецитинов и открытие составных частей
Выполнение работы: В пробирку наливают 10 капель раствора лецитина и добавляют 20 капель 10% -ного раствора гидроксида натрия, содержимое осторожно кипятят 2-3 минуты. Холин, образующийся при гидролизе, превращается в триметиламин, который имеет запах селедочного рассола. К нескольким каплям гидролизата добавляется двойной объем 10% - ного раствора соляной кислоты, выпадает осадок свободных жирных кислот. Для открытия солей фосфорной кислоты к 5 каплям гидролизата добавляют такие же количества молибденового реактива и аскорбиновой кислоты. Жидкость окрашивается в синий цвет. Глицерин открывают по реакции образования хелатного соединения с Cu(OH)2.
С



 Н2
–О – СО -C17H35СН2 –ОH+C17H35COONa
Н2
–О – СО -C17H35СН2 –ОH+C17H35COONa
а

 )
CH – O – CO – C17H33
+ 5NaOH
CH – OH +
C17H33COONa
)
CH – O – CO – C17H33
+ 5NaOH
CH – OH +
C17H33COONa

 O +
O +
C H2
–O –P-O-CH2-CH2-N≡(CH3)3
CH2 –OH
+ Na3PO4
H2
–O –P-O-CH2-CH2-N≡(CH3)3
CH2 –OH
+ Na3PO4
OH
лецитин (фосфатидилхолин)
HO-CH2-CH2-N+≡(CH3)3
холин
↓
(СН3)3N
триметиламин
б) Na3PO4+ молибденовый реактив + аскорбиновая кислота → осадок синего цвета
Работа 25 . Определение непредельности жира
Выполнение работы: В пробирку наливают по 0,5 мл подсолнечного масла и прибавляют 1 мл 1% -ного раствора перманганата калия и 10%- ного раствора карбоната натрия. Содержимое пробирки встряхивают. Через некоторое время окраска раствора перманганата калия исчезает.

