
- •Кафедра химии
- •Содержание
- •Общие правила работы в лаборатории
- •Правила техники безопасности
- •Оказание первой помощи
- •Порядок оформления работ
- •Общая химия
- •Тема 1. Растворы
- •Работа 1. Приготовление рабочего 0,1n раствора hCl
- •Плотность растворов соляной кислоты
- •Работа 2. Определение нормальности рабочего раствора hCl по 0,1n раствору NaOh
- •Работа 3. Древовидные образования
- •Работа 4. Рост искусственной «клетки» Траубе
- •Тема 2. Гетерогенные равновесия и процессы
- •Работа 5. Определение хлоридов мочи по Мору
- •Тема 3. Комплексонометрия
- •Работа 6. Определение общей жесткости воды трилонометрическим методом.
- •Тема 4. Протолитические равновесия и процессы
- •Работа 7. Приготовление буферных растворов
- •Тема 5. Электрохимия
- •Работа 10. Потенциометрический метод определения рН растворов при помощи стеклянного электрода
- •Тема 6. Поверхностные явления. Хроматография
- •Работа 11. Разделение минеральных солей на колонках с твердым адсорбентом
- •Работа 12. Радиальная распределительная хроматография
- •Тема 7. Дисперсные системы
- •Работа 13. Метод замены растворителя
- •Работа 14. Получение золя гидроксида железа (III)
- •Работа 15. Получение золя гексацианоферрата (II) меди
- •Работа 16. Изучение процесса коагуляции коллоидных растворов
- •Тема 8. Растворы вмс
- •Работа 17. Изучение процесса денатурации белка
- •Работа 18. Изучение процесса высаливания белка
- •Биоорганическая химия
- •Тема 1. Спирты, фенолы
- •Тема 2. Тиолы, амины
- •Тема 3. Альдегиды и кетоны
- •Тема 4. Карбоновые кислоты
- •Работа 16. Обнаружение фенольного гидроксила в карбоновых кислотах
- •Тема 5. Аминокислоты. Белки
- •Работа 20. Нингидриновая реакция на α-аминокислоты
- •Тема 6. Липиды
- •Тема 7. Углеводы
- •Дисахариды. Полисахариды
- •Тема 8. Нуклеиновые кислоты
- •Литература
Тема 2. Тиолы, амины
В этом разделе представлены работы по изучению свойств аминов. Анилин находит широкое применение для получения различных лекарственных веществ, в частности сульфаниламидных препаратов и многих других соединений.
Задача работ: познакомиттся с методом получения и изучить химические свойства анилина.
Оборудование, материалы: нитробензол, металлический цинк, дистиллированная вода, хромовая смесь, анилин, концентрированная соляная и серная кислоты, пробирки, пипетки.
Работа 5. Восстановление нитробензола в анилин
При выполнении работ с анилином необходимо учитывать, что он проникает в организм через кожу или при вдыхании паров и действует на кровяные и нервные клетки.
Выполнение работы: В пробирку помещают 3 - 4 капли нитробензола, 5 - 6 капель концентрированной соляной кислоты и кусочек металлического цинка. Пробирку все время встряхивают. Выделяющийся водород восстанавливает нитробензол, о чем можно судить по исчезновению верхнего маслянистого слоя с характерным горькоминдальным запахом. В результате реакции получается прозрачный раствор гидрохлорида анилина (свободный анилин плохо растворим в воде). Раствор сохраняют для следующей работы.


 [H]
[H]




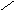
 NO2--------------→NH2+ 2Н2О
NO2--------------→NH2+ 2Н2О
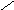 HCI,Zn
HCI,Zn
нитробензол анилин




 +
+





 NH2
NH3
NH2
NH3

 + HCI
CI--
+ HCI
CI--
гидрохлорид анилина
(анилинийхлорид)
Работа 6. Окисление анилина
Выполнение работы: В пробирку наливают 1 мл раствора солянокислого анилина (гидрохлорида анилина) и 4-5 капель хромовой смеси. Содержимое пробирки окрашивается в темно-зеленый цвет, переходящий в синий, а затем в черный. «Черный анилин» является продуктом сложного строения и применяется как краситель.
Работа 7. Образование солей анилина
Выполнение работы: В две пробирки наливают по 1 мл дистиллированной воды, по 2 капли анилина и встряхивают. В обеих пробирках получается эмульсия анилина вследствие его плохой растворимости в воде. В первую пробирку прибавляют 0,5 мл соляной кислоты, во вторую – серной.
После встряхивания содержимого в первой пробирке образуется прозрачный раствор хлорида фениламмония (анилинийхлорид), во второй – выпадает осадок гидросульфата фениламмония (анилинийгидросульфат).
С6Н5 - NH2 + HCl → [C6H5 - NH3]+ Cl-
анилин хлорид фениламмония
С6Н5 - NH2 + H2SO4 → [C6H5 - NH3]+ HSO4-
анилин гидросульфат фениламмония
Тема 3. Альдегиды и кетоны
В этом разделе представлены работы по изучению свойств альдегидов и кетонов. Простейшими представителями альдегидов являются: муравьиный альдегид (формальдегид) и уксусный альдегид (ацетальдегид), простейшим представителем кетонов – ацетон. Альдегиды встречаются в организме человека как продукты обмена веществ. Альдегиды и их производные находят широкое применение в медицинской практике (формальдегид, гексаметилентетрамин (уротропин), хлоральгидрат, цитраль, витамины В6 и А и др.).
Задача работы: изучить химические свойства альдегидов и кетонов. Познакомиться с качественными реакциями на альдегиды и ацетон.
Оборудование, материалы: раствор ацетальдегида, аммиачный раствор оксида серебра, 10%-ный раствор гидроксила натрия, 5%-ный раствор сульфата меди, раствор Люголя, пробирки, пипетки, спиртовка.
Работа 8. Восстанавливающие свойства альдегидов
а) Реакция с аммиачным раствором оксида серебра (реакция «серебряного зеркала)
Выполнение
работы:
В пробирку
наливают 0,5 мл раствора ацетальдегида
(или другого альдегида) и прибавляют 1
мл аммиачного раствора оксида серебра.
Содержимое пробирки осторожно нагревают
(не к ипятить).
Наблюдается восстановление оксида
серебра до металлического серебра,
которое, осаждаясь на стенках пробирки,
образует тончайший, блестящий налет,
напоминающий зеркало.
ипятить).
Наблюдается восстановление оксида
серебра до металлического серебра,
которое, осаждаясь на стенках пробирки,
образует тончайший, блестящий налет,
напоминающий зеркало.

б) Реакция с гидроксидом меди (II)
Выполнение работы: В пробирку наливают по 1 мл раствора ацетальдегида (или другого альдегида) и 10%-ного раствора гидроксида натрия, затем добавляют несколько капель 5% -ного раствора сульфата меди до образования голубой взвеси гидроксида меди(II). Верхнюю часть пробирки нагревают. Наблюдают появление сначала желтого осадка гидроксида меди (I), а потом красного осадка оксида меди (I).

Данные реакции отличают альдегиды от кетонов, которые не так легко окисляются в этих условиях.
Работа 9. Качественная реакция на ацетон (проба Либена)
Выполнение работы: В пробирку наливают 1 мл раствора ацетона, прибавляют несколько капель раствора Люголя и 1 мл 10%-ного раствора гидроксида натрия. Выпадает светло-желтый осадок йодоформа, имеющий специфический запах.
ацетон
ацетат натрия иодоформ
Проба Либена используется в клинических лабораториях для открытия ацетона в моче (при сахарном диабете, голодании).
