
- •Кафедра химии
- •Содержание
- •Общие правила работы в лаборатории
- •Правила техники безопасности
- •Оказание первой помощи
- •Порядок оформления работ
- •Общая химия
- •Тема 1. Растворы
- •Работа 1. Приготовление рабочего 0,1n раствора hCl
- •Плотность растворов соляной кислоты
- •Работа 2. Определение нормальности рабочего раствора hCl по 0,1n раствору NaOh
- •Работа 3. Древовидные образования
- •Работа 4. Рост искусственной «клетки» Траубе
- •Тема 2. Гетерогенные равновесия и процессы
- •Работа 5. Определение хлоридов мочи по Мору
- •Тема 3. Комплексонометрия
- •Работа 6. Определение общей жесткости воды трилонометрическим методом.
- •Тема 4. Протолитические равновесия и процессы
- •Работа 7. Приготовление буферных растворов
- •Тема 5. Электрохимия
- •Работа 10. Потенциометрический метод определения рН растворов при помощи стеклянного электрода
- •Тема 6. Поверхностные явления. Хроматография
- •Работа 11. Разделение минеральных солей на колонках с твердым адсорбентом
- •Работа 12. Радиальная распределительная хроматография
- •Тема 7. Дисперсные системы
- •Работа 13. Метод замены растворителя
- •Работа 14. Получение золя гидроксида железа (III)
- •Работа 15. Получение золя гексацианоферрата (II) меди
- •Работа 16. Изучение процесса коагуляции коллоидных растворов
- •Тема 8. Растворы вмс
- •Работа 17. Изучение процесса денатурации белка
- •Работа 18. Изучение процесса высаливания белка
- •Биоорганическая химия
- •Тема 1. Спирты, фенолы
- •Тема 2. Тиолы, амины
- •Тема 3. Альдегиды и кетоны
- •Тема 4. Карбоновые кислоты
- •Работа 16. Обнаружение фенольного гидроксила в карбоновых кислотах
- •Тема 5. Аминокислоты. Белки
- •Работа 20. Нингидриновая реакция на α-аминокислоты
- •Тема 6. Липиды
- •Тема 7. Углеводы
- •Дисахариды. Полисахариды
- •Тема 8. Нуклеиновые кислоты
- •Литература
Работа 18. Изучение процесса высаливания белка
Задача работы: изучить особенности процесса высаливания белка.
Оборудование, материалы: яичный белок, насыщенный раствор сульфата аммония, спирт, 10%-й раствор щелочи, 1%-й раствор сульфата меди, фильтры, пипетки, пробирки.
Выполнение работы:
а) Осаждение белков сульфатом аммония.
К
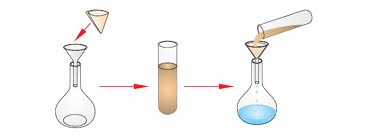 15 каплям раствора белка добавляют 15
капель насыщенного раствора сульфата
аммония и перемешивают. Получается
полунасыщенный раствор сульфата
аммония, в котором выпадает осадок
глобулинов (небольшое количество
белых хлопьев).
15 каплям раствора белка добавляют 15
капель насыщенного раствора сульфата
аммония и перемешивают. Получается
полунасыщенный раствор сульфата
аммония, в котором выпадает осадок
глобулинов (небольшое количество
белых хлопьев).Через 5 минут отфильтровывают содержимое пробирки. В фильтрате остаются альбумины.
К фильтрату добавляют тонкоизмельченный порошок сульфата аммония до полного насыщения, т.е. до тех пор, пока новая порция порошка останется нерастворенной. Выпадает осадок яичного альбумина.
А
 льбумин
отфильтровывают.
льбумин
отфильтровывают.
Проверяют фильтрат на отсутствие белка с помощью биуретовой реакции: к 1 мл исследуемого фильтрата приливают 1 мл 10% раствора гидроксида натрия и 3-5 капель 1% раствора сульфата меди и перемешивают. Фиолетовое окрашивание должно отсутствовать. Содержимое пробирки при наличии белка приобретает фиолетовый цвет в результате образования комплексного соединения.







 OOOO
OOOO
NH2-CH-C-NH-CH-C-NH-CH-C-NH-CH-C-NH- - - -CH-СООН
 | | |
| | +Cu(OH)2
| | |
| | +Cu(OH)2
R1 R2R3R4Rn

 Cu
Cu




 OOOHO
OOOHO
NH2-CH-C=N-CH–C=N-CH–C=N-CH-C-NH- - - -CH-СООН
| | | | |
R1 R2R3R4Rn
Биоорганическая химия
Рассмотрены лабораторные работы, касающиеся теоретических основ строения и реакционной способности различных классов органических соединений. Приобретенные теоретические знания, практические навыки и умения составят базу для дальнейшего изучения биохимии. Они будут востребованы также при изучении фармакологии, гигиены и других дисциплин.
Тема 1. Спирты, фенолы
В этом разделе представлены работы по изучению свойств спиртов и фенолов.
Спирты и их производные находят широкое применение в практической медицине. Так, этиловый спирт, обладая антисептическими свойствами, применяется для обеззараживания хирургических инструментов и операционного поля. Большое количество спирта идет на изготовление настоек и экстрактов из различных лекарственных трав. По фармакологическим свойствам этиловый спирт относится к наркотическим веществам. Поливиниловый спирт входит в состав антисептического средства йодинола. Этот спирт замедляет выделение йода из лекарственного средства и удлиняет взаимодействие йодинола с тканями организма. Глицерин используется в качестве основы для приготовления мазей, паст и других средств. Некоторые из спиртов являются сильными ядами. Так, употребление метилового спирта в незначительном количестве вызывает ослабление зрения или полную слепоту, а дозы более 10 мл могут оказаться смертельными, так как в организме человека превращается в формальдегид и муравьиную кислоту. Сильным токсическим эффектом обладает также этиленгликоль.
Фенолы и его гомологи используются при производстве полимеров, антиоксидантов, а также в качестве антисептиков. Так, лизол (раствор крезола в калийном мыле) используется для обеззараживания выделений, предметов и вещей, зараженных возбудителями кишечных и других инфекций. Резорцин входит в состав лекарственных средств, применяющихся при кожных заболеваниях, тимол является противоглистным средством. Производные пирокатехина — адреналин и норадреналин синтезируются в надпочечниках и обладают заметным биологическим действием: регулируют кровяное давление, уровень глюкозы в крови и др. Токсичные фенолы образуются в нашем организме и обезвреживаются в печени.
Задача работ: изучить физико-химические свойства спиртов и фенолов. Познакомиться с качественными реакциями на многоатомные спирты и фенолы.
Оборудование, материалы: 10%-й раствор щелочи, 1%-й раствор сульфата меди, глицерин, маннит, этиловый спирт, 5%-ные растворы фенола, пирокатехина, резорцина, гидрохинола, пирогаллола. 1%-ный раствор хлорида железа (III), адреналин, пипетки, пробирки.
Работа 1. Растворимость в воде спиртов и фенолов.
Выполнение работы: налейте в 4 пробирки по 1 мл воды и добавьте: в первую – 0,5 мл этилового спирта, во вторую – 0,5 мл бутилового спирта, в третью – 0,5 мл амилового спирта, в четвертую – 0,5 г фенола, все пробирки встряхните. Наблюдения и выводы запишите.
Работа 2. Взаимодействие многоатомных спиртов с гидроксидом меди (II)
В ыполнение
работы:
в
ыполнение
работы:
в три пробирки наливают по 1-2 мл 10%-ного
раствора гидроксида натрия и по несколько
капель 1%-ного раствора сульфата меди.
Во всех пробирках образуется голубой
осадок гидроксида меди (II).
К образовавшемуся осадку в первой
пробирке добавляют 0,5 мл глицерина, во
второй 0,1 г маннита и в третьей - 0,5 мл
этилового спирта. В первых двух пробирках
осадок растворяется и раствор приобретает
темно-синий цвет, что указывает на
образование растворимых в воде комплексных
соединений глицерата и манната меди;
соединения такого типа называют
«хелатными».
три пробирки наливают по 1-2 мл 10%-ного
раствора гидроксида натрия и по несколько
капель 1%-ного раствора сульфата меди.
Во всех пробирках образуется голубой
осадок гидроксида меди (II).
К образовавшемуся осадку в первой
пробирке добавляют 0,5 мл глицерина, во
второй 0,1 г маннита и в третьей - 0,5 мл
этилового спирта. В первых двух пробирках
осадок растворяется и раствор приобретает
темно-синий цвет, что указывает на
образование растворимых в воде комплексных
соединений глицерата и манната меди;
соединения такого типа называют
«хелатными».
В пробирке с этанолом растворения гидроксида меди (II) не происходит.

этиленгликоль

Затем добавьте 1 мл 20% HCI, окраска исчезает. Это качественная реакция на гликоли и полиолы.
Работа 3. Цветные реакции на фенольную группу
Выполнение работы: в пять пробирок наливают по 1 мл 5%-ного раствора фенола, пирокатехина, резорцина, гидрохинола, пирогаллола. В каждую пробирку добавляют по 2-3 капли 1%-ного раствора хлорида железа (III). Появляется окрашивание: в пробирке с фенолом - сине-фиолетовое, с пирокатехином - зеленое, с резорцином - фиолетовое, с гидрохиноном - зеленое, быстро переходящее в желтое, с пирогаллолом - буро-красное.
Одновременно с образованием фенолятов хлорид железа (III) действует как окислитель. Изменение зеленой окраски на желтую в пробирке с гидрохином обусловлено тем, что при его окислении в хинон образуется промежуточное соединение одной молекулы гидрохинона с одной молекулой хинона, так называемый хингидрон. Заметить зеленую окраску можно только в первый момент попадания капли хлорида железа (III) в раствор гидрохинона при рассмотрении на белом фоне. Окраска становится заметнее в насыщенном растворе гидрохинона и разбавленном растворе хлорида железа (III).
 OH
OH


+ FeCI3 → сине- фиолетовое окрашивание
фенол
 OH
OH


 ОН
ОН
+ FeCI3 → зеленое окрашивание
Пирокатехин
 OH
OH


+ FeCI3 → фиолетовое окрашивание
 ОН
ОН
резорцин
 OH
OH


+ FeCI3 → зеленое → желтое окрашивание

ОН
гидрохинон
OH


 ОН
ОН
+ FeCI3 → буро-красное окрашивание
 ОН
ОН
пирогаллол
Работа 4. Взаимодействие адреналина с хлоридом железа (III)
Выполнение работы: В пробирку наливают 1 мл адреналина и 2-3 капли 1%-ного раствора хлорида железа (III). Появляется зеленое окрашивание, т.к. адреналин в своей структуре содержит двухатомный фенол пирокатехин (1,2-дигидроксибензол).
