
- •Кафедра химии
- •Содержание
- •Общие правила работы в лаборатории
- •Правила техники безопасности
- •Оказание первой помощи
- •Порядок оформления работ
- •Общая химия
- •Тема 1. Растворы
- •Работа 1. Приготовление рабочего 0,1n раствора hCl
- •Плотность растворов соляной кислоты
- •Работа 2. Определение нормальности рабочего раствора hCl по 0,1n раствору NaOh
- •Работа 3. Древовидные образования
- •Работа 4. Рост искусственной «клетки» Траубе
- •Тема 2. Гетерогенные равновесия и процессы
- •Работа 5. Определение хлоридов мочи по Мору
- •Тема 3. Комплексонометрия
- •Работа 6. Определение общей жесткости воды трилонометрическим методом.
- •Тема 4. Протолитические равновесия и процессы
- •Работа 7. Приготовление буферных растворов
- •Тема 5. Электрохимия
- •Работа 10. Потенциометрический метод определения рН растворов при помощи стеклянного электрода
- •Тема 6. Поверхностные явления. Хроматография
- •Работа 11. Разделение минеральных солей на колонках с твердым адсорбентом
- •Работа 12. Радиальная распределительная хроматография
- •Тема 7. Дисперсные системы
- •Работа 13. Метод замены растворителя
- •Работа 14. Получение золя гидроксида железа (III)
- •Работа 15. Получение золя гексацианоферрата (II) меди
- •Работа 16. Изучение процесса коагуляции коллоидных растворов
- •Тема 8. Растворы вмс
- •Работа 17. Изучение процесса денатурации белка
- •Работа 18. Изучение процесса высаливания белка
- •Биоорганическая химия
- •Тема 1. Спирты, фенолы
- •Тема 2. Тиолы, амины
- •Тема 3. Альдегиды и кетоны
- •Тема 4. Карбоновые кислоты
- •Работа 16. Обнаружение фенольного гидроксила в карбоновых кислотах
- •Тема 5. Аминокислоты. Белки
- •Работа 20. Нингидриновая реакция на α-аминокислоты
- •Тема 6. Липиды
- •Тема 7. Углеводы
- •Дисахариды. Полисахариды
- •Тема 8. Нуклеиновые кислоты
- •Литература
Работа 16. Обнаружение фенольного гидроксила в карбоновых кислотах
Выполнение работы: взять две пробирки, в одну поместить несколько кристаллов салициловой кислоты, а в другую – аспирина. Прибавить для растворения 3-4 капли воды и затем 1 каплю 1%-ного раствора хлорного железа (III). При наличии свободного фенольного гидроксила в молекуле исследуемого вещества немедленно появляется темно-фиолетовое окрашивание. Напишите формулы салициловой кислоты и аспирина.
Тема 5. Аминокислоты. Белки
В этом разделе представлены работы по изучению химических свойств аминокислот и белков. Аминокислоты являются структурными компонентами пептидов и белков и очень важными метаболитами. Ряд аминокислот и их производных используется с лечебной целью (метионин, глутаминовая кислота, глицин, аминокапроновая кислота и т.д.). В организме человека из аминокислот образуется огромное число биологически важных соединений - гистамин, серотонин, холин и многие, многие другие.
Задача работ: научиться экспериментально доказывать наличие функциональных групп в аминокислотах, а также пептидной связи и индивидуальных аминокислот в белках.
Оборудование, материалы: 1 %-ный раствор яичного белка; 3 %-ный раствор сульфата меди (II); 10%-ный раствор гидроксида натрия; 10 %-ный раствор ацетата свинца (II); концентрированная уксусная кислота; концентрированная серная кислота, концентрированная азотная кислота, раствор аммиака, 2%-ный раствор цистеина, 10%-ный раствор гидроксида натрия, 10% -ный раствор ацетата свинца, пипетки, пробирки, держатель, спиртовка.
Работа 17.Биуретовая реакция Пиотровского (на пептидную связь).
Выполнение работы: в первую пробирку наливают 5 капель 1% раствора яичного белка, во вторую 5 капель 1% раствора желатина. Во все пробирки приливают 5 капель 10% раствора гидроксида натрия и по 1 капле 1% раствора сульфата меди и перемешивают. Во всех пробирках раствор приобретает устойчивую красно-фиолетовую (сине-фиолетовую) окраску.
Эта реакция является универсальной для всех белков, так как она открывает наличие не менее двух пептидных связей, с помощью которых соединяются между собой аминокислоты, входящие в белки, и формируют его первичную структуру. Раствор белка (нативного) дает сине-фиолетовое окрашивание, а продукты его гидролиза (пептиды) - красно-фиолетовый цвет.
Работа 18. Ксантопротеиновая реакция на ароматические аминокислоты
Выполнение работы: в первую пробирку наливают 5 капель 1% раствора яичного белка, во вторую – 5 капель 1% раствора желатина. Во все пробирки добавляют по 2-3 капли концентрированной азотной кислоты. Смесь осторожно нагревают для быстрого протекания реакции, так как она хорошо идет и без нагревания. В первой пробирке жидкость окрашивается в лимонно-желтый цвет, характерный для нитропроизводных. Во второй наблюдается едва заметное бледно-желтое окрашивание. После охлаждения в каждую пробирку добавляют по 10 капель концентрированного раствора аммиака или 30% раствора едкого натра. Окраска жидкости переходит в оранжевую , т.к. образуется аммонийная (или натриевая) соль динитротирозина хиноидной структуры.
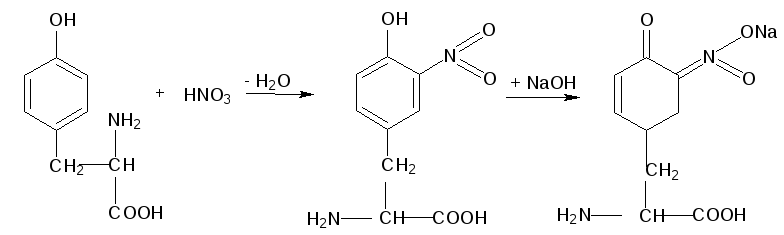
|
тирозин |
нитропроизводное тирозина желтого цвета рН < 7,0 |
хиноидное производное оранжево-желтого цвета рН > 7,0 |
Ароматические аминокислоты фенилаланин, тирозин и триптофан нитруются азотной кислотой с образованием соединений желтого цвета. Реакция положительна также с пептидами и белками, содержащими эти аминокислоты.
Работа 19. Реакция Фоля на серосодержащие аминокислоты.
 Выполнение
работы: в
первую пробирку наливают 2 мл 1% раствора
яичного белка, во вторую – 2 мл 1% раствора
желатина. В обе пробирки добавляют по
2 мл 10%
-ного раствор гидроксида натрия и
осторожно нагревают до кипения. Затем
добавляют 5 капель 10%-ного раствора
ацетата свинца
и вновь кипятят.
Выполнение
работы: в
первую пробирку наливают 2 мл 1% раствора
яичного белка, во вторую – 2 мл 1% раствора
желатина. В обе пробирки добавляют по
2 мл 10%
-ного раствор гидроксида натрия и
осторожно нагревают до кипения. Затем
добавляют 5 капель 10%-ного раствора
ацетата свинца
и вновь кипятят.
В пробирке с яичным белком появляется буровато-черное или черное окрашивание, интенсивность которого зависит от концентрации раствора белка и содержания в нем цистеина и цистина. Раствор желатина не дает окрашивания, т.к. не содержит этих аминокислот.
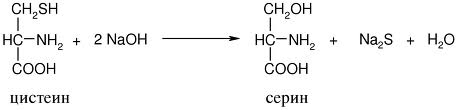
(CH3COO)2Pb + Na2S → PbS↓ + 2CH3COONa
черный осадок
К серосодержащим аминокислотам относятся: цистеин, цистин и метионин. Реакция положительна только с цистеином и цистином. Метионин этой реакции давать не будет, поскольку сера в его молекуле связана прочно.
