
- •Гетероциклические
- •Гетероциклическими соединениями
- •Ароматические
- ••Ароматические ГЦ соединения обладают всеми признаками ароматичности.
- •пятичленные
- •СПОСОБЫ ПОЛУЧЕНИЯ
- ••Фурфурол получил название от латинского слова «отруби».
- ••Пиррол – при фракционной перегонке каменноугольной смолы.
- •• 2. Лабораторные способы
- ••б) Взаимопревращения фурана, пиррола и тиофена: цикл Юрьева.
- ••г) Из бутин-1,4-диола и аммиака в присутствии катализатора
- •СТРОЕНИЕ
- ••Теория резонанса подтверждает ароматический характер фурана, пиррола и тиофена.
- ••Наблюдается отклонение от принципа аддитивности параметров связей и молекулы в этих системах –
- •Ест (кДж/моль)
- •• Все три гетероарена
- •ХИМИЧЕСКИЕ СВОЙСТВА
- •• Относительная
- ••Т.к. в α-положении δ- -заряд больше, то электрофил атакует
- •• Механизм электрофильного замещения (SЕ)
- •• 2) Пятичленные
- ••С-протонирование энергетически более выгодно, чем N-протонирование.
- •Нитрующие реагенты:
- •ульфирующие реагенты:
- •Ацетилирующие
- ••3) Основность - низкая, т.к. пара эл-ов гетероатома занимает р-орбиталь, к-рая участвует в
- •• 4) Реакции нуклеофильного
- •• 5) Склонность вступать в р-
- •• 6) Окисление - можно
- •Фуран
- •Реакции
- •HCON(CH3)2, POCl3
- •• Реакции нуклеофильного
- ••Реакции присоединения
- •• Реакции 1,4-
- ••Производные ФУРАНА
- •• Применение фурана
- ••Производные фурана довольно широко распространены в природе. Фурановые производные входят в состав многих
- ••ПИРРОЛ
- •• Кислотность и реакции
- ••Реакции присоединения
- •• Значение пиррола и его
- ••Все эти соединения содержат
- ••В порфине пиррольные остатки связаны метиновыми мостиками.
- ••Порфины, входящие в состав природных пигментов имеют заместители в пиррольных ядрах (порфирины).
- ••Гемоглобин отвечает за обеспечение тканей кислородом, хлорофилл принимает участие в трансформации солнечной энергии
- ••ТИОФЕН
- •CH3COCl / SnCl4
- •Реакции
- •Производные тиофена
• 2. Лабораторные способы
• а) из алифатических 1,4-дикарбонильных
соединений.
•При нагревании этих соединений в присутствии дегидратирующих реагентов
(Р2О5, Н2SO4 ) образуются производные
фурана,
в присутствии NH3 или аминов – производные пиррола,
фосфорных соединений серы (Р2S5, P2S3) – производные тиофена.
|
R |
R' |
P O |
|
|
|
|
|
|
2 |
5 |
|
|
|
O |
O |
to |
|
R' |
|
|
|
R |
O |
|||
|
to NH3 |
P2S5 |
|
|
||
|
|
|
|
|||
|
|
to |
|
|
|
|
R |
N |
R' |
|
|
R' |
|
|
R |
|
S |
|
||
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
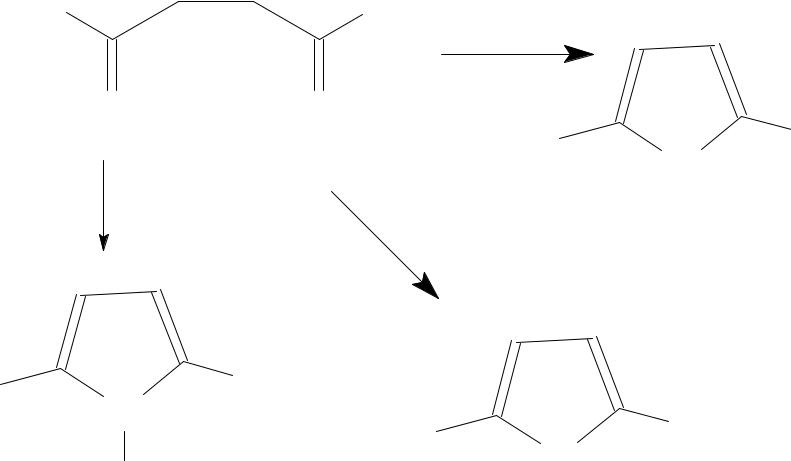
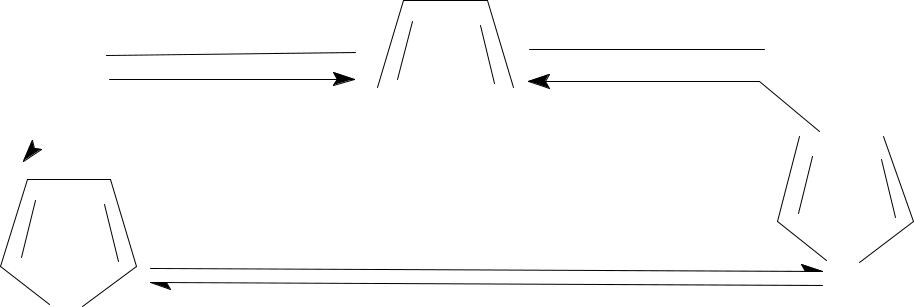
•б) Взаимопревращения фурана, пиррола и тиофена: цикл Юрьева.
• |
Превращения происходят под |
|
д-ем соответствующих реагентов |
|
при т-ре ~400oC в присутствии кат- |
|
ра Al2O3. |
•Однако эту р-цию можно рассматривать только как метод синтеза пиррола и тиофена из фурана, т.к. выход фурана низкий.
H2S/Al2O3 NH3/Al2O3
 H2O/Al2O3
H2O/Al2O3  O
O H2O/Al2O3
H2O/Al2O3
|
NH3/Al2O3 |
N |
||
S |
H2S/Al2O3 |
|||
|
|
|||
H |
||||

•г) Из бутин-1,4-диола и аммиака в присутствии катализатора
H2C C |
|
|
C |
CH2 |
NH3, 300oC |
|
|
||
|
|
|
|
||||||
|
|
|
|
|
|
|
|||
|
|
Al2O3 |
(95%) |
N |
|||||
|
|
||||||||
OH |
|
|
|
OH |
|||||
|
|
|
ThO |
(5%) |
|
|
|
||
|
|
|
|
|
|
||||
|
|
|
|
H |
|||||
|
|
|
|
|
|
||||
|
|
|
|
|
2 |
|
|
||

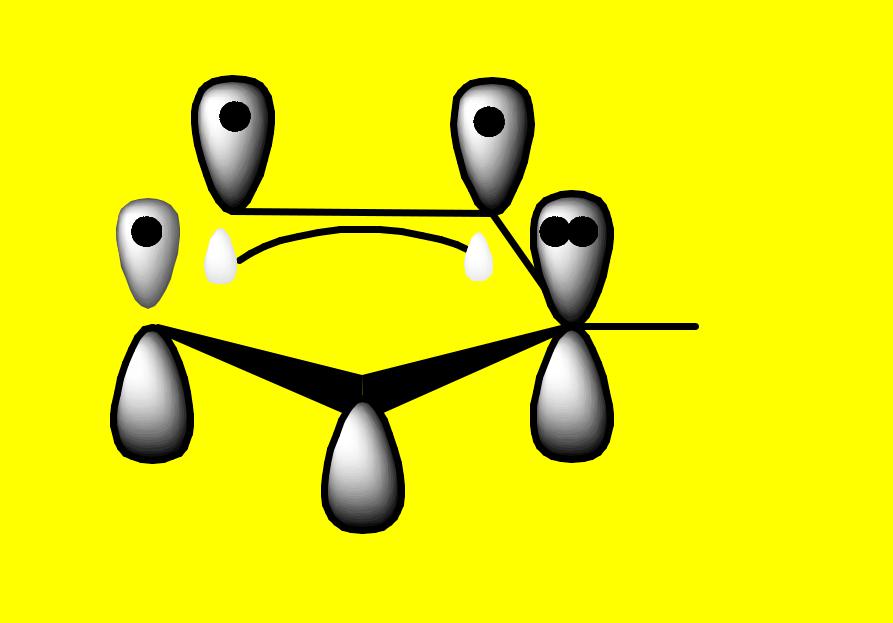
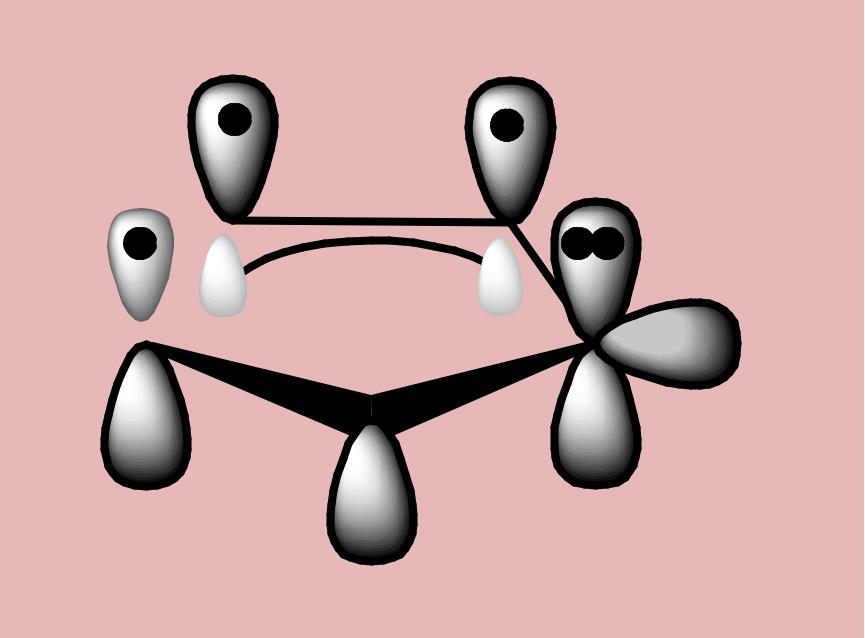
СТРОЕНИЕ
Молекулы всех этих гетероциклов
имеют плоское строение.
Ароматический секстет π-
электронов образуется за счет 4 электронов атомов С и
2-х неподеленных электронов
гетероатомов, находящихся на негибридизованных pz-орбиталях.
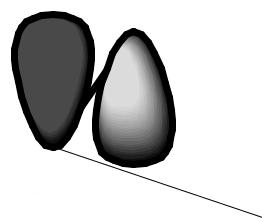





 N H
N H
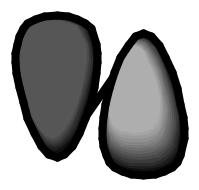






 O
O
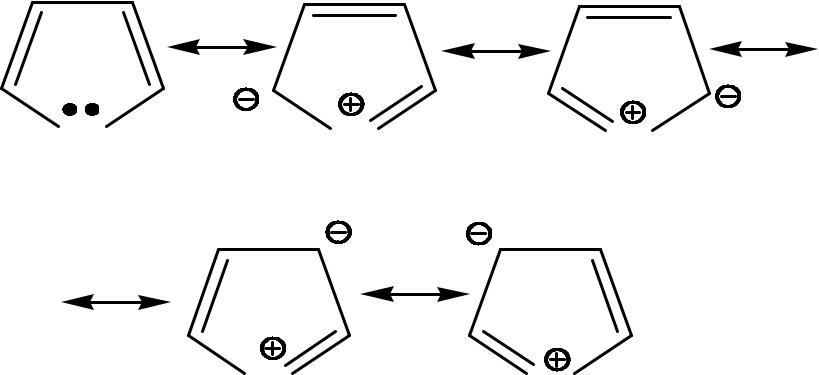
•Теория резонанса подтверждает ароматический характер фурана, пиррола и тиофена.
X |
X |
X |
а |
в |
с |
X |
X |
d |
e |
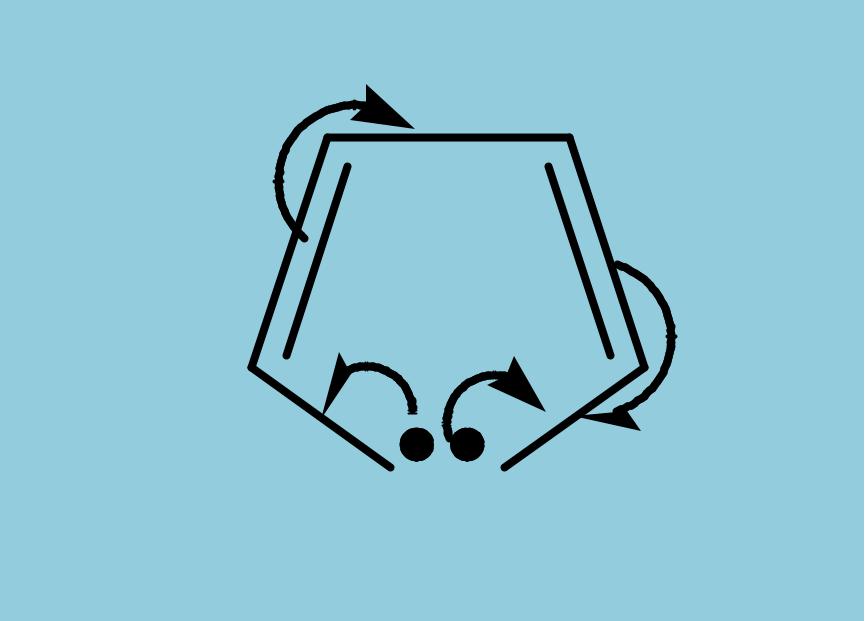
• или
X
