
3159
.pdfсовпадении двух событий: смещение рассматриваемого атома достигнет критического значения и одновременно его соседи образуют «дыру», т. е. займут положения; благоприятствующие скачку. При этом смещения соседей, даже ближайших, при образовании «дыры» значительно меньше, чем у атома, совершающего скачок, соответственно «дыра» образуется чаще, чем атом в нее смещается.
Таким образом, скачок - результат такой флуктуации
в решетке, при которой один атом приобретает большую амплитуду смещения в нужном направлении, а окружающие атомы раздвигаются и дают ему дорогу, так что он может перескочить в соседний узел, не вызывая очень большого увеличения потенциальной энергии решетки.
Никаких ограничений на время перескока этот подход не накладывает.
Что же касается критического смещения, то для большинства металлов с плотноупакованной кубической решеткой (гцк, оцк) хорошее совпадение с экспериментом получилось при величине критического смещения около 30% пути до перевальной точки.
2.5. Диффузия в твердых растворах замещения
Для большей наглядности и простоты ограничимся анализом двухкомпонентной системы A B , образующий твёрдый раствор замещения.
Если раствор на основе компонента A является бесконечно разбавленным, то при диффузии в таком растворе изотопа A* определяется коэффициент изотопной диффузииDAA* , практически не отличающийся от коэффициента
самодиффузии. При диффузии изотопа B* определяется коэффициент изотопной диффузии B в бесконечно разбавленном растворе на основе A.
81
Если раствор не является бесконечно разбавленным и концентрации компонентов соизмеримы, то и при диффузии
изотопа A* , |
и при диффузии |
изотопа |
B* |
определяются |
|
коэффициенты гетеродиффузии |
DAB* |
и |
DAB* в твёрдом |
||
растворе. |
|
A |
|
|
B |
|
|
|
|
|
|
Можно |
сформулировать |
три |
общих |
эмпирических |
|
правила, описывающих разницу между коэффициентом гетеродиффузии примеси и коэффициентом самодиффузии растворителя в бесконечно разбавленном растворе:
-DBA* и DAA* отличаются не более чем на порядок;
-предэкспоненциальные факторы также отличаются не более чем на порядок;
-энергии активации различаются не более чем на 15%. Причины этого различия заключаются в следующем. В
кристаллах с гцк решеткой коэффициент гетеродиффузии примеси можно записать в виде
A |
a2 |
|
|
|||
D |
* |
|
p 2 f |
2 , |
(2.48) |
|
12 |
||||||
B |
|
|
|
|
||
где a — период решетки; p — вероятность обнаружить вакансию среди ближайших соседей атома примеси; 2 — частота обмена местами между вакансией и атомом примеси; f2 - фактор корреляции, равный в соответствии с уравнением (2.16) и схемой скачка, представленной на рис. 2.6.
f |
2 |
|
|
1 3,5 3 |
|
, |
||
|
|
|
||||||
|
|
|
2 |
3,5 |
3 |
|
||
|
|
1 |
|
|
|
|||
где 1 -частота обмена вакансии с атомом растворителя - соседом атома примеси (вакансия была до скачка и остается после скачка соседом атома примеси), 3 - частота обмена
вакансии с атомом растворителя ( в результате вакансия уходит от атома примеси, диссоциативный скачок)
82

Таким образом, при рассмотрении гетеродиффузии примеси необходимо вводить в рассмотрение как минимум три сорта скачков вакансии, а если учитывать также частоту ассоциативных скачков (см. рис. 2.6), то более точное выражение для f2 имеет вид
f |
2 |
|
|
1 2,576 3 |
. |
|||
|
|
|
|
2 |
2,576 |
3 |
|
|
|
|
1 |
|
|
|
|||
В гцк решётке чистого растворителя вероятность обнаружить вакансию на 12 местах вокруг произвольного атома A
p0 12N ,
где N - равновесная атомная доля вакансий, равная
exp S f 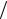 k exp H f
k exp H f  kT .
kT .
Вблизи атома примеси эта вероятность изменяется, поскольку между вакансией и атомом примеси существует взаимодействие.
В соответствии со сказанным для комплекса вакансия - атом примеси можно написать, что
p p0 exp G p kT |
|
kT . |
(2.49) |
|||
12N |
|
exp S |
k exp H |
p |
||
|
p |
|
|
|
||
Здесь S p - изменение энтропии, связанное с образованием пары, H p 0 - разница между энтальпией
образования вакансии вдали и вблизи от атома примеси. Эта величина, приблизительно совпадает с энергией взаимодействия между вакансией и атомам примеси
( H p ).
Частота скачков вакансии в решётке чистого растворителя
0 exp Sm 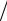 k exp Hm
k exp Hm  kT .
kT .
83

Естественно предположить, что вблизи атома примеси она изменяется, тогда
|
|
|
|
m |
Smp |
|
|
|
m |
Hmp |
|
|
|
|
|
exp |
S |
exp |
|
H |
|
, (2.50) |
|||||
2 |
|
|
|
|
|||||||||
|
|
|
|
k |
|
|
|
|
|
kT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
где Smp |
и Hmp |
- |
изменение энтропии и энтальпии |
||||||||||
перемещения вакансии, когда она обменивается местами не с атомом растворителя, а с атомом примеси.
Подставляя уравнения (2.49) и (2.50) в (2.48), получим
|
|
|
|
|
|
|
|
|
f |
|
m |
S p Smp |
|
|
|
|
||||
DA* a2 |
f exp |
S |
S |
|
|
|
||||||||||||||
|
|
|
|
|
|
|||||||||||||||
B |
|
|
|
2 |
|
|
|
|
|
|
|
k |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
f |
|
|
m |
|
|
|
|
|
|
. |
|
(2.51) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
H |
|
H |
H p Hmp |
|
|
|
|||||||||||||
exp |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
kT |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Сравним это выражение с коэффициент самодиффузии |
||||||||||||||||||||
A |
2 |
|
|
|
|
|
|
|
f |
|
m |
|
|
|
|
f |
m |
|
||
|
|
|
|
|
|
S |
S |
|
|
|
H H |
|
(2.52) |
|||||||
DA* a |
|
f0 |
exp |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
k |
|
exp |
|
|
kT |
|
. |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Следовательно, |
|
|
изменение |
|
предэкспоненциального |
|||||||||||||||
фактора определяется отношением |
f2 |
f0 |
и величинами S p и |
|||||||||||||||||
Smp . Естественно предположить, что они малы, поскольку малы S f и Sm . Отношение f2  f0 может сильно отличаться
f0 может сильно отличаться
от единицы в случае сильной связи между вакансией и атомом примеси. В табл. 2.3 приведены факторы корреляции для гетеродиффузии различных примесей в серебре и отношение f2  f0 .
f0 .
Изменение энергии активации, как это следует из сравнения уравнений (2.49) и (2.50), составит:
84

|
|
E EA* |
EA* |
H |
p |
H |
mp |
kT2 |
ln f2 |
. |
(2.53) |
|||||||||||
|
|
|||||||||||||||||||||
|
|
|
|
|
B |
A |
|
|
|
|
|
T |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 2.3 |
||||||
Факторы корреляции для гетеродиффузии примесей в серебре |
|
|||||||||||||||||||||
Примесь |
|
|
f2 |
|
f2 |
f0 |
|
Примесь |
f2 |
|
|
|
f2 |
f0 |
|
|||||||
Палладий |
|
|
0,96 |
|
1,23 |
|
|
Таллий |
|
0,50 |
|
|
|
0,64 |
|
|
||||||
Медь |
|
|
0,86 |
|
1,10 |
|
|
Германий |
0,39 |
|
|
|
0,50 |
|
|
|||||||
Кадмий |
|
|
0,52 |
|
0,67 |
|
|
Свинец |
|
0,65 |
|
|
|
0,83 |
|
|
||||||
Индий |
|
|
0,43 |
|
0,55 |
|
|
Сурьма |
|
0,64 |
|
|
|
0,82 |
|
|
||||||
В случае |
сильной |
связи |
|
между |
вакансией |
и |
атомом |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
A |
|
|
a2 |
|
|
||
примеси |
( |
|
) |
коэффициент |
диффузии |
D |
* |
|
|
p f |
|
|||||||||||
|
12 |
|
||||||||||||||||||||
|
|
|
2 |
|
1 |
|
|
|
|
|
|
|
|
|
B |
|
|
|
|
1 |
2 |
|
Очевидно, в этом случае энергия активации диффузии есть сумма энергии образования вакансии вблизи атома примеси и энергии перемещения, характерной для чистого растворителя. В величину E не войдет слагаемое Hmp .
|
|
В |
случае |
слабой связи ( 1 2 ) фактор |
f2 |
1 и |
||||
A |
|
a2 |
|
|
|
|
|
|
|
|
D |
* |
|
p . |
В |
энергию |
активации |
войдет |
энергия |
||
|
||||||||||
B |
|
12 |
1 |
|
|
|
|
|
|
|
перемещения, характерная для примесного атома. |
|
|
||||||||
|
|
Теоретическая |
оценка |
величин H p |
и Hm p |
была |
||||
сделана Дж. Лазарусом для одновалентных растворителей для случая температурной независимости фактора корреляции. Он предположил, что атом примеси вносит в решётку избыточный заряд Ze (Z - разница валентностей примеси и одновалентного растворителя). Экранированный потенциал этого заряда можно записать как
V r |
Ze |
|
|
r |
|
|
|
exp |
|
|
, |
(2.54) |
|
|
|
|||||
|
r |
|
|
|
|
|
|
|
|
|
|
||
85

где r - расстояние от заряда, находящегося в точке r 0;
|
- радиус экранирования, |
равный h2 16 2 |
me2 3ne 13 ; |
h |
- постоянная Планка; ne |
— число электронов в единице |
|
объема; m и e — масса и заряд электрона. |
|
||
|
Между вакансией, имеющей заряд -1, и примесным |
||
атомом, находящимся на расстоянии a от |
неё, возникает |
||
взаимодействие, и энергия образования вакансии уменьшается на величину
|
|
eV a |
Ze2 |
|
|
a |
|
|
H |
p |
|
exp |
|
|
. |
(2.55) |
|
|
|
|||||||
|
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Энергия образования вакансии уменьшается, если |
Z 0 |
|||||||
(примесь находится справа от растворителя в периодической системе элементов), и наоборот.
Аналогичным образом Лазарус оценил и Hm p .
Эксперимент действительно показывает, что энергия
активации гетеродиффузии |
EA* меньше энергии активации |
|
B |
самодиффузии EA* , если |
Z 0 . Теория предсказывает |
A |
|
линейную зависимость EBA* от Z . Это подтверждается опытом для одновалентных растворителей Cu , Ag , Au (рис. 2.10).
Общее правило, сформулированное Лазарусом,
заключается в том, что при добавлении в раствор «быстрой» примеси (т. е. такой, что DBA* DAA* ) оба коэффициента
растут, причем коэффициент самодиффузии растворителя (DAA* ) растет быстрее, чем гетеродиффузии примеси (DBA* ).
Однако это правило не всегда выполняется.
Очень часто наблюдают линейную зависимость коэффициента самодиффузии растворителя от концентрации примеси:
DA* N |
B |
DA* 0 1 bN |
B |
. |
(2.56) |
A |
A |
|
|
86

Рис. 2.10. Зависимость энергии активации (E ) диффузии примесей в серебре (1) и меди (2) от разницы валентностей
( Z )
Это выражение можно получить теоретически в приближении слабых возмущений, когда малая доля вакансий связана с атомами примеси, пользуясь соответствующим выражением для фактора корреляции. При этом
|
4 f |
0 |
|
|
DA* |
|
|
|
b 18 |
|
|
|
B |
|
. |
(2.57) |
|
1 f |
|
DA* |
||||||
|
2 |
|
|
|
|
|||
|
|
|
|
A |
NB 0 |
|
|
|
Поскольку для металлов с гцк решеткой f0 =0,78, можно,
измерив b , найти f2 . Существует эмпирическая корреляция между влиянием примеси на самодиффузию растворителя и температуру его плавления:
DAA* NB |
K1 exp |
|
K T N |
B |
|
|
|
||
|
2 |
пл |
|
|
, |
(2.58) |
|||
|
T |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
87 |
|
|
|
|
|
|
|
|
где K1 и K2 - константы.
Витоге на основании вышеприведенных рассуждений следует, что в плотноупакованных решетках (гцк и гпу) преобладает вакансионный механизм диффузии.
Вметаллах с более открытой решеткой, в частности с оцк решеткой наиболее вероятным представляется вакансионный механизм, однако, нельзя исключить ни прямой межузельный, ни межузельный механизм вытеснения. Некоторые исследователи считают возможным даже обменный механизм.
Наконец, следует упомянуть еще о двух «аномальных» эффектах, имеющих отношение к механизмам диффузии. Для обоих не дано общепринятого теоретического объяснения.
Было обнаружено, что коэффициент диффузии меди в
германии очень велик (D 4 10 5 см2/с) и слабо зависит от температуры в интервале 700—900°С. Это видимо связано с тем, что значительная доля атомов примеси находится в междоузлиях. Поскольку коэффициент межузельной диффузии примеси гораздо больше вакансионного, то именно диффузия по междоузлиям определяет экспериментальное значение D. В дальнейшем такой же эффект был обнаружен для железа в германии и кремнии.
Позднее было показано, что диффузия примесей в элементах с решеткой типа алмаза (Ge, Si ) - не единственный пример «сверхбыстрой» диффузии в твердом состоянии. Благородные примеси (медь, серебро, золото) диффундируют частично по межузельному механизму в многовалентных растворителях III и IV групп периодической системы, таких как свинец (гцк), олово (тетрагональная), индий (тетрагональная), таллий (гцк). Эффект был обнаружен также для меди в празеодиме как в -состоянии (ГПУ), так и - состоянии (оцк).
Коэффициент диффузии примесей, по крайней мере, на три порядка превышает коэффициент самодиффузии, а для меди в олове при 25°С это отношение доходит до 2 109 (в направлении оси a) и 1012 (параллельно оси c). Заметим, что
88
радиус атомов золота и серебра составляет около 80% от атомного радиуса свинца и еще большую долю от радиусов олова, индия и таллия, тем не менее, всю совокупность опытных данных удалось объяснить, только приняв предположение о межузельном механизме.
Если бы действовал вакансионный механизм, потребовалось бы огромное увеличение частоты скачков иона растворителя в присутствии примеси. Однако добавление к свинцу 0,02% Cu или серебра практически не меняло его подвижности.
Было предложено качественное объяснение, почему благородные металлы могут занимать междоузлия в многовалентных растворителях. Обычно этому препятствует сильное ион - ионное отталкивание. Однако ионные радиусы индия, олова, свинца и таллия относительно малы, а междоузлия сравнительно велики, так что перекрытие практически отсутствует. Кроме того, кулоновское отталкивание ионов сильно экранируется большим числом валентных электронов растворителя.
Вместе с тем между d -электронами примеси и растворителя возникает сильное корреляционное взаимодействие. Этому благоприятствует изоэлектронность ионных остовов, а также равенство ион - ионного расстояния с тем, которое есть в примесном металле. Оба условия лучше выполняются для междоузлий и хуже для узлов. Расстояние между последними слишком велико для возникновения эффективной d -d связи.
Несмотря на непротиворечивость предложенного объяснения, никаких расчетов сделано не было. Стоит отметить, что во всех упомянутых случаях общее содержание примесей не превышало 0,1%. Из теоретического анализа не следует, что это условие является обязательным.
Вторая диффузионная «аномалия» относится к некоторым металлам с оцк решеткой: наиболее ярко она представлена у -титана, -циркония и -урана. Для этих
89
металлов в широком интервале над температурой превращения не выполняется линейная зависимость логарифма коэффициента диффузии от обратной температуры. Энергия активации и предэкспоненциальный фактор относительно низки: первая составляет около 60% от 18kTпл , a
D0 10 3 см2/с. Наконец, некоторые примеси диффундируют в них на два порядка быстрее, чем атомы растворителя при самодиффузии (Ti и U ).
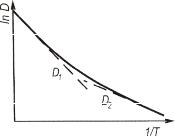
Коэффициент диффузии в этих металлах можно представить в виде суммы двух коэффициентов (рис. 2.11).
Рис. 2.11. Зависимость коэффициента диффузии от температуры в аномальных металлах с оцк решёткой
Первый высокотемпературный коэффициент D1 подчиняется правилам вакансионной диффузии и характеризует свойства данного металла; это истинный коэффициент диффузии. Второй, низкотемпературный коэффициентD2 , очень чувствительный к условиям проведения диффузионного опыта. Можно отметить, что все эти металлы претерпевают при нагреве фазовый переход (г.п.у.) - (оцк). Поэтому получила широкое распространение точка зрения, что D2 соответствует диффузии по дефектам, например дислокациям, возникающим при полиморфном превращении.
90
