
Поверхностно-активные вещества в золь-гель технологии
..pdf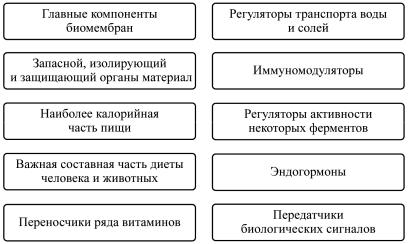
Рис. 12. Основные биологические функции липидов
В последние годы наблюдается тенденция к использованию «зеленых» ПАВ, особенно в быту. Термин «природное ПАВ» служит указанием на природный источник вещества. При этом ни одно ПАВ, используемое сегодня в значительных объемах, нельзя считать природным в полном смысле. Например, моноглицериды широко распространены в природе, но ПАВ, поступающие на рынок как моноглицериды, получают в процессе промышленного гидролиза триглицеридных масел при температурах выше 200 °С, что и приводит к образованию побочных продуктов. Алкилглюкозиды чрезвычайно часто встречаются в живых организмах, но ПАВ этого класса, часто называемые АПГ, получают с помощью многостадийных химических процессов, и их нельзя считать природными.
Синтетические ПАВ в зависимости от сырья, из которого их получают, подразделяют на олеохимические и нефтехимические ПАВ. Олеохимические ПАВ производят из возобновляемого сырья, обычно из растительных масел. Нефтехимические ПАВ производятся из небольших «строительных блоков», таких
21
как этилен, получаемый при крекинге нефти. Часто сырьем для ПАВ одновременно служат растительные масла и продукты нефтехимии. Производство ПАВ с использованием в качестве сырья растительных масел не всегда обеспечивает получение менее токсичных и менее экологически вредных ПАВ, чем нефтехимические производства. Однако с учетом круговорота углекислого газа химическое производство, основанное на возобновляемом сырье, всегда более предпочтительно.
Важным аспектом применения синтетических ПАВ является их биоразлагаемость. Попадая в водоемы, ПАВ способны нанести природе существенный ущерб, изменяя поверхностное натяжение и тем самым оказывая отрицательное влияние на жизнедеятельность растений и живых организмов. В качестве основных рассматривают три фактора:
1)биоразлагаемость (способность к деструкции в природных условиях);
2)биоаккумулирование (способность накапливаться в растениях и живых организмах);
3)токсичность в водной среде.
К дополнительным факторам биотоксичности ПАВ относятся анаэробная биоразлагаемость, продолжительность токсического эффекта, влияние на работу очистных сооружений предприятий, токсичность производства, влияние на жизненные циклы, биотоксичность на единицу эффективности.
Контрольные вопросы к главе 1
1.Какие вещества называют поверхностно-активными?
2.Что такое адсорбция?
3.Является ли поверхностная активность индивидуальным свойством вещества?
4.Охарактеризуйте молекулы, имеющие дифильную структуру.
22
5.Чем обусловлено появление избыточной энергии на границе раздела двух фаз?
6.Как называется основная термодинамическая характеристика поверхности раздела между разными фазами в дисперсной системе?
7.Какие факторы определяют величину поверхностного натяжения?
8.Как классифицируют ПАВ по растворимости?
9.На какие группы разделяют ПАВ по диссоциации в воде?
10.На какие группы разделяют ПАВ по физико-химичес- ким механизмам воздействия?
11.Какие соединения называют липидами?
12.Назовите основные биологические функции липидов.
13.Из какого сырья получают синтетические ПАВ?
14.Какие факторы рассматривают при определении биотоксичности ПАВ?
15.Чем опасно биоаккумулирование ПАВ?
23
Глава 2. Мицеллообразование в растворах ПАВ
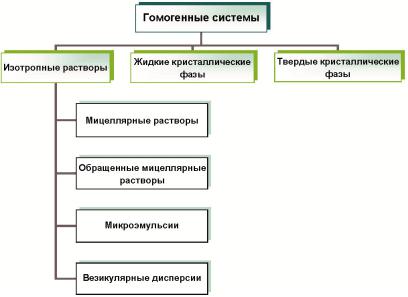
Системы, содержащие поверхностно-активные вещества, подразделяют на гомогенные (рис. 13) и гетерогенные. И те и другие представляют существенный интерес для материаловедов
испециалистов, разрабатывающихновыетехническиерешения.
Кгомогенным системам, содержащим ПАВ, относятся изотропные растворы, жидкие кристаллические фазы и твердые кристаллические фазы. Для твердых кристаллических фаз характерен как дальний, так и ближний порядок. В жидких кристаллических фазах (мезофазах) нет ближнего порядка, но есть определенный порядок на больших расстояниях. Изотропные растворы характеризуютсяотсутствиемпорядканаближнихидальнихрасстояниях.
Рис. 13. ГомогенныесистемыПАВ
24
По структуре жидкие кристаллы представляют собой жидкости, похожие на желе, состоящие из молекул, определенным образом упорядоченных во всем объеме этой жидкости. По форме молекулы, образующие жидкие кристаллы, могут быть либо вытянутые и стержнеобразные, либо плоские и круглые (дискообразные). Сильная анизотропия подобных молекул приводит к их упорядочиванию за счет межмолекулярных взаимодействий и высокой вязкости жидкой фазы. При этом незначительные возмущения способны привести к изменению ориентации упорядоченных областей друг относительно друга.
Жидкие кристаллы подразделяют на две большие группы: термотропные и лиотропные. Термотропные жидкие кристаллы образуются в результате нагревания твердого вещества и существуют в определенном интервале температур и давлений. Лиотропные жидкие кристаллы представляют собой двухкомпонентные (или более) системы, образующиеся в смесях стержневидных молекул данного вещества и воды (или других полярных растворителей). Эти стержневидные молекулы имеют на одном конце полярную группу, а большая часть стержня представляет собой гибкую гидрофобную углеводородную цепь, т.е. лиотропные жидкокристаллическиефазыобразуютсявсистемах, содержащихПАВ.
Лиотропные жидкие кристаллы образуют только ПАВ с высокой способностью к мицеллообразованию – самоорганизации молекул ПАВ. При низких концентрациях дифильных ПАВ образуются истинные (молекулярные) растворы. При увеличении концентрации до некоторого порогового значения, называемого
критической концентрацией мицеллообразования (ККМ), в
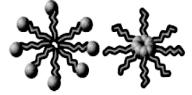
растворе возникают мицеллы – термодинамически устойчивые молекулярные агрегаты характерной сферической формы
(рис. 14).
Рис. 14. Схематический вид сферической мицеллы
в полярной и неполярной средах
25
ККМ – минимальная концентрация растворенного ПАВ, при которой можно экспериментально обнаружить коллоиднодисперсную фазу (наличие сферических агрегатов).
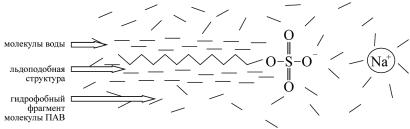
Движущей силой мицеллообразования в воде является гидрофобное взаимодействие, в результате проявления которого системе энергетически не выгодно наличие индивидуальных молекул или ионов ПАВ в растворе (рис. 15). Молекулы воды около гидрофобного фрагмента молекулы ПАВ образуют напряженную «льдоподобную» структуру. Стремление молекул воды вернуться в исходное состояние, характерное для молекул, не контактирующих с гидрофобным фрагментом ПАВ, и есть та сила, которая выталкивает молекулы ПАВ на поверхность раздела фаз или приводит к их самоорганизации (мицеллообразованию).
Рис. 15. Гидрофобный фрагмент анионного ПАВ н-додецилсульфата натрия в воде
К проявлению гидрофобных эффектов в водных растворах относятся:
1)выталкивание гидрофобных фрагментов ПАВ;
2)образование мицелл;
3)ассоциация углеводородных цепей и белков;
4)сильная адгезия гидрофобных поверхностей друг к другу;
5)несмачивание;
6)быстрая коагуляция гидрофобных частиц в воде;
7)прикрепление гидрофобных частиц к пузырькам воздуха.
26
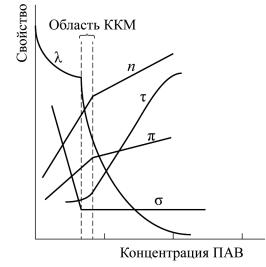
При достижении критической концентрации мицеллобразования (переходе истинного раствора в коллоидный) наблюдается изменение различных свойств растворов ПАВ (рис. 16). Наличие резкого перелома на кривых зависимостей изменения свойств при увеличении концентрации ПАВ позволяет достаточно легко определять ККМ различными способами, которых известно свыше 70. Наиболее распространены способы определения ККМ по измерению поверхностного натяжения.
Рис. 16. Зависимость свойств растворов ПАВ от их концентрации: λ – молярная электрическая проводимость; n – показатель преломления света; τ – мутность; π – осмотическое давление; σ – поверхностное натяжение
Существенное влияние на величину ККМ оказывает строение молекулы ПАВ:
1. ККМ сильно снижается при увеличении длины алкильной цепи ПАВ (в 2–3 раза на 1 метиленовую группу).
27
2.ККМ неионных ПАВ существенно ниже, чем ионных (приблизительно на 2 порядка).
3.Влияние природы полярных групп минимально, но ККМ анионных групп всегда меньше, чем катионных.
4.Величина ККМ сильно зависит от природы противоиона. Простые однозарядные неорганические противоионы не влияют на ККМ. Двухзарядные противоионы снижают ККМ примерно в 4 раза.
5.При наличии разветвленных алкильных цепей, двойных связей, ароматических групп или любом другом увеличении полярности гидрофобной части молекул ККМ снижается.
Растворенные вещества оказывают существенное влияние на величину ККМ. При введении инертного электролита в раствор одновалентного ПАВ в соотношении 1:1 происходит:
1) сильное снижение ККМ (на порядок);
2) эффект снижения зависит от длины углеводородной цепи ПАВ (у длинноцепочечных много сильнее);
3) при высоких концентрациях соли изменение ККМ с ростом числа атомов углерода в цепи проявляется сильнее, чем в отсутствие электролита;
4) влияние солей может быть описано с помощью простой модели электростатических взаимодействий (уравнение Пуас- сона–Больцмана);
5) ККМ сильно зависит от заряда ионов соли; 6) простые соли оказывают слабое влияние на ККМ не-
ионогенных ПАВ.
Формирование мицелл с единственной критической концентрацией мицеллообразования характерно лишь для некоторых «модельных» разбавленных растворов с небольшими по размерам и простыми по структуре дифильными молекулами. Многие же макромолекулы, содержащие атомные группы различной химической природы, способны самоорганизовываться
вразнообразные сложные трехмерные ансамбли (фазы). Область концентраций, в которой происходит превращение сфери-
28
ческих мицелл в анизометрические цилиндрические мицеллы,
называют второй критической концентрацией мицеллообра-
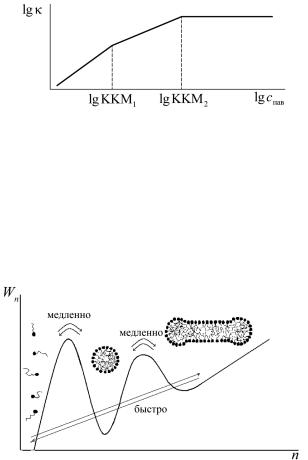
зования и обозначают как ККМ2, подразумевая, что «обычная» ККМ есть ККМ1. На зависимости ряда свойств растворов ПАВ (например, электрической проводимости) от концентрации ПАВ имеется второй изгиб (рис. 17). Для олеата натрия: ККМ1 = = 0,001 моль/л, а ККМ2 = 0,2 моль/л.
Рис. 17. Зависимость логарифма удельной электрической проводимости растворов ионогенного ПАВ от логарифма концентрации ПАВ
На рис. 18 представлена зависимость выраженной в тепловых единицах работы образования агрегата из молекул ПАВ (Wn) от концентрации ПАВ. Стрелками показаны переходы, соответствующие быстрым и медленным процессам в растворе ПАВ.
Рис. 18. Процесс образования сферических и цилиндрических мицелл
29

Цилиндрические мицеллы кооперируются в ламеллярные (слоистые) структуры или гексагональные упаковки. На рис. 19 показаны структуры, образующиеся при повышении концентрации раствораиуглублениипроцессасамоорганизациимолекулПАВ.
а б в
Рис. 19. Некоторые типы структур, образованных амфифильными молекулами в водных растворах: а – цилиндрическая мицелла;
б– гексагональная упаковка цилиндрических мицелл;
в– ламеллярный смектический жидкий кристалл
После стадии превращения сферических мицелл в цилиндрические и ламеллярные (слоистые, пластинчатые) рост концен-
|
трации коллоидных ПАВ в воде |
||
|
приводит к образованию сплош- |
||
|
ных гелеобразных систем, харак- |
||
|
теризующихся наличием биконти- |
||
|
нуальных |
структур. |
В таких |
|
структурах молекулы ПАВ объ- |
||
|
единены в единую сеть, находя- |
||
|
щуюся в растворителе (воде). |
||
|
Биконтинуальные структуры |
||
|
чрезвычайно |
разнообразны по |
|
|
своему строению. Один из про- |
||
Рис. 20. Биконтинуальная |
стейших вариантов организации |
||
структура из разветвленных |
цилиндрических мицелл |
пред- |
|
цилиндрических мицел |
ставлен на рис. 20. |
|
|
30
