
- •2 Фаза – конъюгация
- •Этилморфин
- •Изолирование:
- •Обнаружение:
- •1. Морфин:
- •2. Героин (субстанция):
- •Анализ на наличие меконовой к-ты и меконина:
- •Изолирование
- •Обнаружение
- •Метаболизм
- •Обнаружение:
- •Стрихнин
- •Вопрос 75 Производные пурина (кофеин). Химикотоксикологическая характеристика, физикохимические свойства, метаболизм. Особенности изолирования и химико-токсикологического анализа.
- •1. Химические методы:
- •2. Инструментальные методы:
- •Вопрос 76 Синтетический аналог морфина - промедол. Химико-токсикологическая характеристика, физико-химические свойства, метаболизм. Особенности изолирования и химикотоксикологического анализа.
- •1. Химический метод:
- •2. Инструментальные методы:
Изолирование
Объекты исследования:
Трупный материал: содержимое желудка, печень, головной мозг, кровь, моча, волосы, ногти
При отравлении: рвотные массы, кровь, моча, промывные воды
Методы изолирования: общими методами, и частным – Крамаренко
Обнаружение
Цветные реакции:
Исследуемое вещество |
Окраска, возникающая при добавлении реактива |
|||
Манделина |
Марки |
Фреде |
Эрдмана |
|
Папаверин |
сине-фиолетовая |
розовая → фиолетовая |
зеленая |
красная |
Микрокристаллические реакции (подтверждающая):
Сухой остаток + HCl и каплю реактива → образуются кристаллы характ.форм.
Реактивы: HgCl2, CdCl2, NaCN, соль Рейнеке, пикролоновая к-та
Вопрос 74
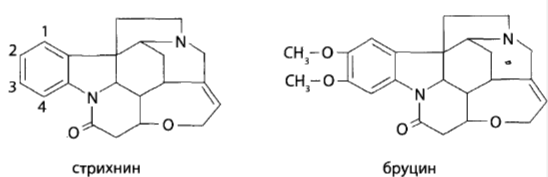
Алкалоиды; производные индола (стрихнин, бруцин). Химико-токсикологическая характеристика, физико-химические свойства, метаболизм. Особенности изолирования и химико-токсикологического анализа.
Стрихнин как стимулятор ЦНС относится к числу допинговых средств - веществ, способных улучшить спортивные показатели, работоспособность, силу мышц. Также используется как средство против грызунов (отравление при случайно употреблении)
Отравление развивается быстро. Вначале больной ощущает онемение шейной и лицевой мускулатуры. Затем появляются мышечные подергивания, а через короткое время – типичные спинномозговые судороги. Тело отравленного изгибается дугообразно и касается кровати только теменем и пятками. Жевательные и лицевые мышцы сокращены, и лицо выражает неестественную улыбку. Больной не дышит, так как сокращена диафрагма и межреберная мускулатура. Судороги при полном сознании длятся 1-2 мин, при более продолжительных судорогах больной теряет сознание. Затем наступает расслабление мускулатуры. Следующий приступ судорог наступает через 8-15 мин и может закончиться параличом дыхательного центра
Бруцин имеет токсикологическое значение при отравлении семенами чилибухи
или препаратами из них
Метаболизм
I фаза – окисление
II фаза – образование глюкоуронида
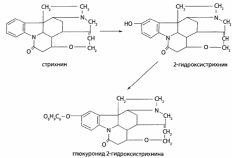
Объекты анализа: отравление, трупный материал (как обычно)
Изолирование: экстрагируются органическими р-лями как из кислых, так из щелочных р-ров общими методами. Из щелочных в большом количестве
Обнаружение:
Общие:
1. ТСХ-скриннинг: на пластинках фиксируется реактивом Драгендорфа в виде оранжевого пятна
2. Общеалкалоидные реакции с реактивами (см. табл. в предыдущем вопросе)
Частные:
Стрихнин
1. Реакция окисления K2Cr2O7 в среде конц. H2SO4 → появление быстро исчезающих сине-фиолетовых струек.
2. Реакция нитрования с конц. HNO3 → оранжевое окрашивание
(р. Витали-Морена: если добавить спирт. р-р KOH → красно-фиолет. окраш-е)
3. С реактивом Манделина: сине-фиолетовое окраш-е, переходящее в пурпурное
4. Микрокристаллоскопические реакции: обр-ся кристаллические осадки с реактивами: соль Рейнеке, платинохлороводородая к-та, пикриновая к-та, NaNO2, KOH, хлорпалладиевая к-та, пикролоновая к-та
ТСХ: Извлечение из объекта наносят на пластинку со слоем силикагеля КСК и одновременно наносят «стандарт» - раствор стрихнина. Пластинку помещают в систему растворителей хлороформ - диэтиламин (9:1). Для обнаружения места расположения на пластинке пятен стрихнина ее обрабатывают реактивом Драгендорфа → пятна оранжевого цвета.
Фармакологическая проба. Очищенный остаток извлечения из объекта наносят на спинку лягушки. Наблюдают появление характерных судорог.
УФ-спектрофотометрия. Остаток после испарения органического экстракта из объекта, очистки его с помощью хроматографии в тонком слое сорбента растворяют в С2Н5ОН или р-ре H2SO4. В полученных растворах регистрируют спектр поглощения в области длин волн.
ИК-спектроскопия. Сухой остаток после испарения органического растворителя и очистки растирают с KBr, прессуют и регистрируют ИК-спектр.
Бруцин
1. Реакция с реактивами, содержащими конц. H2SO4 или конц. HNO3.
Реактив Манделина → красное окрашивание → желтое окрашивание
Реактив Фреде → красное окрашивание → желтое окрашивание
Реактив Эрдмана → красное окрашивание → желтое окрашивание
NB! Отличие от стрихнина: стрихнин НЕ образует окрашивания с реактивом Эрдмана и с HNO3
3. Реакция с конц. HNO3: → красное окрашивание → желтое окрашивание
4. Реакция с SnCl2 → желтая окраска → фиолетовая окраска
NB! Отличие от стрихнина: Стрихнин НЕ дает окраски при проведении
этой реакции.
5. Микрокристаплоскопические реакции. Образуются кристаллические осадки с реактивами: пикролоновая к-та, стифниновая к-та, нитраниловая к-та
ТСХ, ВЭЖХ, УФ-спектрофотометрия, ИК-спектроскопия – аналогичны.
Количественное определение:
Колориметрия. Метод основан на восстановлении в-в водородом в момент выделения. При добавлении окислителя (NaNO2) образуется:
Красное окрашивание – стрихнин
Желто-зеленое – бруцин
Сухой остаток + вода очищенная + р-р HCl + Zn. Смесь нагревают до кипения и охлаждают. После раствор отделяют от цинковой пыли декантацией. После добавляют р-р 0,1% NaNO2 – характ. окрашивание.
Определяют оптическую плотность с помощью фотоэлектроколориметра. Расчет концентрации ведут по калибровочному графику.
