
- •Химические методы
- •2. Инструментальные методы.
- •1. Химические методы:
- •2. Инструментальные методы:
- •1. Химический метод.
- •2. Инструментальные методы:
- •Вопрос 70 Алкалоиды производные хинолина (хинин). Химико-токсикологическая характеристика, физико-химические свойства, метаболизм. Особенности изолирования и химикотоксикологического анализа.
- •1. Химический метод.
- •2. Инструментальные методы.
Вопрос 64
Методы количественного определения «лекарственных ядов». Дифференциальная спектрофотометрия (на примере производных барбитуровой кислоты). Чувствительность и специфичность методов. Значение данных о количественном содержании вещества в органах трупа и биологических жидкостях при оценке результатов исследования.
Этот метод приемлем в том случае, когда при различных значениях pH среды изменяется спектр поглощения исследуемого вещества, а спектр поглощения примесей (посторонних экстрактивных веществ) остается без изменений.
В основу метода дифференциальной спектрофотометрии положена способность барбитуратов к лактим-лактамной таутомерии.
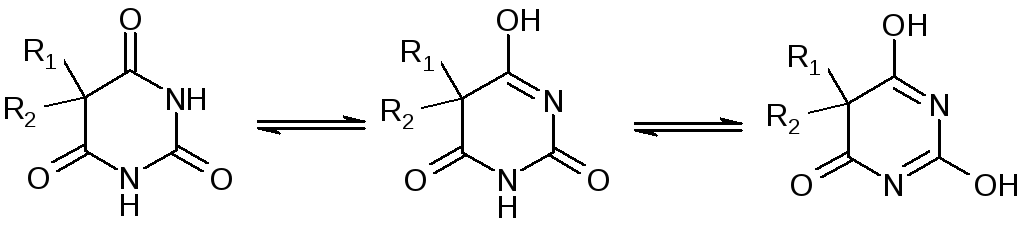
В органическом растворителе после экстракции барбитураты находятся в лактамной форме. В этом случае спектр поглощения барбитурата представляет собой ниспадающую кривую 1 в области 220-320 нм. Это связано с тем, что в лактамной форме в молекуле барбитурата отсутствуют сопряженные двойные связи.
При значении рН=10 барбитураты перейдут в лактимную форму. При регистрации спектра такого раствора обнаруживается максимум светопоглощения при 240 нм – кривая 2.
При значении рН=13 барбитураты перейдут в дилактимную форму. Спектр поглощения барбитурата имеет полосу с максимумом при 260 нм – кривая 3.
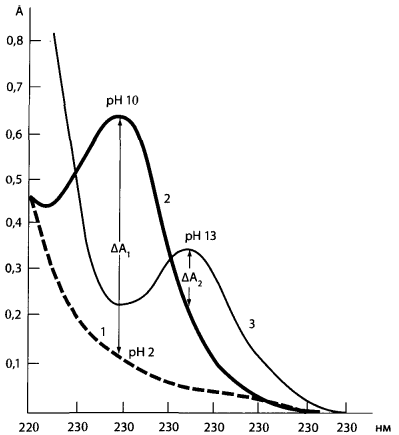
При исследовании внутренних органов определяют разницу в оптической плотности при рН=10 и рН=2 при длине волны 240 нм: ΔА1=А(рН10)-А(рН2)
При исследовании биологических жидкостей определяют разницу в оптической плотности при рН=13 и рН=10 при длине волны 260 нм: ΔА2=А(рН13)-А(рН10)
Расчет содержания барбитуратов проводят по удельному показателю поглощения, который рассчитывают при тех же значениях pH для раствора стандартного образца:
Е= ΔА/С*I
Более воспроизводимые результаты получаются в том случае, когда расчеты проводят по стандартному образцу: Сх=ΔАх*Сст./ΔАст.
Использование дифференциального варианта спектрофотометрического определения барбитуратов позволяет получить достаточно надежные результаты и исключить влияние посторонних веществ, экстрагируемых в процессе анализа вместе с барбитуратами из раствора при рН=2-2,5.
Вопрос 65
Фотометрические и экстракционно-фотометрические методы анализа (на примере азотсодержащих оснований). Чувствительность и специфичность методов. Значение данных о количественном содержании вещества в органах трупа и биологических жидкостях при оценке результатов исследования.
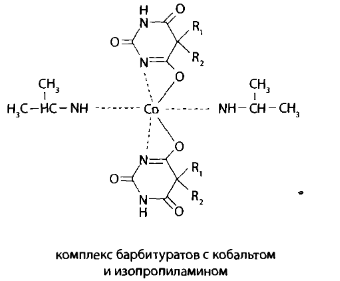
Фотометрический метод основан на образовании окрашенных соединений и измерении их опт. плотности. В данном случае – на взаимодействии барбитуратов с раствором ацетата кобальта в присутствии изопропиламина и метанола.
Хлороформный экстракт барбитуратов из биолог. материала выпаривают до сухого остатка. Сухой остаток, в зависимости от обнаруженного барбитурата, растворяют в хлороформе (барбитал, фенобарбитал) или метиловом спирте (барбамил, этаминал)
К полученным растворам добавляют по 5 мл 0,125% раствора ацетата кобальта в метиловом спирте и по 1 мл 50% изопропиламина в метиловом спирте. Оптическую плотность растворов, окрашенных в фиолетовый цвет, измеряют с помощью фотоэлектроколориметра ФЭК-М при зеленом светофильтре в кювете 20 мм. В качестве раствора сравнения применяют смесь реактивов.
Экстракционно-фотометрический метод используется для определения эфедрина в моче. Экстракционно-фотометрический метод основан на сочетании экстракции определяемого вещества и его последующим фотометрировании. Его применяют при анализе сложных смесей, когда нужно определить малые количества одних веществ в присутствии больших количеств др. веществ (как раз, например, в моче)
5 мл мочи подщелачивают 0,5% раствором NaOH до рН=12 и экстрагируют 3 раза 20 мл диэтилового эфира. Эфирные экстракты объединяют и испаряют досуха. Остаток переносят в колориметрич. пробирку, добавляют до насыщения кристаллич. CuSO4 и смешивают с 1 мл аммиачного р-ра CuSO4 и 3 мл 5% раствора сероуглерода в бензоле.
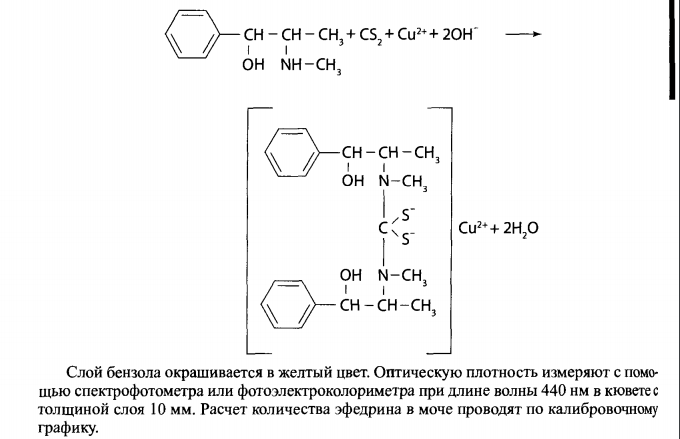
Слой бензола окрашивается в желтый цвет. Опт. Плотность измеряют при помощи спектрофотометра и фотоэлектроколориметра при 440нм в кювете с толщиной слоя 10мм.
Расчет кол-ва эфедрина проводят по калибровочному графику.
Вопрос 67
Производные барбитуровой кислоты (барбитал, фенобарбитал, барбамил, этаминал-натрия). Химико-токсикологическая характеристика, физико-химические свойства, метаболизм. Особенности изолирования и химикотоксикологического анализа.
Токсикологическое значение. Применяют как снотворные и успокаивающие ЛС (барбитал и фенобарбитал). Угнетают ЦНС. Развивается пристрастие и синергизм при приеме их с другими препаратами.
Злоупотребление приводит к наркомании: приятное ощущение состояния эйфории, общего благополучия, оглушенность, сонливость, вплоть до комы.
Состояние барбитуровой абстиненции развивается на следующие сутки и характеризуется мрачным настроением, тревогой, тремором рук, судорогами. Резко меняется соматическое состояние, наступает одряхление, снижается давление.
Тяжелые отравления характеризуются глубокой комой, редким поверхностным дыханием, слабым пульсом, цианозом, зрачки узкие, не реагирующие на свет.
Смерть от остановки дыхательного центра.
Применяют перорально в виде таблеток, порошков. Барбитураты способны кумулироваться в организме, и их длительное применение может привести к острым отравлениям.
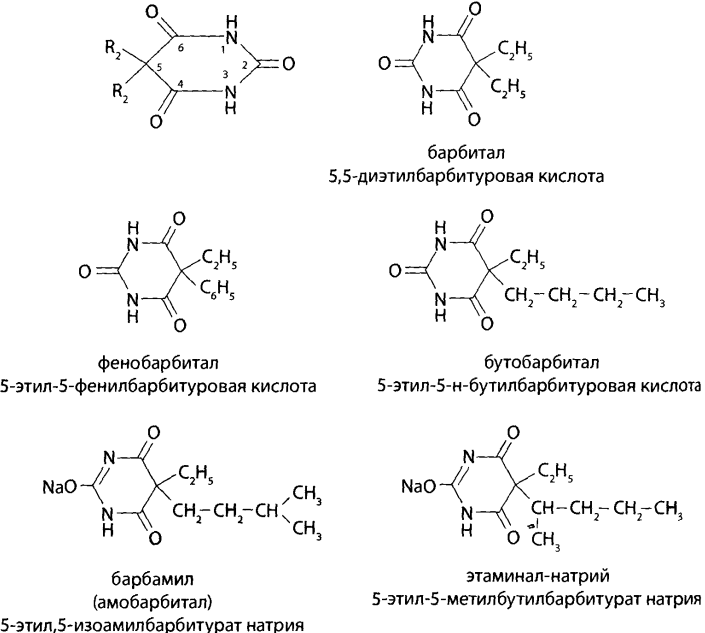
Метаболизм. 1 фаза – окисление.
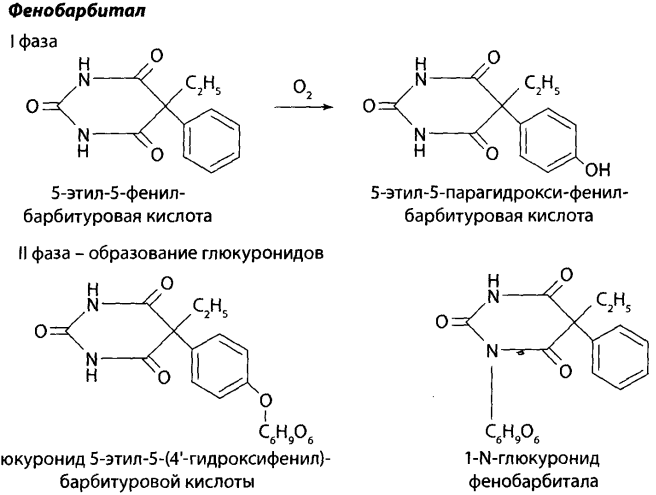
2 фаза – глюкуронирование.
Объекты анализа: трупный материал (1/3 печени, 1 почка, 1м толстого и тонкого кишечника, желудок с содержимым, головной мозг), лица с острым отравлением (промывные воды желудка, диализные воды, рвотные массы), наркоманы (кровь, моча)
Изолирование: общими методами Стаса – Отто и Швайковой-Васильевой (идут в кислое извлечение), частные методы Валовой и Поповой.
Обнаружение:
Химические методы
Мелкокристаллические реакции:
1. Обнаружение кислотной формы барбитуратов – экстракт испаряют на предметном стекле, растворяют в капле H2SO4 – обр. кристаллы специф. формы (реакция специфична, но имеет низк. чувствительность)
2. Реакция с хлорцинкйодом – характерные кристаллы (подтверждающая).
3. Реакция с подкисленным спиртовым раствором йодида калия – характерные кристаллы (подтверждающая).
4. Реакция со смесью растворов FeCl3 и KI (железойодидной комплексной солью) – характерные кристаллы (подтверждающая).
Цветные реакции:
1. Реакция с аммиачным раствором нитрата кобальта – красное-фиолетовое окрашивание (судебно-химическое значение при «-» результате – дальше исследование не проводят).
2. Реакция с меднопиридиновым реактивом (реакция Цвиккера) –
характерные кристаллы (подтверждающая).
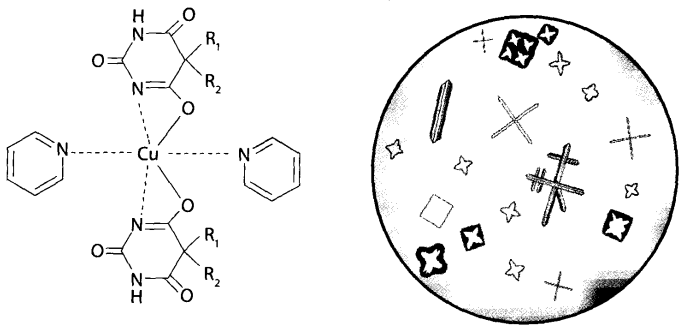
3. Мурексидная проба – красное окрашивание.
4. Реакция с родамином 6Ж – к р-ру исслед. в-ва добавляют родамин 6Ж и р-р ЧХУ. При наличии барбитуратов – слой ЧХУ приобретает оранж. Окраску
5. С изопропиламином и солями кобальта – фиолетовое окрашивание.
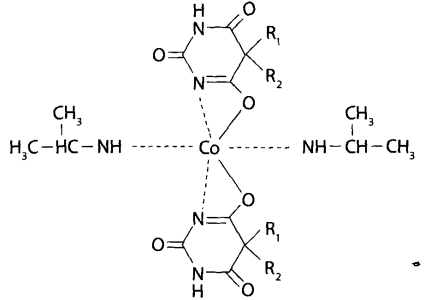
2. Инструментальные методы.
1. ТСХ в частной системе растворителей.
Сорбент: силикагель КСК, забуференный 0,1н р-ром H3BO3
Растворители: хлороформ (70) : бутанол (40) : 25% р-р аммиака (5)
Время насыщения камеры: 10 мин
Обнаружение:
Дифенилкарбазон (0,1% р-р в хлороформе)
Р-р CuSO4 5% в конц. H2SO4
Имеет «-» судебно-химическое значение при отсутствии на хроматограмме красно- или сине-фиолетовых пятен, дальнейшее исследование на барбитураты не проводят.
2. УФ-спектрофотометрия. Определяют спектры поглощения при различных превращения барбитуратов. - см. вопрос 64
3. ИК-спектрометрия. Для регистрации ИК-спектра остаток после испарения хлороформа (диэтилового эфира) растирают с бромидом калия и после прессования помещают в прибор для снятия спектра.
4. ГЖХ в сочетании с масс-спектрометрией (МС). Идентифицируют барбитураты по времени удерживания и по отношению массы ионов к заряду
Количественное определение:
1. Фотометрический метод основан на взаимод. барбитуратов с раствором ацетата кобальта в присутствии изопропиламина и метанола (полную методику см. вопрос 65).
Опт. плотность растворов, окрашенных в фиолетовый цвет, измеряют с помощью фотоэлектроколориметра ФЭК-М при зеленом светофильтре в кювете 20 мм. В качестве раствора сравнения применяют смесь реактивов.
6. Дифференциальная спектрофотометрия. см. вопрос 64
7. Метод ВЭЖХ.
Метод добавок. Для выделения токсических веществ из мочи используют жидкость-жидкостную экстракцию. Анализ ведут с двумя пробами мочи. С помощью ВЭЖХ проводят анализ экстракта из одной пробы мочи и экстракта из второй пробы мочи с добавлением в нее определенного количества вещества (эталонного раствора), обнаруженного при качественном анализе.
Метод внешнего стандарта. Он основан на линейной зависимости выходного сигнала от массы вещества. В этом случае параллельно с анализом экстракта из мочи в тех же условиях проводят анализ эталонного раствора найденного вещества приблизительно той же концентрации.
Метод внутреннего стандарта. К пробе мочи до операции пробоподготовки добавляют определенное количество вещества, которое является стандартом. Стандарт и определяемое вещество должны хорошо разделяться в процессе анализа.
При анализе барбитуратов в качестве внутренних стандартов рекомендуется использовать одно из следующих веществ: апробарбитал, метилфенобарбитал, фенилгидантоин, которые при хроматографировании полностью отделяются от компонентов образца.
Вопрос 68
Алкалоиды - производные пиридина и пиперидина (пахикарпин, никотин, анабазин). Химико-токсикологическая характеристика, физико-химические свойства, метаболизм. Особенности изолирования и химикотоксикологического анализа.
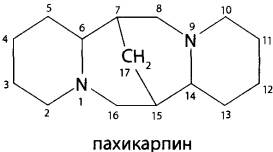
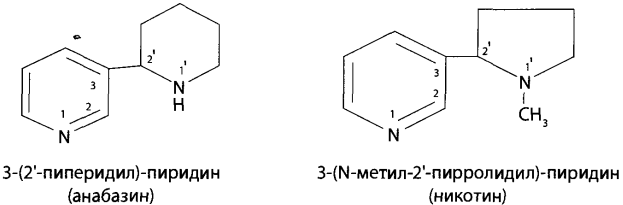
Токсикологическое значение.
1. Анабазина сульфат применяют в виде раствора и таблеток. Н-холиномиметик, поражает ЦНС, сначала возбуждает, потом парализует. При попадании per os возникают головные боли, понос, отдышка, желтуха, расстройство слуха, затем потеря сознания, остановка дыхания.
2. Пахикарпина гидрохлорид в виде растворов и таблеток. Вызывает слабость, головокружение, тошнота, рвота, боли в нижней части живота, помрачение сознания, похолодание рук и ног, ортостатический коллапс, тахикардия, клонико-тонические судороги, остановка дыхания и сердечной деятельности.
3. Никотин в медицине не используется. Проявления отравлений аналогичны. Вызывает сильную психическую зависимость, физическую слабо. Смерть быстрая от остановки сердца в диастоле.
Попадает в организм ингаляционно, перорально, инъекционно.
Объекты: как обычно (трупы, нарики, отравления)
Метаболизм. 1 фаза – метилирование, деметилирование у азота пироллидинового кольца, окисление.
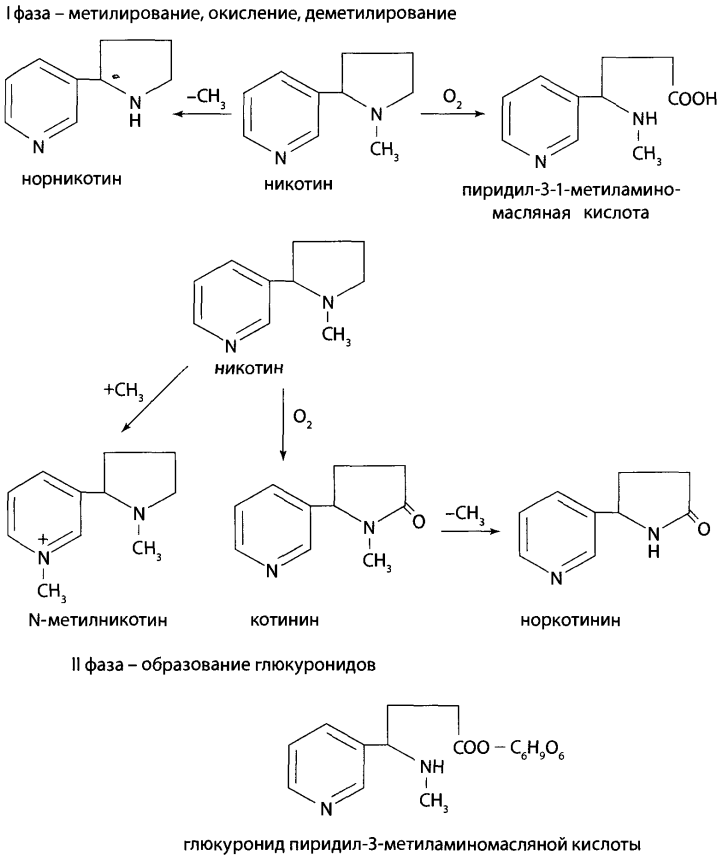
2 фаза – глюкуронирование.
Изолирование. Направленный анализ – перегонка с водяным паром. Ненаправленный – общими методами (идут в щелочное извлечение).
Частный метод – Крамаренко.
Обнаружение.
