
- •Вопрос 52 Общие методы изолирования ядовитых веществ полярными растворителями. Привести принципиальную схему изолирования по методу Стаса-Отто. Достоинства и недостатки метода.
- •Вопрос 53 Общие методы изолирования ядовитых веществ полярными растворителями. Привести принципиальную схему изолирования по методу Швайковой-Васильевой. Достоинства и недостатки метода.
- •Вопрос 54 Общие методы изолирования ядовитых веществ полярными растворителями. Привести принципиальную схему изолированиям по методу Карташова.
- •Вопрос 55. Частные методы изолирования ядовитых веществ поярными растворителями. Привести принципиальную схему изолирования по методу Крамаренко.
- •Вопрос 56 Частные методы изолирования ядовитых веществ полярными растворителями. Привести принципиальные схемы изолирования по методам Валова, Поповой.
- •Вопрос 57 Частные методы изолирования ядовитых веществ полярными растворителями. Привести принципиальную схему изолирования по методу Саломатина.
Вопрос 50
Общая характеристика, физико-химические свойства и реакционная способность ядовитых и сильнодействующих веществ органической природы. Основные физико-химические константы (рН, рКа, коэффициент распределения - Кр).
Ядовитые и сильнодействующие вещества – в-ва синтетического или природного происхождения, в том числе растения, способные при воздействии на организм вызвать острое или хроническое отравление или смерть.
Токсичность ксенобиотика зависит от физико-химических св-в ксенобиотика, таких как:
Устойчивость вещества – энергия Гиббса;
Проницаемость для клеточных мембран;
Кислотно-основные свойства;
Окислительно- восстановительный потенциал;
Способность к электрической диссоциации (ионизации);
Растворимость;
Липофильность;
Диффузионная способность;
Поверхностная активность;
Адсорбционные свойства;
Способность к комплексообразованию.
Характерной особенностью ксенобиотика явл-ся способность давать ионизированные и неионизированные формы. Существование различных форм зависит от величины константы ионизации в-ва и значения pH среды.
Для кислот константа ионизации определяется уравнением:
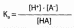
или в логарифмической форме:
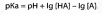
Для оснований константа ионизации:
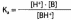
в логарифмической форме:
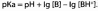
Кислота будет полностью ионизирована при рН=рКа+3, а основание при рН=рКа-3 в водных растворах. В смешанных или неводных растворителях эти соотношения могут изменяться. В этих случаях ограничивают значения pH до величины рКа±2 и даже меньше. При рН=рКа только 50% в-ва будет находиться в ионизированной форме.
При проведении ХТА большинство токсических в-в органической природы изолируются экстракцией в два этапа (1ый – твердо-жидкостная, 2ой – жидкость-жидкостная экстракция) например, для внутр. органов или в один этап (жидкость-жидкостная экстракция) для извлечения в-в из крови, мочи, слюны, лимфы, промывных вод желудка.
Жидкость-жидкостная экстракция – это метод выделения, разделения и концентрирования веществ, основанный на распределении растворенного вещества между двумя жидкими несмешивающимися фазами.
В токсикологии чаще всего одной жидкой фазой явл-ся вода, другой – органич. растворитель, который должен обладать высокой растворяющей способностью для анализируемого в-ва, иметь низкую температуру кипения (диэтиловый эфир, хлороформ). Выбор органич. растворителя определяется св-вами анализируемого в-ва.
В условиях равновесия отношение концентраций в-ва в обеих фазах представляется константой распределения (Кр), которая не зависит от общей концентрации в-ва.
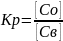
Co – конц. в орг. фазе;
Cв – конц. в водной фазе.
Чем больше Кр, тем эффективнее идет экстракция.
Коэффициент распределения определяют экспериментально в реальных условиях. Его значение используют для разработки условий экстракции ядовитого в-ва.
Вопрос 51 Общие и частные методы изолирования. Теоретические основы изолирования. Термодинамика процесса. Факторы, влияющие на эффективность экстракции на разных этапах изолирования (рН среды, степень ионизации вещества, природа экстрагента, время и кратность экстракции, влияние электролита и др.).
В токсикологии путем экстракции выделяют ксенобиотики из твердой фазы (различные ткани, органы, растительные объекты) и из жидкой фазы (кровь, моча, слюна, промывные воды желудка, перитонеальная жидкость и др).
Выделение токсических в-в из жидкой фазы (реэкстракция) часто используется и для очистки извлечений от примеси эндогенных соединений. С помощью жидкостной экстракции проводят выделение из объектов различных групп соединений: лекарственные, наркотические вещества, пестициды и др.
Общие методы:
Метод Стасса-Отто (изолирование подкисленным спиртом);
Метод Швайковой-Васильевой (изолирование подкисленной водой);
Частные методы:
Метод Крамаренко;
Метод Валова;
Метод Поповой;
Метод Саломатина;
Метод Карташова и др.
1-й этап изолирования – твердо-жидкостная экстракция: извлечение ксенобиотика из твердых объектов (твердая фаза) водным или спиртовым р-ром кислоты или основания. На этом этапе измельченные внутренние органы заливают экстрагентом, устанавливают необходимое значение pH и настаивают в течение определенного времени.
Факторы, влияющие на эффективность экстракции на 1ом этапе изолирования:
Степень измельчения органов;
Время настаивания;
Свойства растворителя, его природа;
Кратность операций;
рН среды и степень ионизации вещества;
Методы очистки.
В воде и спирте хорошо раствор-ся многие соли оснований и кислот. Время настаивания зависит от скорости проникновения экстрагента внутрь ткани.
Время настаивания объекта с водой: 1-2 ч. Вода легко проникает в ткани, поэтому быстро наступает равновесие между конц. токс. в-ва в ткани и в окружающей жидкости.
Время настаивания со спиртом: не менее 6 часов. Спирт денатурирует белковые молекулы на поверхности кусочков биоматериала, его проникновение в ткани затрудняется.
Для создания необходимого значения pH среды объект с экстрагентом подкисляют органической или неорганической кислотой (разбавленной). Природа кислоты может оказывать влияние на степень изолирования алкалоидов и органических оснований из биоматериала.
Чем лучше растворяются соли ядовитых веществ в данном растворителе, тем лучше они будут извлекаться.
Очистка вытяжек на 1 этапе изолирования:
Осаждение примесей;
Фильтрование;
Центрифугирование;
Гель-хроматография.
2-й этап изолирования ядов из биоматериала – жидкость-жидкостная экстракция. Самостоятельно применяется при извлечении веществ из крови, лимфы, слюны, перитониальной жидкости, мочи и промывных вод желудка. В процессе экстракции происходит распределение растворенного ксенобиотика между двумя несмешивающимися жидкостями, чаще всего 1 жидкая фаза – вода, 2 – органический растворитель.
Факторы, влияющие на эффективность экстракции на 2ом этапе изолирования:
рН и степень ионизации вещества;
Кратность операций;
Свойства экстрагента и его природа;
Объём растворителя;
Добавление электролита.
Добавление электролитов в водную вытяжку оказывает высаливающее действие за счет понижения растворимости ядовитых веществ в воде. В результате повышается степень их экстракции органическим растворителем. Влияние pH зависит от характера извлекаемого вещества:
При экстракции органическим растворителем вещество в водной фазе должно находиться в молекулярном, неионизированном состоянии;
Для веществ кислотного хар-ра необходимо создать в растворе рН=рКа-2, а для оснований – рН=рКа+2;
Для веществ нейтрального хар-ра значение pH особого значения не имеет. Эти соединения экстрагируются как из кислой, так и из щелочной среды;
Для веществ, являющихся амфолитами, расчет pH для экстракции производится иначе. В этих соединениях имеются кислотная и основная группы, и для каждой известна величина рКа.
Очистка экстрактов на 2 этапе изолирования:
Возгонка;
Реэкстракция;
Электрофорез;
ТСХ.
Вопрос 52 Общие методы изолирования ядовитых веществ полярными растворителями. Привести принципиальную схему изолирования по методу Стаса-Отто. Достоинства и недостатки метода.
Метод Стаса-Отто (изолирование подкисл. спиртом):
1 этап твердо-жидкостная экстракция:
Настаивание 100 г измельченного объекта (0,5х0,5х0,5) с этанолом 96%, подкисленным щавелевой кислотой до рН=2,5-3 в течение суток, трижды (24+24+24=72 ч), каждую надосадочную жидкость сливают, объединяют;
Упаривание объединенных спиртовых извлечений при 40-50 С до густого остатка, в который по каплям добавляют абсолютный этанол для коагуляции белков до прекращения образования хлопьев, фильтруют;
Упаривание фильтрата снова при 40-50 С до густого остатка и разбавление горячей водой для удаления смолистых в-в, жиров, пигментов.
2 этап жидкость-жидкостная экстракция:
Экстрагирование в-в кислого, нейтрального, слабоосновного характера из водного фильтрата хлороформом при рН=2 (трехкратно по 50 мл), отделяют и объединяют хлороформные извлечения (150 мл), концентрируют полученное кислое извлечение упариванием (фракция А);
Подщелачивание NaOH оставшегося после разделения фаз водного слоя до рН=9-10, экстрагирование в-в сильноосновного хар-ра (трехкратно по 50 мл) хлороформом, отделяют и объединяют органич. фазу, концентрируют общее щелочное извлечение упариванием (фракция Б).
Достоинства:
Метод универсален, т. к. этанол явл-ся хорошим растворителем для многих в-в этой группы;
Метод предусматривает очистку от балластных в-в;
Можно использовать для материала, подвергшегося гниению.
Недостатки:
Длительность (8-10 дней) и многостадийность;
Потери искомых в-в;
Сравнительная дороговизна метода.
Вопрос 53 Общие методы изолирования ядовитых веществ полярными растворителями. Привести принципиальную схему изолирования по методу Швайковой-Васильевой. Достоинства и недостатки метода.
Метод Швайковой-Васильевой (изолирование водой, подкисл. щавелевой кислотой):
1 этап твердо-жидкостная экстракция:
Настаивание 100 г измельченного объекта (0,5х0,5х0,5) с водой, подкисленной щавелевой к-той до рН=2-3, дважды, в течение 2х часов, затем 1 час, каждую надосадочную жидкость сливают, объединяют;
Центрифугирование объединенного извлечения 30 мин при 3000 об/мин;
2 этап жидкость-жидкостная экстракция:
Экстрагирование в-в кислого, нейтрального и слабоосновного хар-ра из водного фильтрата (центрифугата) хлороформом при рН=2 (трехкратно по 50 мл), отделяют и объединяют хлороформные извлечения (150 мл), концентрируют упариванием (кислое извлечение);
Подщелачивание оставшегося после разделения фаз водного слоя 25% р-ром NH4OH до рН= 9-10, экстрагирование в-в основного хар-ра (трехкратно по 50 мл) хлороформом, отделяют и объединяют органич. фазу, концентрируют упариванием (щелочное извлечение).
Достоинства:
Быстрота (в течение 1 дня);
Меньшее кол-во операций, меньше потери искомых веществ;
Экономичность и дешевизна.
Недостатки:
Образование стойких эмульсий при экстрагировании в-в из водной фазы хлороформом;
Не пригоден при анализе загнившего материала.
