
- •ВВЕДЕНИЕ
- •1.1. История открытия эффекта памяти формы
- •1.3. Мартенситные превращения
- •1.4. Термоупругие мартенситные превращения
- •1.5. Кинетика и термодинамика мартенситного превращения
- •1.6. Механические эффекты в сплавах с термоупругим мартенситным превращением
- •1.8. Сплавы на основе Ni-Ti
- •1.9. Сплавы на основе меди
- •1.10. Профилированные монокристаллы Cu-Al-Ni
- •1.11. Выращивание монокристаллов Cu-Al-Ni методом Степанова
- •1.12. Применение сплавов с эффектом памяти формы
- •2. НИТЕВИДНЫЕ КРИСТАЛЛЫ
- •2.1. Нитевидные нанокристаллы
- •2.2. Классическая картина ПЖК-роста
- •2.3. Металлические катализаторы
- •2.4. Температура процесса роста ННК
- •2.5. Кристаллографическое направление роста
- •2.6. Поверхностная миграция катализатора
- •2.7. Прочность и совершенство кристаллической структуры
- •3. ТЕРМОЭЛЕКТРИЧЕСКИЕ МАТЕРИАЛЫ
- •3.1. Эффект Зеебека
- •3.2. Эффект Пельтье
- •3.3. Эффект Томсона
- •3.4. Эффективность термоэлектрических материалов
- •3.5. Существующие «классические» термоэлектрические материалы
- •3.6. Новые подходы к получению материалов с высокой термоэлектрической добротностью
- •3.8. Примеры применения термоэлектрических материалов
- •ЗАКЛЮЧЕНИЕ
- •БИБЛИОГРАФИЧЕСКИЙ СПИСОК
катализатора, выраженного через угол ϕ между касательной к поверхности капли и осью кристалла, как r = Rcosϕ (рис.
2.7, а).
Из данного выражения следует, что более тонкие проволоки могут быть получены с использованием более мелких капель
(рис. 2.7, б).
2.4. Температура процесса роста ННК
Интервал температур, при котором удается стабильно выращивать ННК различных веществ, составляет 600-1000 K. Удивительным фактом является то, что наноразмерные ННК некоторых полупроводниковых материалов выращиваются при температурах ниже наименьшей точки плавления раствора с метал- лом-катализатором (эвтектической точки), т.к. при температуре ниже эвтектической раствор в жидком состоянии существовать не может. Типичным примером является выращивание ННК InAs с Au-катализатором в интервале температур 653−703 K, что ниже минимальной эвтектической точки раствора Au−In, равной 727 K. Похожие результаты получены при выращивании нанокристаллов в системе Al−Si при температуре 703-763 К, в то время как температура эвтектики на фазовой диаграмме Al−Si составляет 850 K, и при выращивании НК Si с частицами Ag при 773 K, при этом температура эвтектики сплава Ag−Si 1109 K. Cамая низкая эвтектическая точка диаграммы Ti−Si составляет 1603 K, что значительно выше температур 913-943 K, используемых для выращивания нанопроволок Si с титановым катализатором. Для объяснения этих и других подобных результатов был предложен механизм роста ННК пар−кристалл−кристалл (ПКК), согласно которому рост ННК при температурах ниже эвтектических происходит из твердого раствора на вершине кристалла. Однако, например, имеющиеся данные по картинам дифракции быстрых электронов на отражение (ДБЭО) от поверхности InAs с частицами Au, полученными
63
разбиением пленки толщиной 1 нм, свидетельствуют о фазовом переходе твердое→жидкое в области температур между 633 и 698 К при выращивании ННК InAs, что ниже температуры эвтектики.
Для объяснения указанных фактов сделано предположение, что, принимая во внимание сложный состав и малый размер нанокапли, ответ на вопрос о фазовом состоянии катализатора неочевиден, и можно полагать, что фазовая диаграмма «наноскопическая капля металла-ННК» квазидвойной системы Au−InAs, как и других подобных систем (Au −Si, Al−Si, Ti−Si, Fe−C и др.) может существенно изменяться за счет поверхностной энергии капли. На диаграммах фазовых равновесий предельные концентрации растворенного вещества, находящегося в равновесии с дисперсной средой малых размеров, должны быть смещены в сторону меньших значений.
На смещение линий фазовых равновесий указывает также повышение абсолютной величины равновесной температуры кристаллизации (растворения) Si с увеличением дисперсности R-1 капли катализатора. Другими словами, поскольку с уменьшением размера R (увеличением дисперсности) частиц катализатора растворимость твердой фазы в них понижается, а абсолютная величина равновесной температуры кристаллизации (растворения) Si повышается, то это должно отражаться на смещении линий ликвидуса и солидуса для дисперсных частиц катализатора диаграмм состояния Ме−Si, например, для диаграммы состояния двухфазной системы эвтектического типа Au−Si
(рис. 2.8).
64
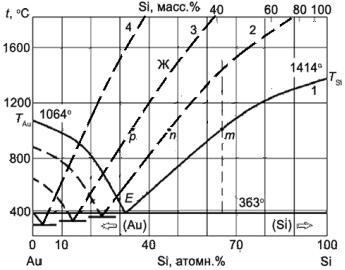
Рис. 2.8. Диаграмма фазового равновесия Si-Au, схематически иллюстрирующая зависимость предельной концентрации Si в макроскопических и наноскопических каплях металлакатализатора. Пунктирными линиями показано смещение линий ликвидуса и солидуса при увеличении дисперсности (уменьшение радиуса капель) частиц катализатора Au-Si: цифры 1-4 обозначают переход от макроскопической системы к нанодисперсной
Как видно из рис. 2.8, диаграмма распадается на три поля: верхнее поле расплава Au−Si, снизу ограниченное кривой ликвидуса TАu-E-TSi; нижнее поле твердых фаз, ограниченное сверху кривой солидуса с точкой Е; между этими кривыми – область кристаллизации. Для роста ННК с участием наноразмерных час-
тиц, для которых давление насыщенного пара мало (Р~ →0), в соответствии с правилом фаз Гиббса в качестве независимых переменных в принята температура и дисперсность.
65
Процесс охлаждения (кристаллизации) двухкомпонентного сплава Au-Si в фигуративной точке m на линии ликвидуса со стороны Si (рис. 2.8) можно представить следующим образом.
Для макроскопической системы Si−Au (полагаем R-1=0 и
Р~ =0) при охлаждении расплава в фигуративной точке m начинается кристаллизация Si и имеется две фазы (жидкая и твердая), система является гетерогенной и моновариантной (число степеней свободы i=2−2+1=1).
Для дисперсных наноскопических частиц Si−Au (R-1>0, Р~ =0) в точке m система имеет две степени свободы (i=2−2+2=2). Это означает, что в данной точке можно произвольно изменять температуру и размер частиц катализатора, не изменяя числа фаз.
Изменение состава Au-Si (содержания Si в капле) при дальнейшем охлаждении не может быть произвольным и будет определяться линией mE (при охлаждении выпадает все большее количество кристаллов Si, а состав расплава капли смещается в сторону эвтектики Е, обогащаясь Au). При достижении в точке Е линии солидуса кристаллизуется эвтектическая смесь. При этом сама линия mE будет смещаться при изменении R-1, т.е. состав капли будет зависеть от величины дисперсности.
Необходимо заметить, что с уменьшением характерного размера капли катализатора угол наклона линии ликвидуса mE, nЕ, pE и т.д. в силу экспоненциальной зависимости растворимости кристаллизуемого вещества от радиуса капли должен увеличиваться. Поэтому пересыщение или переохлаждение, возникающее в каталитической частице при росте ННК, с уменьшением их размера должно увеличиваться. Следовательно, скорость роста ННК, как правило, должна быть возрастающей функцией радиуса, что в большинстве случаев подтверждается на практике.
66
