
Средние циклы
Внутримолекулярная циклизация производных дикарбоновых кислот.
Синтез циклов среднего размера путем внутримолекулярной циклизации, как правило, дает очень низкие выходы целевых продуктов. По причинам, которые были рассмотрены выше, предпочтительным оказывается межмолекулярное взаимодействие, приводящее к линейным димерам и полимерам. Для подавления межмолекулярного взаимодействия реакции проводят в условиях сверхразбавления, которое должно препятствовать межмолекулярному взаимодействию (бимолекулярной реакции). Однако и в этих условиях выходы продуктов циклизации низки.
Исключение составляет ацилоиновая конденсация, которая дает высокие выходы средних циклов (схема 8, n>6). Это гетерогенный процесс, протекающий на поверхности металлического натрия. Гетерогенные условия реакции способствуют циклизации. При высоком разбавлении электронодефицитные центры на концах молекулы адсорбируются на поверхности натрия, сближаются и взаимодействуют с образованием цикла.
Реакции циклоолигомеризации.
Ц иклотетрамеризация
ацетилена в присутствии солей никеля
дает циклооктатетраен:
иклотетрамеризация
ацетилена в присутствии солей никеля
дает циклооктатетраен:
Циклодимеризацией и циклотримеризацией 1,3-бутадиена на металлокомплексных катализаторах получают соответственно 1,5-циклооктадиен и 1,5,9-циклододекатриен:
С елективное
протекание процесса обеспечивается
предварительной координацией ненасыщенного
соединения вокруг комплексообразователя
за счет образования -комплекса
. В результате этого формируется взаимное
расположение молекул субстрата, близкое
по геометрии к переходному состоянию,
ведущему к образованию циклического
продукта определенного строения.
елективное
протекание процесса обеспечивается
предварительной координацией ненасыщенного
соединения вокруг комплексообразователя
за счет образования -комплекса
. В результате этого формируется взаимное
расположение молекул субстрата, близкое
по геометрии к переходному состоянию,
ведущему к образованию циклического
продукта определенного строения.
Физические свойства и строение
Физические свойства циклоалканов аналогичны свойствам алканов. Это бесцветные нерастворимые в воде вещества. Циклопропан и циклобутан – газы, циклоалканы С5-С11 – жидкости, начиная с С12 – твердые вещества. Температуры кипения и плавления, а также плотности у циклоалканов несколько выше, чем у соответствующих алканов, что связано с большей упорядоченностью циклических структур.
Циклоалканы обладают разной термодинамической стабильностью, которая зависит от размера цикла. Это связано с существованием у циклических молекул напряжения. Напряжение возникает в результате отклонения параметров молекулы от стандартных величин. В циклических структурах существует три основных вида напряжения.
Угловое напряжение (напряжение Байера) обусловлено отклонением валентных углов в цикле от стандартных значений.
Торсионное напряжение (напряжение Питцера) – напряжение, вызванное заслоненным положением химических связей.
Напряжение Ван-дер-Ваальса обусловлено взаимодействиями между валентно не связанными атомами при их сближении на расстояние меньшее суммы ван-дер-ваальсовых радиусов. В циклах этот тип напряжения проявляется во взаимодействии между атомами, расположенными на противоположных сторонах. Такие взаимодействия называют трансаннулярными, а возникающее в результате напряжение - трансаннулярным (или напряжением Прелога).
Молекулы стремятся принять конформацию, свободную от всех видов напряжения. Циклические молекулы, как правило, не могут полностью освободиться от напряжения, так как для них снятие одного вида напряжения приводит к увеличению другого. Поэтому они стремятся принять конформацию, в которой сумма всех видов напряжения минимальна.
Напряжение молекулы количественно выражается её избыточной энергией по сравнению со стандартным соединением, в котором все структурные параметры (длины связей, валентные углы, расстояния между валентно не связанными атомами) не отклоняются от стандартных значений и все связи находятся в заторможенных конформациях. Эта избыточная энергия называется энергией напряжения. Энергия напряжения определяется как разность энтальпий образования исследуемого вещества и стандартного вещества. Для циклоалканов стандартом служит линейный алкан с длинной цепью или циклогексан. И тот, и другой практически свободны от всех видов напряжения. Для сравнения термодинамической устойчивости циклоалканов используют энергию напряжения в расчете на одну группу СН2. Наибольшее напряжение существует в малых и средних циклах. Обычные циклы и макроциклы практически свободны от напряжения.
Таблица 44.1. Энергии напряжения циклоалканов относительно циклогексана в расчете на одну группу СН2.
Циклоалкан |
Энергия напряжения, кДж/моль |
Циклоалкан |
Энергия напряжения, кДж/моль |
Циклопропан |
37,7 |
Циклооктан |
5,1 |
Циклобутан |
26,4 |
Циклононан |
5,9 |
Циклопентан |
5,0 |
Циклодекан |
5,0 |
Циклогексан |
0 |
Циклоундекан |
4,2 |
Циклогептан |
3,7 |
Циклододекан |
1,8 |
Малые циклы
Циклопропан
Молекулы циклопропана представляет собой правильный треугольник. Связи С-Н расположены в плоскости, перпендикулярной плоскости цикла.
Э то
означает, что в молекуле циклопропана
существует значительное угловое
напряжение (валентные углы в цикле 600
вместо 1090 для sp3-гибридизации)
и торсионное напряжение (все связи
неизбежно находятся в заслоненном
положении). Как результат этого,
циклопропан имеет наибольшую среди
циклоалканов энергию напряжения в
расчете на одну группу СН2.
то
означает, что в молекуле циклопропана
существует значительное угловое
напряжение (валентные углы в цикле 600
вместо 1090 для sp3-гибридизации)
и торсионное напряжение (все связи
неизбежно находятся в заслоненном
положении). Как результат этого,
циклопропан имеет наибольшую среди
циклоалканов энергию напряжения в
расчете на одну группу СН2.
Связи С-С и С-Н в циклопропане отличаются от связей в алканах. Гибридные орбитали атомов углерода в циклопропане неэквивалентны. Орбитали, за счет которых образуются связи С-Н, имеют больший s-характер по сравнению с sp3 –гибридными орбиталями. Орбитали, образующие С-С связи, имеют меньший s-характер и, следовательно, близки по характеру к р-орбиталям. В силу геометрии молекулы при образовании С-С связей не достигается максимальное перекрывание атомных орбиталей. Орбитали перекрываются не на линии, связывающей центры атомов, а в стороне от кольца. Такие связи называют -связями («банановые» связи). По своему характеру они занимают промежуточное положение между - и -связями. Доказательством частичного -характера С-С связей в циклопропане является сравнительно низкая энергия ионизации (для пропана 11,5 эВ, циклопропана – 10,5 эВ, пропена – 9,7.эВ), а также способность циклопропанового кольца к сопряжению с -связями, что проявляется в спектральных характеристиках винилциклопропанов и их химических свойствах.
Циклобутан
В случае плоского строения молекула
циклобутана должна иметь угловое
напряжение (валентные углы в цикле 900
вместо 1090) и торсионное напряжение
(все связи находятся в заслоненном
положении). В действительности циклобутан
имеет неплоское строение. Он существует
преимущественно в сложенной конформации
с углом между плоскостями ~ 1450.
Переход в сложенную конформацию уменьшает
торсионное напряжение, так как связи
переходят в частично скошенное положение.
Однако при этом увеличивается угловое
напряжение за счет уменьшения углов.
Разница в энергиях между плоской и
сложенной конформациями невелика
случае плоского строения молекула
циклобутана должна иметь угловое
напряжение (валентные углы в цикле 900
вместо 1090) и торсионное напряжение
(все связи находятся в заслоненном
положении). В действительности циклобутан
имеет неплоское строение. Он существует
преимущественно в сложенной конформации
с углом между плоскостями ~ 1450.
Переход в сложенную конформацию уменьшает
торсионное напряжение, так как связи
переходят в частично скошенное положение.
Однако при этом увеличивается угловое
напряжение за счет уменьшения углов.
Разница в энергиях между плоской и
сложенной конформациями невелика
сложенная плоская сложенная
Искажение валентных углов приводит к тому, что связи в циклобутане изогнуты, но в значительно меньшей степени, чем в циклопропане. Общая напряженность молекулы циклобутана достаточно велика, но она меньше, чем у циклопропана (см. таблицу 44.1).
Обычные циклы
Циклопентан
П лоский
циклопентан практически лишен углового
напряжения (валентные углы в цикле 1080
вместо 1090), но имеет значительное
торсионное напряжение (заслоненное
положение связей). Уменьшение энергии
реальной молекулы циклопентана происходит
за счет вывода из плоскости одного
(конформация «конверт») или двух соседних
(конформация «твист») атомов углерода.
лоский
циклопентан практически лишен углового
напряжения (валентные углы в цикле 1080
вместо 1090), но имеет значительное
торсионное напряжение (заслоненное
положение связей). Уменьшение энергии
реальной молекулы циклопентана происходит
за счет вывода из плоскости одного
(конформация «конверт») или двух соседних
(конформация «твист») атомов углерода.
«конверт» «твист»
При этом уменьшается торсионное напряжение, так как несколько связей переходят из заслоненного в скошенное положение. Одновременно происходит некоторое искажение валентных углов. Таким образом, молекула циклопентана имеет небольшое угловое и торсионное напряжения. Выигрыш в энергии при переходе из плоской конформации в конформации «конверт» или «твист» составляет 22 кДж/моль. Неплоские конформации циклопентана близки по энергии и быстро переходят друг в друга. При этом поочередно отгибаются все пять углов цикла, который, таким образом, находится в волнообразном движении («псевдовращение»).
Циклогексан
Незамещенный циклогексан
В случае плоского строения циклогексан имел бы значительное угловое напряжение (валентные углы в цикле 1200 вместо 1090) и торсионное напряжение. Термодинамические измерения показывают, что циклогексан практически лишен всех видов напряжения.
Молекула циклогексана может существовать в виде нескольких неплоских конформаций, в которых сохраняются нормальные валентные углы:
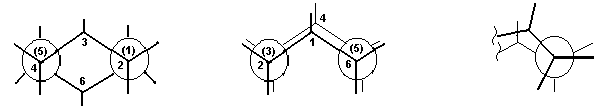
 «кресло»
«ванна»
«твист»
«кресло»
«ванна»
«твист»
Наиболее устойчивой из них является конформация «кресло», которая лишена углового и торсионного напряжения. Рассмотрение проекций Ньюмена для любого из четырехуглеродных (бутаноподобных) фрагментов показывает, что в этой конформации нет заслоненных положений С-С и С-Н связей, а расположение С-С- связей такое же, как в скошенной конформации бутана.
Конформация «ванна», несмотря на нормальные валентные углы, значительно менее устойчива. Это обусловлено торсионным напряжением, так как в заслоненном положении оказываются связи С-Н в положениях 2 и 3, 5 и 6 в основании ванны. Кроме того, возникает ван-дер-ваальсово напряжение между «бушпритными» атомами Н в вершинах «ванны» (положения 1 и 4), которые сближаются на расстояние, меньшее суммы их радиусов. В результате форма «ванны» на 29 кДж/моль превышает по энергии форму «кресла».
«Твист» –конформация может быть получена из конформации «ванна» путем скручивания её вокруг центральной оси. При этом атомы С1 и С4 удаляются друг от друга, что приводит к устранению ван-дер-ваальсова напряжения, а атомы Н в основании ванны частично выводятся из заслоненного положения, что уменьшает торсионное напряжение. Т. о., конформация «твист» беднее энергией, чем конформация «ванны», но превышает по энергии конформацию «кресла».
При обычных
температурах циклогексан на 99,9% существует
в конформации «кресла». В этой конформации
циклогексан имеет два типа связей С-Н:
аксиальные (а) и экваториальные
(е). Аксиальные связи ориентированы
параллельно оси симметрии цикла и
направлены попеременно вверх и вниз.
Экваториальные связи расположены под
углом 1090 к оси симметрии цикла и
направлены также попеременно вверх и
вниз. Для незамещенного циклогексана
возможны две энергетически равноценные
конформации «кресла», которые превращаются
друг в друга путем вращения вокруг С-С
связей. Такое превращение называют
интерконверсией ц икла.
При интерконверсии все экваториальные
связи переходят в аксиальные и наоборот.
икла.
При интерконверсии все экваториальные
связи переходят в аксиальные и наоборот.
Взаимопревращение между двумя конформациями «кресла» происходит через ряд менее устойчивых форм. Механизм интерконверсии может быть представлен следующей схемой.
« кресло»
«полукресло» «твист» «ванна»
«твист» «полукресло» «кресло»
кресло»
«полукресло» «твист» «ванна»
«твист» «полукресло» «кресло»
К онформация
«кресло» переходит в «твист»-форму
через стадию образования неустойчивой
конформации «полукресло», в которой в
одной плоскости находятся четыре
соседних атома углерода. Т. о., конформация
«полукресло» является переходным
состоянием между конформациями «кресло»
и «твист». Далее «твист»-конформация
через конформацию «ванны» скручивается
в другую сторону и превращается в
альтернативную «твист»-конформацию и
далее через конформацию «полукресло»
превращается в другую конформацию
«кресла». Т. о., конформация «ванны»
является переходным состоянием между
двумя «твист»-формами.
онформация
«кресло» переходит в «твист»-форму
через стадию образования неустойчивой
конформации «полукресло», в которой в
одной плоскости находятся четыре
соседних атома углерода. Т. о., конформация
«полукресло» является переходным
состоянием между конформациями «кресло»
и «твист». Далее «твист»-конформация
через конформацию «ванны» скручивается
в другую сторону и превращается в
альтернативную «твист»-конформацию и
далее через конформацию «полукресло»
превращается в другую конформацию
«кресла». Т. о., конформация «ванны»
является переходным состоянием между
двумя «твист»-формами.
