
Циклобутан
Дегалогенирование 1,4-дигалогеналканов (схема 1, n=2).
Циклоалкилирование 1,3-дигалогеналканами соединений с активной метиленовой группой. (схема 3, n=3).
Ацилоиновая конденсация.
2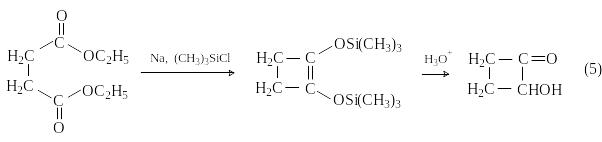 -Гидроксибутанон
(ацилоин) может быть получен
внутримолекулярной ацилоиновой
конденсацией диэтилового эфира
янтарной
кислоты в присутствии триметилхлорсилана:
-Гидроксибутанон
(ацилоин) может быть получен
внутримолекулярной ацилоиновой
конденсацией диэтилового эфира
янтарной
кислоты в присутствии триметилхлорсилана:
[2+2]-Циклоприсоединение.
А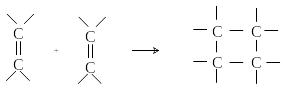 лкены
и их производные вступают в реакции
циклоприсоединения с образованием
циклобутанового кольца:
лкены
и их производные вступают в реакции
циклоприсоединения с образованием
циклобутанового кольца:
Реакции инициируется нагреванием или облучением:
Э
 лектроциклические
реакции 1,3-диенов.
лектроциклические
реакции 1,3-диенов.
Сопряженные диены
в ступают
в реакцию внутримолекулярной циклизации
с образованием новой -связи
по концам сопряженной системы:
ступают
в реакцию внутримолекулярной циклизации
с образованием новой -связи
по концам сопряженной системы:
Реакция протекает по синхронному механизму и инициируется термически или фотохимически. Стереохимический результат реакции определяется правилами орбитальной симметрии и зависит от способа инициирования:
О бычные циклы
Циклогексан, циклопентан и их гомологи получают при переработке нефти (нафтены). Синтетически они могут быть получены следующими методами.
Восстановление аренов и ненасыщенных алициклических соединений.
Ц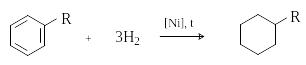 иклогексан
и его гомологи получают каталитическим
гидрированием
бензола и гомологов бензола:
иклогексан
и его гомологи получают каталитическим
гидрированием
бензола и гомологов бензола:
Ц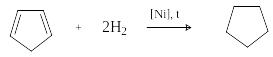 иклопентан
может быть получен гидрированием
ненасыщенного алициклического
углеводорода – циклопентадиена
(содержится в продуктах переработки
каменного угля и нефти).
иклопентан
может быть получен гидрированием
ненасыщенного алициклического
углеводорода – циклопентадиена
(содержится в продуктах переработки
каменного угля и нефти).
Дегидроциклизация алканов.
При пропускании над платиновым катализатором при 3000С алифатических углеводородов с пятью углеродными атомами в цепи происходит их дегидроциклизация с образованием циклопентана и его гомологов, например:
Е сли
алкан содержит цепь из 6 и более атомов
углерода, то происходит замыкание
шестичленного цикла, который при
отсутствии в цикле четвертичного атома
углерода далее дегидрируется в бензол
или его гомолог.
сли
алкан содержит цепь из 6 и более атомов
углерода, то происходит замыкание
шестичленного цикла, который при
отсутствии в цикле четвертичного атома
углерода далее дегидрируется в бензол
или его гомолог.
Внутримолекулярная циклизация производных дикарбоновых килот..
Обычные циклы легко образуются в результате внутримолекулярной циклизации ,-бифункциональных соединений, содержащих функциональные группы, способные взаимодействовать с образованием С-С связи. Такие реакции являются внутримолекулярными аналогами известных межмолекулярных реакций.
Сухая перегонка солей дикарбоновых кислот и щелочно-земельных металлов приводит к образованию циклических кетонов:
В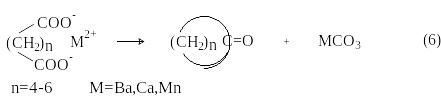
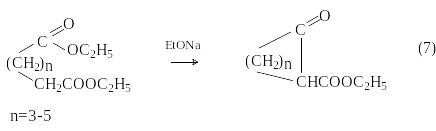 нутримолекулярной
сложноэфирной конденсацией эфиров
дикарбоновых кислот (конденсация
Дикмана)
получают циклические кетоэфиры
нутримолекулярной
сложноэфирной конденсацией эфиров
дикарбоновых кислот (конденсация
Дикмана)
получают циклические кетоэфиры
Внутримолекулярная ацилоиновая конденсация дает циклические ацилоины:
В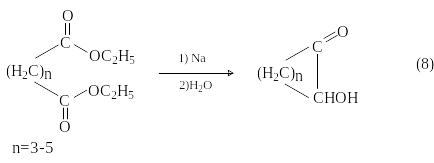
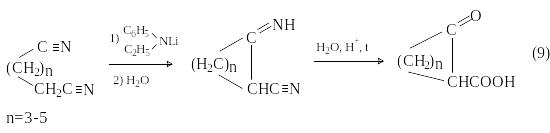 нутримолекулярная
циклизация динитрилов карбоновых кислот
(метод Торпа-Циглера)
приводит к иминонитрилам и далее к
кетокислотам:
нутримолекулярная
циклизация динитрилов карбоновых кислот
(метод Торпа-Циглера)
приводит к иминонитрилам и далее к
кетокислотам:
Межмолекулярная сложноэфирная конденсация.
П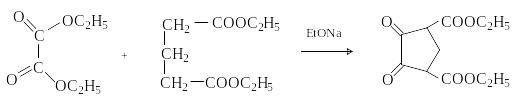 ерекрестной
сложнофирной конденсацией эфиров
щавелевой (не содержит атомов водорода
в -положении
и не может, следовательно, выступать в
качестве метиленовой компоненты) и
глутаровой кислот получают производные
1,2-циклопентандиона:
ерекрестной
сложнофирной конденсацией эфиров
щавелевой (не содержит атомов водорода
в -положении
и не может, следовательно, выступать в
качестве метиленовой компоненты) и
глутаровой кислот получают производные
1,2-циклопентандиона:
С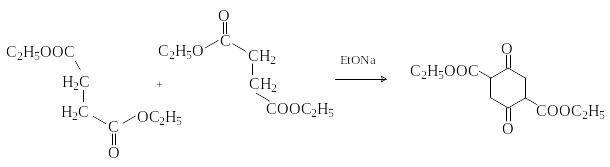 ложноэфирная
конденсация эфира янтарной кислоты
дает производные 1,4-гександиона:
ложноэфирная
конденсация эфира янтарной кислоты
дает производные 1,4-гександиона:
Реакции [2+4]-циклоприсоединения (реакция Дильса-Альдера)
В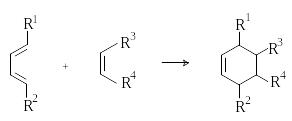 ажный
метод синтеза шестичленных циклов. См.
лек.№14.
ажный
метод синтеза шестичленных циклов. См.
лек.№14.
Электроциклические реакции сопряженных триенов.
П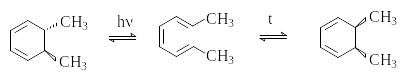 роизводные
1,3,5-гексатриена при нагревании или
облучении циклизуются в производные
1,3-циклогексадиена. При термической
циклизации образуются цис-,
а при фотохимической – транс-дизамещенные
циклогексадиены:
роизводные
1,3,5-гексатриена при нагревании или
облучении циклизуются в производные
1,3-циклогексадиена. При термической
циклизации образуются цис-,
а при фотохимической – транс-дизамещенные
циклогексадиены:
