
- •Лекция №38
- •1,3 Дикетоны. , - Непредельные альдегиды и кетоны. Ароматические альдегиды и кетоны
- •Кислотность и енолизация
- •Образование солей
- •Взаимодествие с электрофильными реагентами.
- •Взаимодействие с нуклеофильными реагентами.
- •Соединения этого ряда могут быть представлены структурой
- •Методы получения
- •Структурные особенности , - ненасыщенных карбонильных соединений
- •Химические свойства
- •Ароматические альдегиды и кетоны
- •Классификация и номенклатура
Образование солей
Следствием кислотности 1,3–дикетонов является образование ими солей при взаимодействии с активными металлами или сильными основаниями.
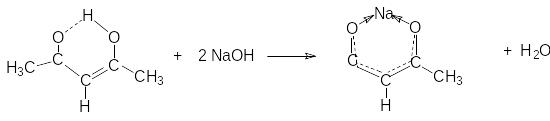
Особенно характерны соли тяжелых металлов, которые в растворах практически не диссоциируют. Благодаря этому в качестве реагентов для синтеза таких солей можно использовать соли тяжелых металлов – сильные электролиты.
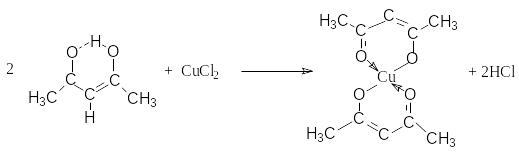
Взаимодествие с электрофильными реагентами.
Анион, ионная пара соли или енольная форма восприимчивы к действию электрофильных агентов. Примером могут быть реакции алкилирования или ацилирования. Как енол, так и анион являются амбидентными частицами. Местом электрофильной атаки в них могут быть кислородные атомы или углеродный атом между карбонильными группами (активная метиленовая группа).
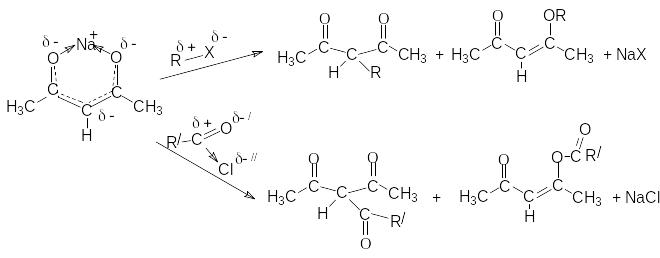
В общем случае получается смесь продуктов С- и О-алкилирования или ацилирования. В случае 1,3–дикарбонильных соединений, образующих цис–енольную форму, преимущественно образуются С-производные, так как атомы кислорода значительно блокированны ионом металла. Если обьектом электрофильного замещения являются транс- фиксированные 1,3–дикетоны, то преимущественно могут получаться продукты О- замещения.
Взаимодействие с другими электрофильными реагентами (нитрование, сульфирование, галогенирование, нитрозирование, азосочетание) может быть изображено общей схемой.
 +
-
+
-
где Е – NO, NO2, ArN2, SO3H, Cl, Br, I.
Взаимодействие с нуклеофильными реагентами.
Енольная или дикарбонильная форма 1,3–дикетонов могут быть объектами нуклеофильной атаки, причем атакующим реакционным центром в этих реакциях выступает карбонильный углерод. Если в реакциях участвуют слабые нуклеофилы (вода, спирты, тиолы), то для успешной реализации реакции используют кислотный катализ.
Примером нуклеофильной атаки является взаимодействие с аммиаком и аминами. Считается, что активной формой, реагирующей с RNH2, является дикарбонильная форма.

Результатом этих реакций является образование енаминов, стабилизированных за счет образования прочной внутримолекулярной водородной связи.
В случае реакции с гидроксиламином и гидразинами образуются гетероциклические соединения. Подробное описание этих реакций будет дано в материале по гетероциклическим соединениям.
П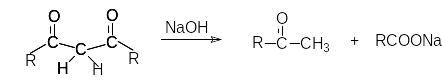 римером
другой реакции нуклеофильного замещения
является щелочной гидролиз 1,3 – дикетонов.
римером
другой реакции нуклеофильного замещения
является щелочной гидролиз 1,3 – дикетонов.
Р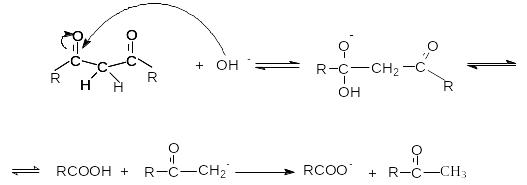 еакция
может быть представлена механизмами.
еакция
может быть представлена механизмами.
, - Непредельные альдегиды и кетоны
Соединения этого ряда могут быть представлены структурой
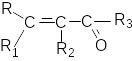
где R ,R1 ,R2 ,R3 - представляют собой алкильные группы или атом водорода.
Методы получения
1. Дегидратация альдолей, кротоновая конденсация
Альдоли - продукты альдольной конденсации, легко отщепляют воду, особенно при кислотном катализе.
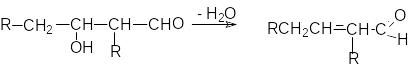
В результате дегидратации альдоля получается кротоновый альдегид, поэтому часто этот процесс называют кротонизацией.
В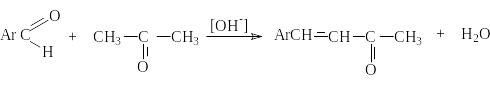 ряде реакций карбонильных соединений,
например, аренкарбальдегидов с кетонами,
продукт альдольного присоединения
выделить не удается и сразу получается
ненасыщенные соединения. Такие реакции
называют кротоновой конденсацией.
ряде реакций карбонильных соединений,
например, аренкарбальдегидов с кетонами,
продукт альдольного присоединения
выделить не удается и сразу получается
ненасыщенные соединения. Такие реакции
называют кротоновой конденсацией.
Реакции окисления алкенов и алкинов
Использование некоторых окислителей, например, CrO3 при низких температурах, позволяет селективно окислять спиртовые группы до альдегидных и кетонных:
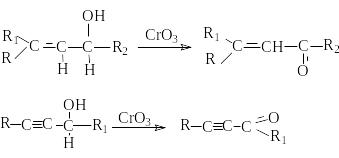
Другой вариант подобного синтеза – каталитическое окисление кислородом
![]()
