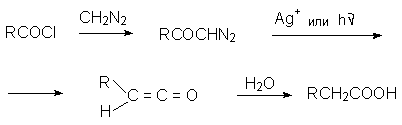- •Лекция №47-48 диазосоединения
- •Ароматические диазосоединения Классификация и номенклатура
- •Соединения, содержащие ионную связь (соли диазония):
- •Методы получения солей арендиазония
- •Механизм реакции диазотирования
- •Условия проведения реакции диазотирования
- •Физические свойства и строение
- •Химические свойства
- •1. Равновесия между различными формами диазосоединений в водных растворах. Образование и строение диазотатов
- •2. Реакции солей арендиазония
- •Замещение диазогруппы на иод
- •Реакции, идущие без выделения азота
- •Строение и физические свойства
- •Методы получения
- •Химические свойства
- •Реакции с протонными кислотами
- •2. Реакции с карбонильными соединениями
- •Реакции биполярного присоединения
- •Фотохимическое и термическое разложение
Строение и физические свойства
Диазоалканы – газообразные или жидкие вещества желтого цвета, взрывоопасные и ядовитые. Газообразный диазометан разлагается со взрывом при комнатной температуре при соприкосновении со шлифованной или шероховатой поверхностью, поэтому его используют и хранят в виде раствора в эфире при низких температурах.
Д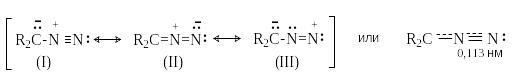 иазоалканы
имеют структуру внутренних солей,
которая может быть представлена набором
резонансных структур.
иазоалканы
имеют структуру внутренних солей,
которая может быть представлена набором
резонансных структур.
Длина связи N-N близка к тройной, т.е. структура диазоалканов близка к структуре биполярного иона (I).
П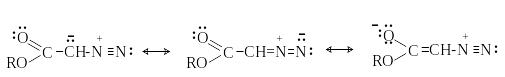 роизводные
диазоалканов с электроноакцепторными
группами - -диазоэфиры,
-диазокарбонильные
соединения более стабильны за счет
делокализации заряда с участием
карбонильной группы.
роизводные
диазоалканов с электроноакцепторными
группами - -диазоэфиры,
-диазокарбонильные
соединения более стабильны за счет
делокализации заряда с участием
карбонильной группы.
Методы получения
Д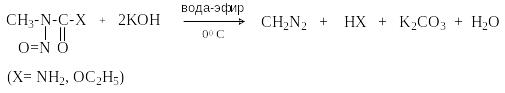 иазоалканы
не могут быть получены нитрозированием
первичных аминов, так как образующиеся
алкандиазониевые соли спонтанно
разлагаются с выделением азота (см.
лек.№42). Диазометан получают обработкой
N-нитрозометилмочевины
или N-нитрозометилуретана
щелочью.
иазоалканы
не могут быть получены нитрозированием
первичных аминов, так как образующиеся
алкандиазониевые соли спонтанно
разлагаются с выделением азота (см.
лек.№42). Диазометан получают обработкой
N-нитрозометилмочевины
или N-нитрозометилуретана
щелочью.
П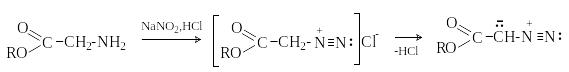 ри
взаимодействии -аминоэфиров
с азотистой кислотой дезаминирования
не происходит. Из -положения,
активированного карбонильной группой,
отщепляется протон и образуются
-диазоэфиры.
ри
взаимодействии -аминоэфиров
с азотистой кислотой дезаминирования
не происходит. Из -положения,
активированного карбонильной группой,
отщепляется протон и образуются
-диазоэфиры.
Нитрозированием -аминокетонов получают -диазокетоны. Другой способ получения -диазокетонов – ацилирование диазометана ацилгалогенидами (см. далее).
Химические свойства
Реакции с протонными кислотами
Д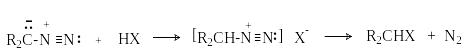 иазоалканы
являются С-основаниями и легко реагируют
с соединениями, содержащими кислый
водород. Реакция протекает через стадию
протонирования диазоалкана с образованием
нестабильного катиона алкандиазония,
который реагирует с нуклеофилом с
выделением азота.
иазоалканы
являются С-основаниями и легко реагируют
с соединениями, содержащими кислый
водород. Реакция протекает через стадию
протонирования диазоалкана с образованием
нестабильного катиона алкандиазония,
который реагирует с нуклеофилом с
выделением азота.
Таким образом диазометан количественно реагируют с гидроксильной группой карбоновых кислот и фенолoв. Обладающие меньшей кислотностью спирты реагируют при катализе эфиратом трехфтористого бора.
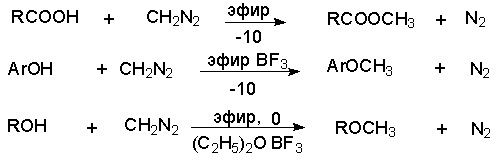
-Диазоэфиры реагируют аналогично, но в силу меньшей основности менее реакционноспособны.
2. Реакции с карбонильными соединениями
Диазоалаканы как нуклеофилы присоединяются по карбонильной группе альдегидов и кетонов. Менее реакционноспособные -диазоэфиры реагируют только с альдегидами. Дальнейшие превращения приводят в случае альдегидов к метилкетонам, из кетонов образуются их гомологи. В обоих случаях побочно образуются оксираны.
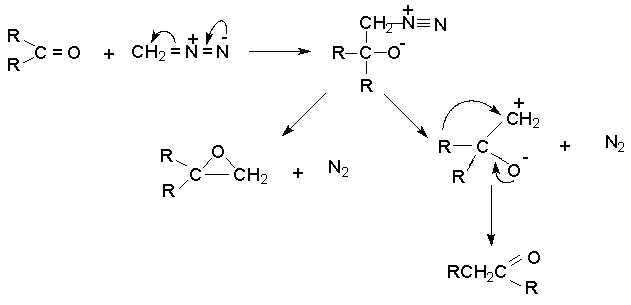
Реакция имеет препаративное значение для синтеза некоторых циклических кетонов как метод расширения цикла.
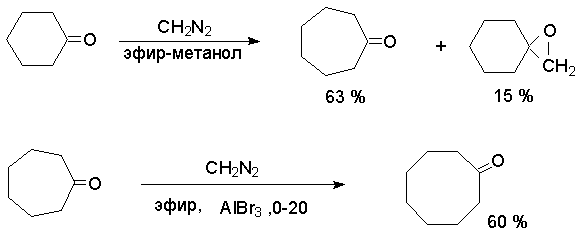
Взаимодействие диазометана с хлорангидридами приводит к -диазокетонам.
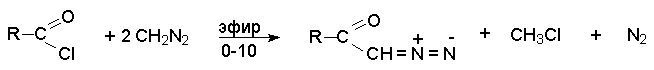
В этом случае от продукта присоединения диазометана к карбонильному атому углерода отщепляется не азот, хлороводород и образуется относительно устойчивый диазокетон. Избыток диазометана необходим для связывания образующегося HCl.
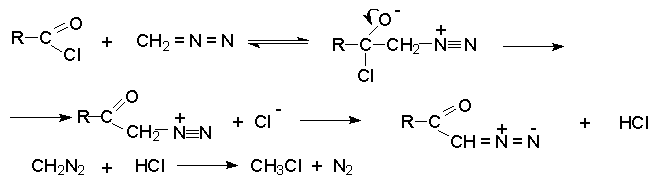
-Диазокетоны являются важными промежуточными продуктами. Они могут быть восстановлены в аминокетоны, превращены в -галогенкетоны действием HНal. При катализе ионами серебра или при облучении диазокарбонильные соединения превращаются в кетены (перегруппировка Вольфа). Эта перегруппировка лежит в основе общего метода синтеза карбоновых кислот по Арндту - Эйстерту.