
- •Методы получения
- •3) Гидрирование алкенов и алкинов
- •5) Восстановление карбонильных соединений:
- •6) Реакция Вюрца
- •7) Реакция галогеналканов с диалкилкупратами лития
- •8) Электролиз водных растворов солей карбоновых кислот
- •9) Сплавление солей карбоновых кислот со щелочами
- •Физические свойства и строение
- •Конформации этана
- •Энергетическая диаграмма конформационных превращений этана
- •Энергетическая диаграмма конформационных превращений бутана
- •Химические свойства
- •Хлорирование метана
- •Хлорирование гомологов метана. Региоселективность реакции
- •Увеличение стабильности свободных радикалов
- •Температура, 0С
- •Бромирование алканов
- •2) Сульфохлорирование
- •3) Нитрование
- •4) Окисление алканов
- •Инициирование цепи:
- •Обрыв цепи:
- •Антиоксиданты («ловушки» свободных радикалов) – это вещества, которые обрывают цепь в реакциях свободно-радикального
- •5) Термолиз алканов
- •Инициирование цепи:
- •Перенос цепи:
- •• Каталитический крекинг (изомеризация)
А Л К А Н Ы
|
Углеводород |
Название |
Радикал |
Название |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH 4 |
Метан |
|
|
CH3 |
Метил |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3CH 3 |
Этан |
CH3CH 2 |
Этил |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH 3CH 2CH3 |
Пропан |
CH3CH 2 CH 2 |
Пропил |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
CH3- |
|
CH-CH3 |
Изопропил |
|
||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3CH 2CH 2CH3 |
н-Бутан |
CH3CH 2 CH 2CH 2 |
н-Бутил |
|
||||||||||
|
CH3- |
|
CH-CH2-CH3 |
втор-Бутил |
|||||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
CH3- |
|
CH-CH3 |
Изобутан |
CH3- |
|
CH-CH2- |
Изобутил |
|
||||||
|
|
|
|
||||||||||||
|
|
|
CH |
|
|
|
|
|
CH3 |
|
|
||||
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
трет-Бутил |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
CH3-C- |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
||

4 3 2 1
CH3CHCH2CH2 CH3
CH3
3 2 1
CH3CCH2
CH3
Изопентил 3-Метилбутил
Неопентил 2,2-Диметилпропил
Методы получения
1) Гидрирование оксидов углерода
4000C [Ni]
CO2 + 4H2  CH4 + 2H2O
CH4 + 2H2O
3000C [Co]
nCO + (2n+1)H2  CnH2n+2 + nH2O
CnH2n+2 + nH2O
синтез-газ
2) Гидрирование угля
4500C, 250 атм, [Fe]
nC + (n+1)H2  CnH2n+2
CnH2n+2

3) Гидрирование алкенов и алкинов
RCH=CH |
+ H |
cat, t, p |
RCH2CH3 |
|
|||
2 |
2 |
|
|
cat, t, p
RC CH + 2H2
CH + 2H2  RCH2CH3
RCH2CH3
cat: Ni, Pt, Pd
4) Гидрогенолиз галогеналканов
RX + H2 |
cat, t, p |
RH + HX |
|
RI + HI  RH + I2
RH + I2
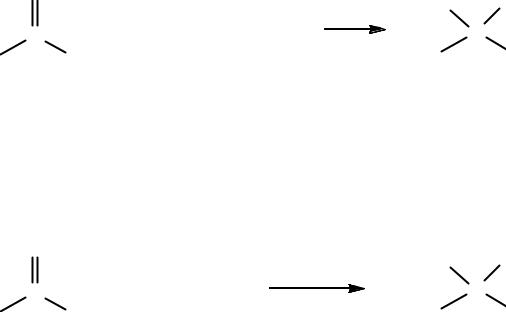
5) Восстановление карбонильных соединений:
• |
по Клемменсену |
|
|
|
|
|
O |
|
H |
|
H |
|
|
|
|
||
|
C |
+ 2Zn + |
4HCl |
C |
+ 2ZnCl2 + H2O |
R |
R |
амальгама |
R |
|
R |
• по Кижнеру-Вольфу
O |
[KOH], t |
H |
H |
|
|||
C |
+ NH2NH2 |
C |
+ N2 + H2O |
R |
R |
R |
R |
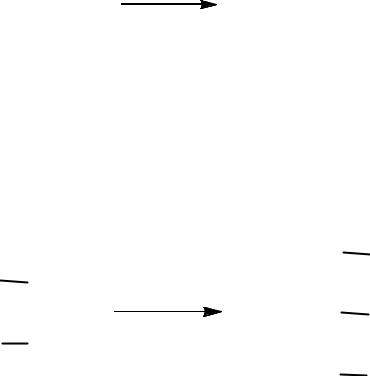
6) Реакция Вюрца
|
t |
2RX + 2Na |
R-R + 2NaX |
Х - галоген |
симметричный |
|
алкан |
Перекрестная реакция Вюрца
R1 |
|
R |
R |
|
X |
Na |
|
||
R2 |
X |
R1 |
R1 |
|
R2 |
R2 |
|||
|
|
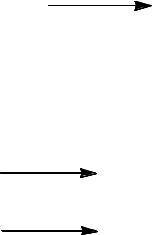
7) Реакция галогеналканов с диалкилкупратами лития
R2CuLi + R/X |
R-R/ + RCu + LiX |
несимметричный
алкан
RX |
+ |
2Li |
RLi + |
LiX |
2RLi |
+ |
CuI |
R2CuLi |
+ LiI |
8) Электролиз водных растворов солей карбоновых кислот
|
электролиз |
2RCOONa + 2H O |
R-R + 2CO2 + 2NaOH + H2 |
2 |
|
симметричный
алкан
катод: |
2H O + 2e |
H2 + 2OH- |
|
2 |
|
анод: |
2RCOO- - 2e |
2RCOO |
|
2RCOO |
2R + 2CO2 |
|
2R |
R-R |

9) Сплавление солей карбоновых кислот со щелочами
|
t |
RCOONa + NaOH |
R-H + Na2CO3 |
10) Протолиз реактивов Гриньяра
RMgX + H2O |
H + MgOHX |
RMgX + D2O  R-D + MgODX
R-D + MgODX
RX + Mg  R-MgX
R-MgX

Физические свойства и строение
Алканы С1 – С4 - газы С5 – С15 - жидкости
С16 и выше - твердые вещества
CH3CH2CH2CH2CH3 |
CH3 |
|
CHCH2CH3 |
|
|||
|
|
CH3 |
|
н-пентан |
изопентан |
||
Ткип.= 360С |
Ткип.= 280С |
||
CH3
CH3CCH3 CH3
неопентан
Ткип.= 90С

Конформации этана
заслоненная (1%) |
заторможенная (99%) |
торсионный угол
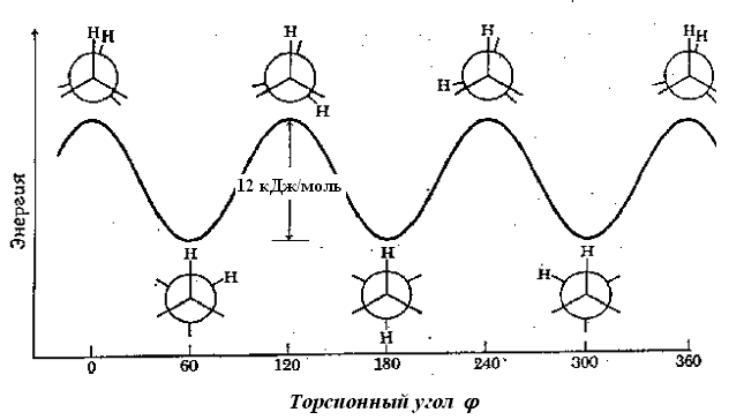
Энергетическая диаграмма конформационных превращений этана
H3C CH3
полностью
заслоненная
синпланарная (sp)
CH3
CH3
заторможенная
антипланарная (ap)
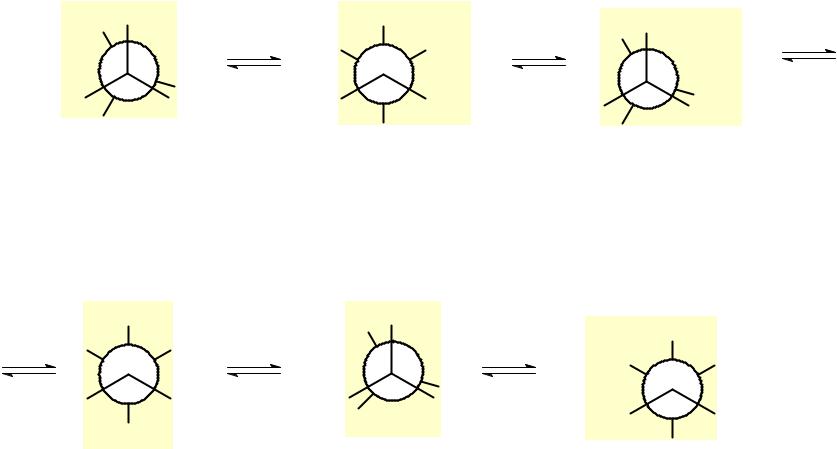
Конформации бутана
CH3 |
CH3 |
|
CH3 |
|
CH3 |
скошенная (гош) (+)cинклинальная (+sc)
CH3
CH3
частично
заслоненная (-)антиклинальная (-ac)
частично
заслоненная
(+)антиклинальная (+ac)
CH3
H3C
скошенная (гош) (-)cинклинальная (-sc)
