
- •Пищевые белки как источник аминокислот. Качественный состав и биологическая ценность пищевых белков.
- •Динамическое состояние белков в организме. Нормы белка в питании. Азотистый баланс.
- •П ереваривание белков
- •Протеиназы пищеварительного тракта (общая характеристика и классификация)
- •Минеральный состав желудочного сока. Роль соляной кислоты в процессах пищеварения.
- •Виды кислотности желудочного сока, определение и расчет всех видов кислотности по михаэлису.
- •Проферменты пищеварительных протеиназ, механизм превращения в ферменты. Субстратная специфичность протеиназ.
- •Желудочные протеиназы: пепсин, гастриксин, их роль в переваривании белков.
- •Методы количественного определения пепсина.
- •Химический состав панкреатического и кишечного соков. Роль панкреатических и кишечных протеиназ в переваривании белков.
- •Б иохимические механизмы регуляции пищеварения, гормоны желудочно-кишечного тракта. Всасывание аминокислот.
- •Общая схема источников и путей расходования аминокислот в тканях. Экзогенный и эндогенный пул аминокислот
- •Трансаминирование, химизм. Трансаминазы, их специфичность. Роль витамина в6 в трансаминировании.
- •Биологическая роль реакций трансаминирования
- •Определение трансаминаз в сыворотке крови.
- •Д езаминирование аминокислот
- •Окислительное дезаминирование химизм. Роль глутаматдегидрогеназы. Биологическая роль окислительного дезаминирования аминокислоты.
- •Непрямое дезаминирование аминокислот, понятие, стадии, биологическое значение.
- •Декарбоксилирование аминокислот, химизм, ферменты, субстратная специфичность декарбоксилаз.
- •Биогенные амины, механизм образования, влияние на процессы метаболизма и физиологические функции. Окисление биогенных аминов.
- •Образование катехоламинов и гамк, функции аминов.
- •Понятие о свободном амином азоте. Принцип метода определения, диагностическое значение.
- •Трансметилирование. Метионин и s-аденозилметионин. Роль метионина в биосинтезе биологически важных соединений, в реакциях обезвреживания.
- •Тетрагидрофолиевая кислота и ее роль в синтезе и переносе одноуглеродных радикалов.
- •Обмен фенилаланина и тирозина. Пути превращения в норме.
- •Врожденные нарушения обмена ароматических аминокислот. Методы предупреждения, диагностики и лечения врожденных нарушений обмена фенилаланина и тирозина.
- •Наследственные нарушения обмена других аминокислот.
- •Понятие о скрининг-тестах.
- •Качественное открытие фенилпировиноградной и гомогентезиновой кислот.
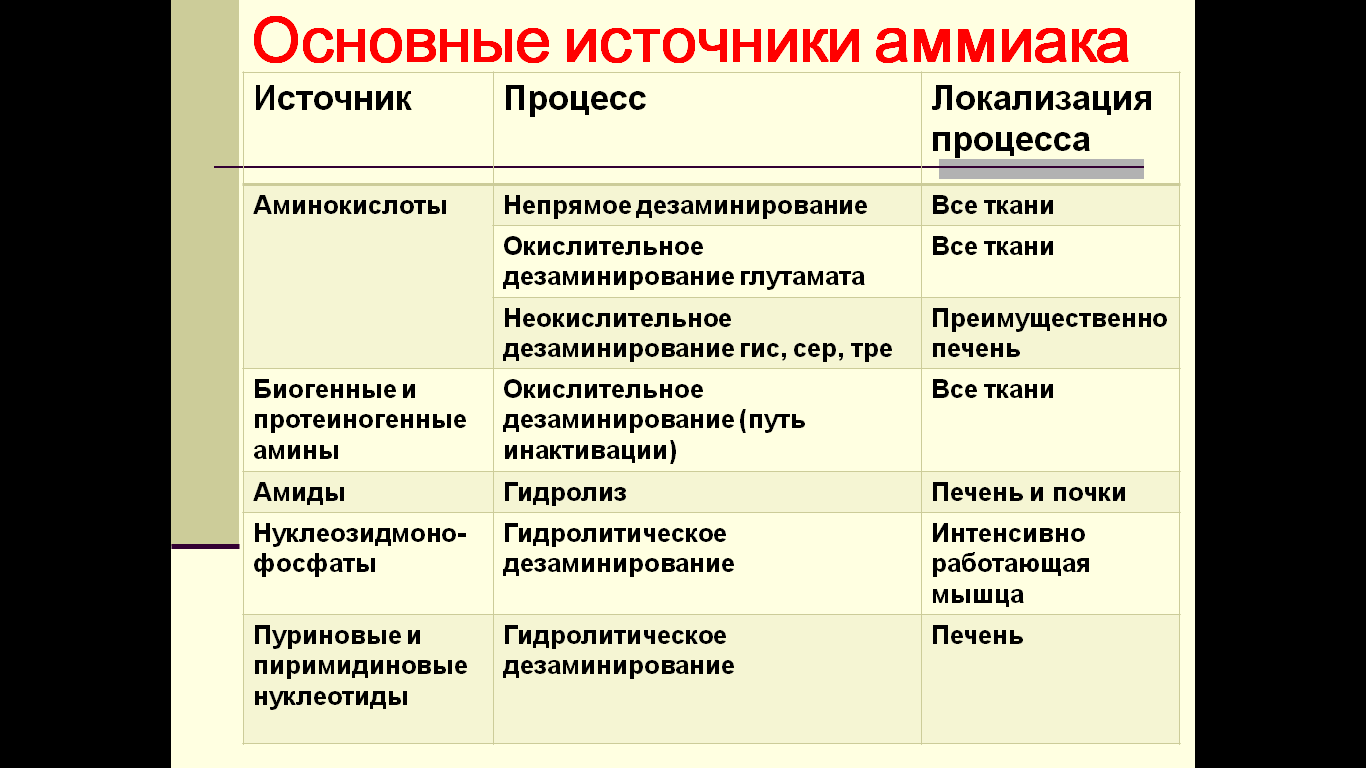
- •Конечные продукты азотистого обмена. Основные источники аммиака в организме.
- •О безвреживание аммиака в месте образования в организме.
- •Транспортные формы обезвреженного аммиака
- •Г люкозо-аланиновый цикл
- •Синтез мочевины как путь окончательного обезвреживания аммиака. Химизм, ферменты, энергетика. Биологический смысл цикла мочевинообразования, связь с цтк.
- •Нарушения синтеза и выведения аммиака. Причины уремии.
- •Патология азотистого обмена.
- •Определение мочевины в сыворотке крови. Диагностическое значение.
- •Креатин и креатинин. Количественное определение креатинина, роль, диагностическое значение.
- •Образования аммонийных солей
Конечные продукты азотистого обмена. Основные источники аммиака в организме.
Аммиак в организме образуется в результате дезаминирования аминокислот, биогенных аминов и нуклеотидов. Часть аммиака образуется в кишечнике в результате действия бактерий на пищевые белки (гниение). Концентрация аммиака в крови в норме – 0,4-0,7мг/л. Это токсичное соединение, поэтому аммиак не накапливается, а вступает в реакцию с глутаминовой или аспарагиновой кислотами с образованием индифферентной транспортной формы – глутамина или аспарагина.
+NН3
 НООС-(СН2)2-СН-СООН
Н 2NОС-(СН2)2-СН-СООН
НООС-(СН2)2-СН-СООН
Н 2NОС-(СН2)2-СН-СООН

NН2 АТФ NН2
-Н 2О
глутаминовая кислота глутамин
+NН3
 НООС-СН2-СН-СООН
Н2NОС-СН2-СН-СООН
НООС-СН2-СН-СООН
Н2NОС-СН2-СН-СООН
 АТФ
АТФ
NН2 -Н 2О
NН2
аспарагиновая кислота аспарагин
О безвреживание аммиака в месте образования в организме.

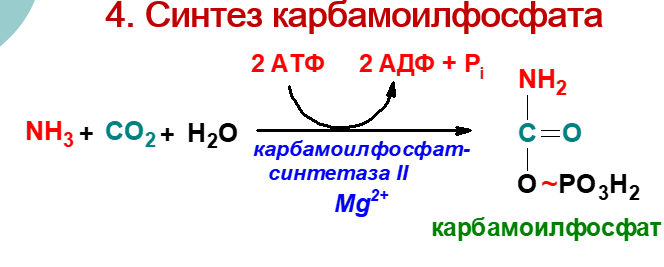
В почках глутамин под влиянием глутаминазы расщепляется с образованием аммиака, идущего на нейтрализацию кислых соединений с образованием аммонийных солей. Этот процесс является одним из механизмов регуляции кислотно-щелочного равновесия в организме и сохранения важнейших катионов (Na+, K+) для поддержания осмотического давления. Глутамин – основной донор азота в организме. Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосахаров, белков, глюкозы. Также источниками образования аммиака служат процессы:
дезаминирования биогенных аминов;
распад пиримидиновых оснований (урацил, тимин, цитозин);
дезаминирования аминокислот;
дезаминирования пуриновых оснований (гуанина и аденина).
Пути использования аммиака в организме:
Синтез аминокислот из соответствующих кетокислот:
АТФ
 СН3-С-СООН
+ NН3
СН3-СН-СООН
СН3-С-СООН
+ NН3
СН3-СН-СООН
О NН2
ПВК аланин
Синтез аммонийных солей в почках.
Синтез пуриновых и пиримидиновых нуклеотидов.
Синтез мочевины – основной путь обезвреживания аммиака.
Транспортные формы обезвреженного аммиака
Глутаминовая кислота
Амиды аминокислот (аспарагин и глутамин)
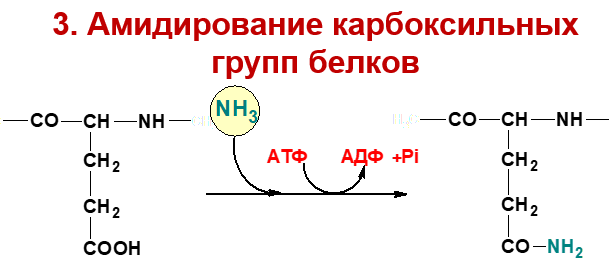
Амидированные белки
Транспортными формами аммиака из тканей в печень являются глутамин и аланин, в меньшей степени аспарагин и глутамат, некоторое количество аммиака находится в крови в свободном виде. Глутамин и аланин являются наиболее представленными, их доля среди всех аминокислот крови составляет до 50%. Большая часть глутамина поступает от мышц и нервной ткани, аланин переносит аминный азот от мышц и стенки кишечника.
