
Задачи Крюкова / Кинетика 5
.docxЗадача 1.
Разложение пербората натрия
NaBO3 + H2O → NaH2BO3 + 1/2O2
реакция первого порядка. Константы скорости реакции при 303 и 308 К соответственно равны 2.2·10-3 и 4.1·10-3 мин-1. Вычислите энергию активации и время, в течение которого при 313 К разложится 99.99% пербората натрия.
Решение:
Вычислим энергию активации:

Рассчитаем константу скорости при температуре 313 К:

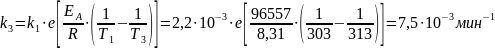
Вычислим время, в течение которого при 313 К разложится 99.99% пербората натрия:
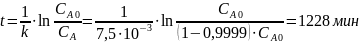
Ответ:
 ;
;
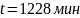
Задача 2.
При определённой температуре 0.01N раствор этилуксусного эфира омыляется 0.002N раствором NaOH за 23 мин на 10%. Через сколько минут он будет омылён до такой же степени 0.005N раствором щёлочи, если скорость омыления описывается кинетическим уравнением реакции второго порядка.
Решение:
Рассчитаем константу скорости реакции второго порядка с разными начальными концентрациями реагирующих веществ:
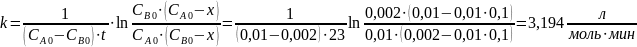
Вычислим время, за которое раствор будет омылён до такой же степени 0.005N раствором щёлочи:

Ответ: 7,38 мин
Задача 3.
Изучая кинетику некоторой реакции А → продукты, обнаружено, что при начальной концентрации реагента А, равной 4.86·10-3 моль/л, 50%-ная конверсия достигалась через 399 сек, при начальной концентрации, равной 2.28·10-3 моль/л, – через 696 сек. Определите порядок реакции и константу скорости реакции.
Решение:
Определим порядок реакции аналитическим способом:

Определим константу скорости реакции второго порядка при t = 399 сек, CA0 = 4,86∙10-3:

Ответ: n = 1,735 ≈ 2; k
=

