
Задачи Крюкова / Кинетика 16
.docx
Дано:
MA
=
0,142 кг/моль
МВ
=
0,068 кг/моль

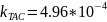 л∙моль-1∙с-1
P
= 0,8
Т = 291 К
RА
= 2,64*10-8
см
RВ
= 2,74*10-8
см
л∙моль-1∙с-1
P
= 0,8
Т = 291 К
RА
= 2,64*10-8
см
RВ
= 2,74*10-8
см
Решение:
Согласно
теории активных соударений, константа
находится по следующей формуле:
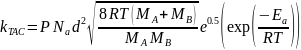
Выразим и найдем энергию активации:
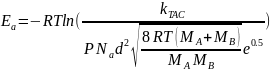
Ea=-8,31*291*ln(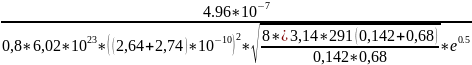 )=
)=
= 80865Дж
Ответ: Ea = 80865 Дж
2.Сколько граммов уксусной кислоты разложится по фотохимической реакции СН3СООН → СН4 + СО2 при поглощении кислотой 1 кДж электромагнитного излучения с длиной волны λ=2000 нм. Квантовый выход равен 0.5
Дано:
Е = 1000 Дж
λ=2000
нм
=
0,5
М = 0,06 кг/моль

Воспользуемся следующими формулами:
Квантовый выход фотохимической реакции:
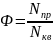
Количество поглощенных квантов:
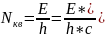
Количество моль прореагировавшего вещества:
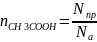
Масса прореагировавшего вещества:
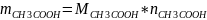
Откуда масса прореагировавшей уксусной кислоты:
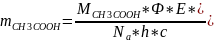
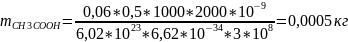
Ответ:
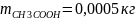
3. Для реакции разложения оксида азота 2NO → N2 + O2 константы скорости: при Т1=1620К и при Т2=1525К составляют k1=0.0108 моль/(л·с·атм2) и k2=0.003 моль/(л·с·атм2), соответственно. Используя уравнение теории переходного состояния, рассчитайте ΔН≠ и ΔS≠ реакции при температуре 1527К.
Дано:
Т1=1620К
k1=0.0108
моль/(л·с·атм2)
Т2=1525К
k2=0.003
моль/(л·с·атм2)
Т3=1527К

Запишем
уравнение Арениуса:
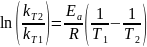
Выразим и найдем значение энергии активации:
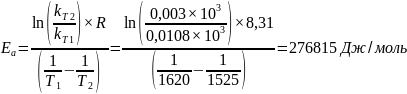
Найдем ΔН≠:
ΔН≠1527=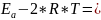 276815-2*8,31*1527 = 251436 Дж/моль
276815-2*8,31*1527 = 251436 Дж/моль
Используя уравнение Арениуса найдем константу скорости при Т=1527К:
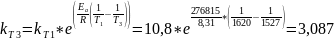
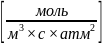
Выразим
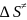 из уравнения константы скорости:
из уравнения константы скорости:
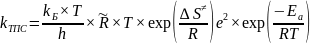
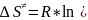 )
)
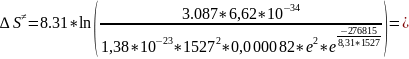 -67,077
Дж/(моль*К)
-67,077
Дж/(моль*К)
Ответ: ΔН≠ = 251,436 кДж, = -67,077 Дж/(моль*К)
