
Прирост содержания кальция и истощение запасов атф
Уже через несколько секунд после начала глубокой ишемии содержание макроэргических фосфатов (аденозинтрифосфата и креатинфосфата) начинает уменьшаться. Приблизительно через 1 мин содержание креатинфосфата может снизиться более чем на 80% [18]; через 15 мин исчезает 65% общего содержания АТФ в ткани и 55% всех адениннуклеотидов [19]. Через 40 мин ишемии запасы макроэргических фосфатов практически полностью истощаются [18], и ткань необратимо повреждается в такой степени, что уже не способна восстановиться при реперфузии [19, 20]. Согласно результатам работы [21], восстановление подачи кислорода не приведет к развитию клеточных аномалий, если уровень АТФ при ишемии не снижался ниже 5 мкмоль на 1 г сухой массы. И наоборот, если уровень АТФ в ткани падает приблизительно до 2 мкмоль/г сухой массы, реоксигенация или реперфузия ускоряют начавшийся процесс разрушения мембран. По-видимому, истощение запасов макроэргических фосфатов и перегрузка кардиомиоцитов ионами Са2+ взаимосвязаны, однако такое истощение запасов предшествует началу увеличения тканевого содержания Са2+. Например, как показано в работах [1, 20, 21], реперфузия после относительно коротких периодов ишемии не сопровождается суммарным приростом содержания кальция, несмотря на истощение запасов АТФ и КФ. Однако после длительных периодов ишемии (более 40 мин) реперфузия практически всегда приводит к повышению тканевого содержания кальция, если не предпринять специальных защитных мер. В таком случае развитие процесса перегрузки клеток кальцием может быть представлено последовательностью событий, показанной на схеме 18.1. Таким образом, вскоре после начала эпизода гипоксии или ишемии тканевые запасы АТФ и КФ снижаются настолько, что концентрация ионов Са2+ в цитозоле может возрасти без какого бы то ни было увеличения тканевого содержания кальция или же он будет очень небольшим. Такое повышение цитоплазматической концентрации ионов Са2+ может быть связано с ингибированием Са2+-АТФазы саркоплазматического ретикулума, Са2+-АТФазы сарколеммы и (Na+, К+-АТФазы в результате истощения запасов АТФ. Угнетение Nа+/К+-насоса объясняет раннее повышение тканевого содержания ионов Na+ в этих условиях [1], что в свою очередь может ускорить вход ионов Са2+ в обмен на ионы Na+. Повышение концентрации ионов Na+ способствует также освобождению ионов Са2+ из митохондрий [17]. Все эти события приводят к повышению цитоплазматической концентрации ионов Са2+, после чего может развиться вторая фаза ишемической реакции, включающая активацию Са2+-чувствительных протеаз и фосфолипаз [22, 23] и вызывающая, по-видимому, необратимые изменения структуры и целостности сарколеммного комплекса. При достижении этой стадии можно ожидать быстрого массированного входа ионов Са2+, похожего на описанный первоначально в работе [1], а также потерю внутриклеточных компонентов, включая адениновые основания, являющиеся предшественниками синтеза АТФ [24].
Схема 18.1. Возможная последовательность событий, запускаемых гипоксией или ишемией
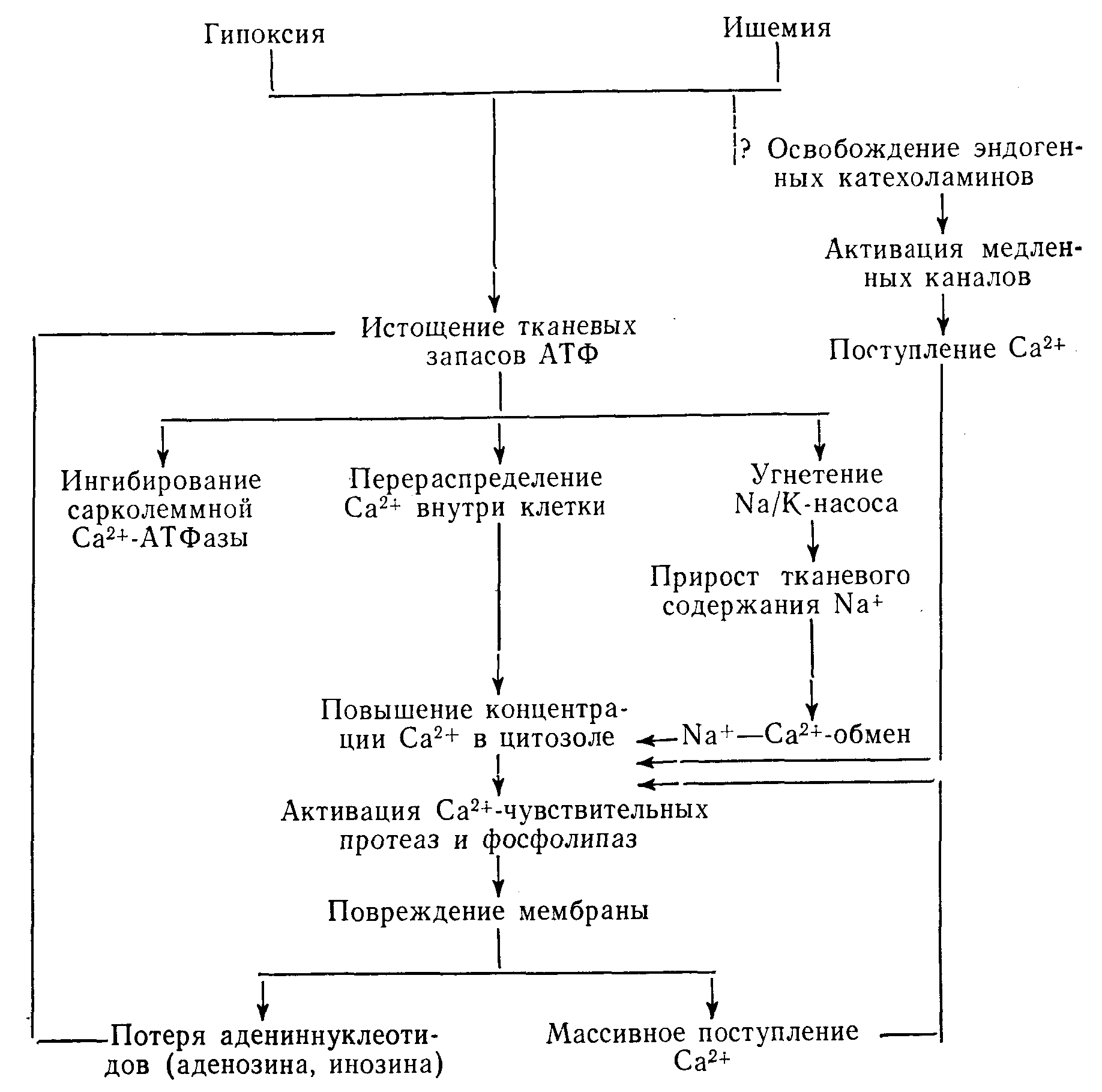
Следовательно, перегрузка ишемического миокарда ионами Са2+ представляет собой сложное явление, обусловленное истощением запасов макроэргических фосфатов на ранней стадии ишемии. Первоначально повышение концентрации Са2+ в цитоплазме может сопровождаться увеличением общего содержания их в ткани. Некоторая часть Са2+ может поступать в миоплазму в обмен на ионы Na+; кроме того, Са2+ может выходить из митохондрий, а также освобождаться из саркоплазматического ретикулума в ответ на быстрое поглощение Н+ [25]. Поступающий Са2+ будет оставаться в цитозоле, так как вследствие истощения клеточных запасов субстратов нарушается работа различных АТФаз, ответственных за поддержание низкой миоплазматической концентрации Са2+. При достижении некоторого критического уровня концентрации Са2+ в цитозоле можно ожидать практически мгновенного разрушения сарколеммы и других липидобелковых мембран в результате активации эндогенных Са2+-активируемых фосфолипаз и протеаз. При достижении этой стадии уже невозможно предотвратить поступление Са2+ из внеклеточного пространства внутрь клеток. Поэтому при реперфузии раствором, содержащим ионы Ca2+, мы можем ожидать дальнейшего развития повреждений, вызванных ишемией.
