- •Передмова
- •Загальні вказівки щодо вивчення дисципліни
- •Змістовий модуль і Ациклічні вуглеводні та їхні похідні
- •Теорія будови органічних сполук. Ізомерія. Номенклатура
- •1.1 Загальна характеристика органічних сполук
- •Питання для самоперевірки
- •1.2 Теорія хімічної будови органічних сполук о.М. Бутлерова
- •Питання для самоперевірки
- •1.3 Класифікація органічних сполук
- •Питання для самоперевірки
- •1.4 Ізомерія органічних сполук
- •Питання для самоперевірки
- •1.5 Номенклатура органічних сполук
- •Питання для самоперевірки
- •1.6 Типи реакцій за участю органічних сполук
- •Питання для самоперевірки
- •Тема 2 Насичені та ненасичені вуглеводні аліфатичного ряду: алкани, алкени, алкіни, алкадієни
- •2.1 Насичені вуглеводні (алкани)
- •Питання для самоперевірки
- •2.2 Ненасичені вуглеводні
- •2.2.1 Алкени (або олефіни, або етиленові вуглеводні)
- •Питання для самоперевірки
- •2.2.2 Алкадієни (дієнові вуглеводні)
- •Питання для самоперевірки
- •2.2.3 Алкіни (ацетиленові вуглеводні)
- •Питання для самоперевірки
- •Тема 3 Природні джерела вуглеводнів. Переробка нафти. Найважливіші нафтопродукти. Асфальти, бітуми, їх використання в будівництві
- •Питання для самоперевірки
- •Тема 4 Галогенопохідні вуглеводнів
- •Питання для самоперевірки
- •Змістовий модуль іі. Кисневмісні органічні сполуки
- •Тема 5 Спирти (алканоли, алкоголі)
- •Питання для самоперевірки
- •Тема 6 Аліфатичні альдегіди і кетони
- •Питання для самоперевірки
- •Тема 7 Карбонові кислоти та їхні похідні
- •7.1 Карбонові кислоти
- •Питання для самоперевірки
- •7.2 Складні ефіри (естери). Жири та мила
- •Питання для самоперевірки
- •Змістовий модуль ііі Ароматичні та високомолекулярні сполуки
- •Тема 8 Ароматичні вуглеводні та їхні похідні
- •Питання для самоперевірки
- •Тема 9 Феноли
- •Питання для самоперевірки
- •Тема 10 Високомолекулярні сполуки. Органічні полімерні матеріали в будівництві
- •Питання для самоперевірки
- •Загальні вказівки щодо виконання контрольної роботи
- •Перший тип вправ контрольної роботи
- •Другий тип вправ контрольної роботи
- •Третій тип вправ контрольної роботи
- •Четвертий тип вправ контрольної роботи
- •П’ятий тип вправ контрольної роботи
- •Запитання до контрольної роботи
- •Список рекомендованої літератури
- •Навчальне видання
- •Вправи та завдання
- •З органічної хімії
- •Навчально-методичний посібник
- •Роботу до друку рекомендував ю.В. Журавльов
1.3 Класифікація органічних сполук
В основі класифікації органічних сполук лежить будова вуглецевого ланцюга і наявність типових угрупувань атомів (функціональних груп), які визначають певні хімічні властивості сполук. Залежно від будови вуглецевого ланцюга органічні сполуки поділяються на ациклічні та циклічні (рис. 1.1).
Органічні сполуки
Ациклічні Циклічні
(аліфатичні)
Карбоциклічні Гетероциклічні
Аліциклічні Ароматичні
Рисунок 1.1 – Класи органічних сполук
Ациклічними є сполуки, молекули яких мають відкриті (незамкнені) вуглецеві ланцюги: прямі або розгалужені:
— С —
— С — С — С — С —
— С — С — С —
прямий ланцюг розгалужений ланцюг
Ациклічні сполуки називають аліфатичними або сполуками жирного ряду. Їх поділяють на насичені та ненасичені. До насичених відносять такі, які мають лише одинарні С–С зв’язки. В молекулах ненасичених сполук знаходяться подвійні С = С або потрійні С С зв’язки:
СН3 – СН2 – СН3 СН2 = СН – СН3 СН С – СН3 . насичена аліфатична сполука ненасичені аліфатичні сполуки
Циклічними називають сполуки, молекули яких складаються з замкнених у кільця вуглецевих ланцюгів. Циклічні сполуки поділяють на карбоциклічні і гетероциклічні. Карбоциклічні мають цикл, що побудований лише з атомів вуглецю, а гетероциклічні містять у циклі поряд з атомами вуглецю різні за природою елементи (переважно кисню, азоту, сірки), вони бувають насичені і ненасичені.
О НС–СН СН
Н2С СН2 НС СН
НС СН
Н2С СН2 О НС СН
О N
гетероциклічна насичена гетероциклічні ненасичені сполуки
сполука
Карбоциклічні сполуки, в свою чергу, поділяються на аліциклічні (аліфатичні циклічні), які бувають насиченими і ненасиченими, та на ароматичні. Ароматичні сполуки характеризуються наявністю в молекулі специфічного циклічного угрупування з шести вуглецевих атомів – бензольного ядра. Для аліциклічних сполук така бензольна структура не характерна. Нижче наведені приклади аліциклічних та ароматичних сполук.
СН2 СН–СН
Н2С – СН2 Н2С –СН2 Н2С СН2 НС СН
СН2 Н2С СН2 Н2С СН НС СН
СН2 СН СН–СН
насичені аліциклічні сполуки ненасичені аліциклічні сполуки
СН СН3
 НС
СН
НС
СН
НС СН
СН
бензол ароматичні сполуки
Ациклічні й циклічні сполуки поділяються на класи залежно від наявності тих чи інших функціональних груп. Функціональна група – це угрупування різних атомів, які визначають хімічні властивості сполуки. Наприклад, карбоксильна функціональна група визначає властивості будь-якої сполуки як кислоти, а гідроксильна група – як спирту.
Вихідним класом за такої класифікації є сполуки вуглецю з воднем – вуглеводні. Наприклад, СН4 – метан, С2Н4 – етилен, С2Н2 – ацетилен. Шляхом заміщення атома водню в молекулі вуглеводню на функціональну групу можна перейти до будь-якого класу сполук.
Будь-який клас органічних сполук можна зобразити загальною формулою R – X, де Х – функціональна група, R – радикал (залишок вуглеводню, який утворюється, якщо від молекули відняти один атом водню). Наприклад:
СН4 – метан; СН3 – радикал «метил»;
С2Н6 – етан; С2Н5 – радикал «етил»;
С3Н8 – пропан; С3Н7 – радикал «пропіл».
Найважливіші класи органічних сполук наведені в таблиці 1.1.
Таблиця 1.1 – Класифікація основних органічних сполук за функціональною групою
Клас сполук |
Функціональні групи |
|||
Назва |
Загальна формула |
Приклад сполук |
Назва |
Формули |
Вуглеводні |
СnHm або R–H
|
CH4, C2H6, C2H2, C6H6 |
—
|
— |
Галогенопохідні вуглеводнів |
R-Hаl |
CH3Cl, C2H5Br, C2H4Cl2 |
Галогени |
–Hal (–F, –Cl, –Br, –I) |
Спирти, феноли |
R – OH |
CH3OH, C6H5OH |
Гідроксиль-на(гідроксил) |
– OH |
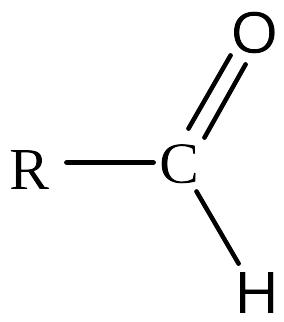
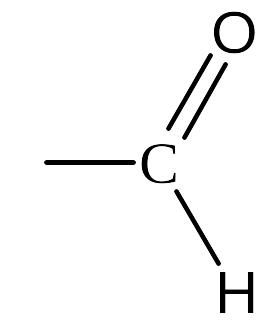
Альдегіди |
|
|
Альдегідна |
|
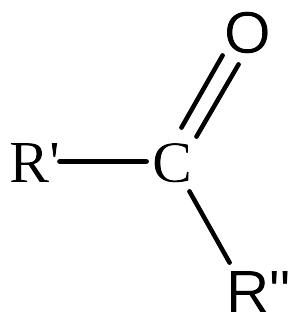
Кетони |
|
|
Карбонільна (карбоніл) |
|
Карбонові кислоти |
|
|
Карбоксильна (карбоксил) |
|
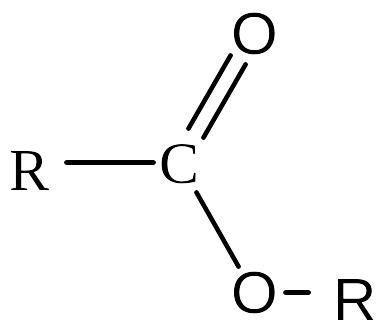
Складні ефіри (естери) |
|
|
Складно-ефірна |
|
Нітросполуки |
R–NO2 |
CH3–NO2, C6H5–NO2
|
Нітрогрупа |
–NO2 |
Аміни |
R–NH2
|
CH3–NH2, C6H5–NH2
|
Аміногрупа |
–NН2 |
Сульфокислоти |
R–SO3H |
CH3–SO3H C6H5–SO3H |
Cульфогрупа |
–SO3H (–SO2–OH) |
Кожний клас сполук утворює гомологічні ряди. Гомологічний ряд – це ряд сполук, у якому кожний наступний представник відрізняється від попереднього на групу атомів –СН2, яка називається гомологічною різницею. Гомологічний ряд кожного класу зображується загальною формулою. Наприклад, насичені вуглеводні мають загальну формулу CnH2n+2.
СН4 – метан; С6Н14 – гексан;
С2Н6 – етан; С7Н16 – гептан;
С3Н8 – пропан; С8Н18 – октан;
С4Н10 – бутан; С9Н20 – нонан;
С5Н12 – пентан; С10Н22 – декан.
Під час вивчення властивостей кожного класу сполук необхідно звернути увагу на закономірності хімічних реакцій, які в межах гомологічного ряду є загальними для всіх гомологів. Знаючи властивості одного із членів гомологічного ряду можна зробити висновки про властивості інших представників цього ряду.