
Экзаменационные ответы
.pdfУЗИ |
+ |
- |
- |
Лапароскопия (мониторная) |
+ |
± |
± |
Чрескожная гепатохолангио-графия |
+ |
+ |
+ |
Компьютерная томография |
+ |
± |
± |
Примечание:
+ - высокоинформативное исследование для данной локализации;
± - относительно информативное исследование для данной локализации; - -неинформативное исследование для данной локализации.
ЛЕЧЕНИЕ Панкреатодуоденальная резекция при раке поджелудочной железы из-за низкого процента резектабельности,
технических трудностей и высокого риска выполняется в настоящее время редко. Большинство хирургов предпочитают паллиативные вмешательства, даже если возможно удаление опухоли.
Больным раком большого дуоденального сосочка проводят гастропанкреатодуоденальную резекцию. При наличии противопоказаний к радикальному вмешательству выполняют условно радикальные операции: папиллэктомию, дуоденэктомию либо экономную панкреатодуоденальную резекцию.
Паллиативные операции производят со следующими целями.
1.Устранение желтухи.
2.Улучшение или восстановление пассажа по двенадцатиперстной кишке.
3.Включение в пищеварение поджелудочной железы.
4.Снятие болей за счет уменьшения напряжения.
Эффект от паллиативных вмешательств недолговременный, так как ликвидируя желчную гипертензию или кишечную непроходимость, операция не оказывает влияния на продолжающийся рост опухоли.
Лучевая терапия рака поджелудочной железы в настоящее время применяется эпизодически, хотя полученные некоторыми исследователями данные позволяют говорить о ее перспективности. Трудность лучевого лечения опухолей этой локализации связана в основном с особенностями анатомического расположения органов панкреатодуоденальной области и близостью жизненно важных органов с малой толерантностью к лучевому воздействию.
Химиотерапия рака панкреатодуоденальной области сопряжена с рядом проблем, связанных прежде всего с тяжестью состояния данной категории больных.
46.Рак поджелудочной железы. Заболеваемость и смертность. Клиническая картина в зависимости от локализации опухоли, Принципы диагностики. Способы морфологического подтверждения диагноза.
47.Рак поджелудочной железы. Информативность различных методов диагностики. Показания к инвазивным методам исследования, Принципы хирургического лечения.
До сих пор рак панкреатодуоденальной области (ПДО) остается самой фатальной опухолью.
Заболеваемость раком поджелудочной железы ежегодно увеличивается. Эта болезнь занимает шестое место по распространённости среди онкологических заболеваний среди взрослого населения. Заболевают в основном лица пожилого возраста, старше 60 лет. Мужчины и женщины болеют одинаково часто. Наиболее частой локализацией рака поджелудочной железы является головка - в 50-60 % случаев, тотальное поражение поджелудочной железы наблюдается в 20-35 % случаев, тело поражается приблизительно в 10 %, хвост - в 5-8 %. В США в данное время рак поджелудочной железы находится на четвертом месте среди причин смерти от рака. При появлении характерных симптомов лишь 10% пациентов оказываются операбельными, а 5 лет после установления диагноза живут менее 1% больных.
Факторами риска рака поджелудочной железы являются:
•употребление спиртных напитков
•курение
•обилие жирной и острой пищи
•сахарный диабет
•цирроз печени
Кпредраковым заболеваниям относятся:
•Аденома поджелудочной железы
•Хронический панкреатит
•Киста поджелудочной железы
Метастазирование при раке поджелудочной железы бывает лимфогенным, гематогенным и имплантационным. При гематогенном метастазировании отдаленные метастазы рака поджелудочной железы наиболее часто обнаруживаются в печени, легких, почках, костях и других органах.
Имплантационное метастазирование рака поджелудочной железы происходит путем контактного переноса раковых клеток по брюшине (карциноматоз брюшины, раковый асцит).
КЛИНИЧЕСКАЯ КАРТИНА Клиническая картина зависит от локализации опухоли. Общими признаками рака поджелудочной железы являются:
потеря аппетита, тошнота, похудение, общая слабость, тупые боли в верхней половине живота, расстройство функции кишечника, повышение температуры тела, симптом Труссо (мигрирующий тромбофлебит).
Часто первым клиническим признаком рака поджелудочной железы («сигналом тревоги») является протекающая без повышения температуры тела и болевых приступов механическая желтуха. Последняя при раке поджелудочной железы обусловлена тем, что раковый узел, увеличиваясь в размерах, вначале раздвигает «подкову» двенадцатиперстной кишки и сдавливает ее просвет, затем прорастает ее стенку, распространяется на желчевыводящие протоки, вызывая нарушение их проходимости. Желтушная окраска кожных покровов сменяется постепенно оливковым, далее - темно-зеленым цветом; характерны желтушность склер глаз и видимых слизистых оболочек, бесцветный (ахоличный) кал, темная моча, кожный зуд. Температура тела становится субфебрильной. В этом периоде становится заметным похудение больного. Давление желчи во всех протоках, расположенных выше сдавления, повышается. Это сопровождается равномерным расширением желчных протоков и приводит к увеличению печени и желчного пузыря.
Болевой синдром в такой ситуации усиливается в положении лежа на спине, когда происходит наиболее сильное давление опухоли на солнечное сплетение. Вследствие этого больные принимают вынужденное положение: сидя, согнувшись кпереди, или лежа на боку с приведенными к животу ногами.
При раке головки поджелудочной железы характерен симптом Курвуазье - обнаружение при пальпации объемного безболезненного образования в правом верхнем квадранте живота (растянутого желчного пузыря).
Для рака головки поджелудочной железы характерны:
-стойкий, прогрессирующий характер желтухи;
-боли в животе, с преимущественной локализацией в эпигастральной области, с иррадиацией в поясницу;
-выраженное похудание: за короткий срок больные теряют в весе до 10-15 кг;
-плохое общее состояние, выражающееся в слабости, потере работоспособности, ухудшении аппетита;
-наличие непереваренных жиров в кале (стеаторея);
-нередко у больных возникает мигрирующий тромбофлебит;
-иногда в начале заболевания отмечается повышение уровня диастазы в крови и моче;
-острое начало заболевания с приступообразных болей в правом подреберье, повышение температуры тела, после чего, как правило, возникает желтуха. Боли иррадиируют в лопатку.
При раке тела и хвоста поджелудочной железы характерна постоянная ноющая боль в эпигастрии с иррадиацией в поясницу; интенсивность боли меняется при изменении положения тела. Растущая опухоль достигает желудка и поперечной ободочной кишки, прорастает их стенки, нарушая проходимость этих органов.
При раке поджелудочной железы нарастает раковая интоксикация, нарушаются все функции железы, деятельность других органов пищеварительной системы; возможны профузные кровотечения в пораженных прорастающей опухолью полых органах.
ДИАГНОСТИКА Установление диагноза представляет наибольшие трудности среди всех остальных локализаций злокачественных новообразований.
В лабораторных анализах крови определяются анемия, лейкоцитоз или лейкопения, ускоренная СОЭ, повышенное содержание билирубина, повышение липазы и амилазы, щелочной фосфатазы и трипсина. Функции печени при раке поджелудочной железы оказываются измененными только спустя более или менее значительный срок после начала болезни. Выраженный рост активности альдолазы и аминотрансфераз при желтухе имеет большое дифференциальнодиагностическое значение.
Рентгенологическая диагностика
1.Рентгеноскопия (-графия) желудка и двенадцатиперстной кишки. При этом методе исследования могут быть выявлены различные деформации желудка и двенадцатиперстной кишки, обусловленные сдавлением или прорастанием их опухолью поджелудочной железы, деформации слизистой оболочки и нарушения моторики двенадцатиперстной кишки.
2.Релаксационная дуоденография. С помощью этого метода при опухоли головки железы выявляются деформация привратника и двенадцатиперстной кишки, ее смещение кверху и вправо, сужение просвета, расширение «подковы».
При опухоли тела железы определяются смещение желудка кпереди и влево, дефект наполнения вследствие прорастания стенки желудка опухолью.
3.Ирригоскопия (-графия) - позволяет выявить сдавление поперечной ободочной кишки, дефект наполнения, обусловленный прорастающей опухолью.
4.КТ. На основании данного, дополнительного, метода исследования выявляются увеличение размеров и неоднородность железы, опухоль с неровными и нечеткими контурами, определяется потеря дифференциации парапанкреатической клетчатки. Примерно у 90 % больных КТ выявляет косвенный признак рака поджелудочной железы - расширение внутрипеченочных желчных протоков при механической желтухе (
Ультразвуковое исследование. При раке поджелудочной железы на сонограммах выявляются увеличение размеров железы, нечеткость ее контуров, расширение протоков; паренхима ее может быть гомогенной или содержать гетерогенные эхоструктуры. Из-за поглощения УЗ опухолью может исчезать задняя граница поджелудочной железы. Определяются симптомы билиарной гипертензии - расширение внутрипеченочных и общего желчного протока, увеличение желчного пузыря.
Пункционная биопсия - выполняется под контролем УЗИ и решает единственную диагностическую задачу: морфологическую верификацию изменений в поджелудочной железе.
Эндоскопические методы исследования
1.Фиброгастродуоденоскопия - позволяет выявить признаки сдавления желудка и двенадцатиперстной кишки. При прорастании опухолью этих органов возможен визуальный осмотр опухоли и биопсия.
2.Пероральная панкреатохолангиоскопия - дает возможность провести визуальный осмотр главного панкреатического и общего желчного протоков, выявить опухоль или стеноз протоков.
3.Лапароскопия - помогает выявить признаки механической желтухи: желто-зеленая окраска нижней поверхности печени, растянутый, напряженный желчный пузырь. Иногда в отлогих местах брюшной полости на фоне макроскопически неизмененной печени обнаруживается асцит.
Рентгеноэндоскопическая диагностика проводится с использованием метода эндоскопической ретроградной панкреатохолангиографии (ЭРПХГ) под рентгенотелевизионным контролем (РТВК) На холангиограммах определяются сегментарные стенозы с престенотическими расширениями, равномерное сужение протока железы или полная его закупорка, при механической желтухе - стриктура внепеченочных желчных протоков.
Рентгенохирургическая диагностика
1.Чрескожная чреспеченочная холангиография (ЧЧХГ). При антеградном введении контрастного вещества в желчные протоки через иглу Хиба, проведенную через кожу и паренхиму печени под РТВК, можно выявить картину механической желтухи, характеризующуюся расширением желчных протоков, напряженным желчным пузырем.
2.Ангиография (спленопортография, целиакография, мезентерикография) - позволяет установить смещение артерий, их сужение с «изъязвлением» контуров, скопление контрастного вещества в артериальной фазе, смещение, стеноз или окклюзию вен, ригидность стенок сосудов, возникновение «опухолевидных» сосудов, неравномерное контрастирование в паренхиматозной фазе.
Радионуклидное исследование. Панкреатосцинтиграфия с применением селенметионина (75Sе-метионина) выявляет «холодные» очаги, соответствующие локализации опухоли, деформацию и нечеткость контуров железы, блок выведения РФП в кишечник.
Опухолевые маркёры
•СА 19-9 - чувствительность при эндокринном раке составляет 80%. Значения данного маркёра коррелируют с распространением опухолевого процесса.
•РЭА - уровень больше 5 нг/мл может свидетельствовать о наличии рака.
Информативность методов исследования в зависимости от локализации опухоли
Метод исследования |
Локализация опухоли |
|
|
|
|
Поджелудочная железа |
|
Большой дуоденальный сосочек |
Желчные |
|
|
|
|
протоки |
Гипотоническая дуодено-графия |
- |
+ |
- |
|
Дуоденоскопия |
- |
+ |
- |
|
Ретроградная холицисто-панкреатография |
+ |
+ |
+ |
|
Селективная ангиография |
+ |
- |
- |
|
Продолжение табл. 5 |
|
|
|
|
Сцинтиграфия |
+ |
|
- |
- |
УЗИ |
+ |
- |
- |
Лапароскопия (мониторная) |
+ |
± |
± |
Чрескожная гепатохолангио-графия |
+ |
+ |
+ |
Компьютерная томография |
+ |
± |
± |
Примечание:
+ - высокоинформативное исследование для данной локализации;
± - относительно информативное исследование для данной локализации; - -неинформативное исследование для данной локализации.
ЛЕЧЕНИЕ Лечение рака поджелудочной железы - один из наиболее сложных разделов онкологии. Трудности лечения прежде
всего связаны с тем, что больные раком поджелудочной железы - это лица пожилого и старческого возраста, с различными сопутствующими заболеваниями и распространенным опухолевым процессом с поражением смежных органов.
Хирургический метод лечения на современном этапе является ведущим в лечении рака поджелудочной железы. Различают радикальные и паллиативные операции. К радикальным операциям при раке поджелудочной железы относят панкреатодуоденальную резекцию в разных модификациях, резекцию тела и хвоста железы, тотальную панкреатодуоденэктомию.
Паллиативные операции выполняются с целью улучшения качества жизни пациентов и направлены на устранение болевого синдрома, механической желтухи, непроходимости двенадцатиперстной кишки. Различают следующие варианты паллиативных операций: наложение билиодигестивных анастомозов между желчным пузырем или общим желчным протоком и тонкой кишкой или желудком; «бескровное желчеотведение».
Операбельность при раке поджелудочной железы составляет от 10 до 25 %. Послеоперационная летальность, достигающая 25-40 %, зависит от стадии опухоли. Основными причинами послеоперационной летальности являются изменения в культе железы, несостоятельность панкреатоеюнального анастомоза, печеночная недостаточность.
Средняя продолжительность жизни больных с установленным диагнозом рака поджелудочной железы составляет:
•без операции - около 6 мес;
•после радикальной операции - 1,5-2 года (в зависимости от стадии опухоли);
•после паллиативной операции - 6-12 мес.
При лечении рака поджелудочной железы используются следующие виды лучевой терапии:
1)дистанционная гамма-терапия;
2)облучение тормозным излучением;
3)облучение быстрыми электронами.
Проводятся пред-, интра- и послеоперационные курсы облучения. Средняя продолжительность жизни больных, получавших лучевую терапию по поводу рака поджелудочной железы, составляет 12-13 мес, в комбинации с паллиативными операциями - около 16 мес. Внутри- и внегоспитальная летальность связана с раковой интоксикацией и кахексией, местными и общими лучевыми реакциями.
Химиотерапия применяется самостоятельно, если невозможно провести другое лечение при распространенном процессе или в сочетании с другими методами лечения. Эффективность монохимиотерапии составляет 15-30 %, ПХТ - 40 %, при этом удается добиться только частичной регрессии опухоли.
48. Дифференциальная диагностика желтухи. Особенности клинических и лабораторных проявлений при механической желтухе. Методы устранения механической желтухи.
Дифференциальная диагностика различных форм желтухи
Форма желтухи |
Билирубин |
Уробилин в моче |
Стеркобилин в кале |
||
в крови |
в моче |
||||
|
|
|
|||
|
|
|
|
|
|
Механическая |
+++ |
++ |
- |
- |
|
Паренхиматозная |
++ |
+ |
++ |
+ |
|
Гемолитическая |
+++ |
- |
+ |
++ |
|
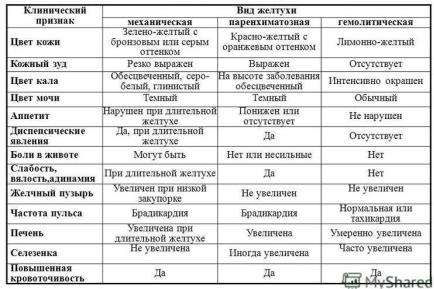
Примечание. +++ концентрация резко повышена; ++ умеренно повышена; + определяется; - не определяется.
Различают следующие варианты паллиативных операций: наложение билиодигестивных анастомозов между желчным пузырем или общим желчным протоком и тонкой кишкой или желудком; «бескровное желчеотведение».
Рентгенохирургическое лечение («бескровное желчеотведение») - вариант паллиативного метода лечения, направленный на декомпрессию желчных протоков у больных с механической желтухой. Выполняются различные рентгенобилиарные вмешательства.
1.Чрескожная реканализация гепатикохоледоха.
2.Наружное и наружновнутреннее дренирование желчных протоков - чрескожная чреспеченочная установка дренажа - трубки из синтетического материала, катетера в желчный проток под РТВК. Применяется самостоятельно, а также как этап подготовки к хирургической операции или эндобилиарному протезированию.
3.Чрескожная гепатикохолангиостомия.
4.Эндобилиарное протезирование (внутреннее дренирование) - чрескожная чреспеченочная установка эндопротеза из синтетического материала или нитинолового эндопротеза в месте стриктуры желчного протока под РТВК. Возможна интраоперационная имплантация. Средняя продолжительность жизни при выполнении эндобилиарного протезирования в качестве альтернативы паллиативной операции составляет 6-12 мес.
49. Первичные и метастатические опухоли печени. Возможности дифференциальной диагностики и лечения.
I. Эпителиальные опухоли. А. Доброкачественные.
1.Печеночно-клеточная аденома (гепатоцеллюлярная аденома).
2.Аденома внутрипеченочных желчных протоков.
3.Цистаденома внутрипеченочных желчных протоков.
Б. Злокачественные.
1.ГЦР (печеночно-клеточный рак).
2.Холангиокарцинома (рак внутрипеченочных желчных протоков).
3.Цистаденокарцинома желчных протоков.
4.Смешанный гепатохолангиоцеллюлярный рак.
5.Гепатобластома.
6.Недифференцированный рак.
II. Неэпителиальные опухоли. A. Гемангиома.
Б. Инфантильная гемангиоэндотелиома. B. Гемангиосаркома.
Г. Эмбриональная саркома. Д. Другие.
III. Различные другие типы опухолей. A. Тератома.
Б. Карциносаркома. B. Другие.
IV. Неклассифицируемые опухоли.
Первичный рак печени в России является сравнительно редким заболеванием и составляет 3-5 % в общей структуре злокачественных новообразований. Более 90 % среди всех злокачественных новообразований печени составляют вторичные, или метастатические, злокачественные опухоли. По локализации метастатического рака печень занимает 1-е место. Обычно метастазирование происходит по печеночной артерии, воротной вене и по протяжению.
Наиболее частые локализации первичной опухоли при MTS в печени - толстая кишка, желудок, поджелудочная железа, легкие, молочная железа. Гистологическое строение MTS в печени чаще всего повторяет гистологическое строение первичных опухолей.
Симптоматология вторичных (метастатических) опухолей печени определяется первичным и вторичным опухолевыми процессами. Метастатический рак печени в целом характеризуется быстрым прогрессированием и отсутствием специфической клинико-лабораторной симптоматики. Hарастающая слабость, ухудшение аппетита, похудание, неинтенсивные давящие боли в эпигастральной области, увеличение печени. Эпизоды повышенной температуры тела у больных с MTS в печени свидетельствуют о значительном поражении печени, вовлечении обеих долей.
Всех больных с MTS в печени делят на 2 группы независимо от источников метастазирования:
-больные с солитарными единичными MTS в печени: -симптомы заболевания напоминают проявления массивной формы первичного рака печени;
-больные с множественными MTS в печени: -локальные и общие симптомы более выражены: нарастающая печеночная недостаточность, механическая желтуха, некроз опухолевых узлов, их разрыв, синдром сдавления нижней полой вены, асцит.
Более 3 MTS считаются множественными.
В диагностике метастатических опухолей печени используют УЗИ, КТ, лапароскопию с взятием биопсии. Необходимо определение уровня маркеров РЭA, СA19-9, которые обнаруживают при РМЖ, раке поджелудочной железы, легкого, яичников и раке толстой кишки. Повышение их концетрации свидетельствует в пользу метастатического рака печени.
Лечение
Основной метод лечения рака печени - хирургический. Выполняются такие операции, как резекция одного сегмента печени, двух сегментов, лобэктомия правосторонняя или левосторонняя, гемигепатэктомия, расширенная гемигепатэктомия. Возраст больных, наличие цирроза печени, выраженной сопутствующей патологии не считаются абсолютными противопоказаниями к операции.
При развитии желтухи в качестве паллиативных операций выполняются различные варианты наружного и внутреннего отведения желчи: наложение билиодигестивных анастомозов с внутрипеченочными желчными протоками, реканализация опухоли, наружное дренирование внутрипеченочных желчных протоков через общий желчный проток, наложение гепатохолангиостомы.
50. Рак печени. Заболеваемость. Гистологические варианты слоения. Клиника. Методы диагностики. Возможности лечения.
Первичный рак печени в России является сравнительно редким заболеванием и составляет 3-5 % в общей структуре злокачественных новообразований.
ФАКТОРЫ РИСКА
1.Вирусоносительство антигена гепатита В (HBs-антиген обнаруживают у 70-90 % больных первичным раком печени). Возбудитель гепатита С также является одним из факторов высокого риска, способствующих развитию гепатоцеллюлярного рака (ГЦР).
2.Длительное употребление алкоголя, приводящее к циррозу печени (ЦП), является одним из факторов риска возникновения рака. При ЦП в печени происходят процессы атрофической клеточной дегенерации, в гепатоцитах наблюдаются признаки клеточной атипии.
3.Описторхозная инвазия.
Среди первичных злокачественных опухолей печени ГЦР встречается чаще, чем холангиокарцинома: в 70-80 % случаев по сравнению c 20-30 %. ГЦР почти всегда сочетается с ЦП, в отличие от рака внутрипеченочных желчных протоков, который сопровождается циррозом примерно в 25 % случаев.
МАКРОСКОПИЧЕСКИЕ ФОРМЫ ПЕРВИЧНОГО РАКА ПЕЧЕНИ
1.Узловая форма - встречается наиболее часто, составляя 60-85 % всех форм рака (рис. 23.1). Почти всегда сопровождается ЦП. В толще увеличенной в размерах печени содержатся многочисленные опухолевые очаги - как микроскопические, так и диаметром до нескольких сантиметров.
2.Массивная форма - встречается почти в 25 % случаев первичного рака печени. Опухоль обычно располагается в правой доле печени и иногда достигает огромных размеров. При массивной форме рака ЦП встречается очень редко. Опухоли единичные либо окружены более мелкими метастатическими очагами.
3.Диффузная форма - встречается реже, чем предыдущие; составляет около 12 % всех случаев первичного рака печени. Печень не увеличена в объеме. На фоне атрофического цирроза развивается милиарный карциноматоз печени.
Метастазирование
К регионарным лимфатическим узлам печени относятся воротные, супрапанкреатические, передние и задние узлы средостения. Длительное время считали, что гематогенные метастазы при первичном раке печени встречаются редко. В настоящее время установлено, что одним из ранних проявлений первичного рака печени в 1,5-5 % случаев являются гематогенные метастазы в ребра и позвоночник. Метастазы первичного рака печени в легкие обнаруживаются на более поздних стадиях заболевания примерно в 10 % случаев. Значительно чаще происходит внепеченочное распространение опухоли в близлежащие органы - диафрагму, желудок, двенадцатиперстную кишку, надпочечники. Метастазы гепатоцеллюлярного рака могут сохранять функциональные свойства клеток печени (например, способность секретировать желчь).
КЛИНИЧЕСКАЯ КАРТИНА Особенностями клинической картины первичного рака печени являются незаметное начало, неспецифичность
субъективных симптомов, быстрое течение болезни, в результате чего диагноз почти всегда устанавливают в запущенной стадии заболевания.
Больные обращаются к врачу впервые в среднем через 3 мес с момента появления первых симптомов заболевания. Примерно 75 % больных жалуются на похудение, отсутствие аппетита, боли в животе. Более половины больных сами обнаруживают у себя опухоль в области печени. Преобладающими среди пациентов являются жалобы на выраженную общую слабость, вялость, быструю утомляемость, увеличение размеров живота, желтуху, повышение температуры тела, понос, тошноту, рвоту, появление отеков, носовые кровотечения.
Основным объективным симптомом заболевания служит гепатомегалия, которая наблюдается примерно у 90 % больных первичным раком печени. Нижняя граница печени по правой среднеключичной линии увеличивается в среднем на 5-10 см. Верхняя граница печени достигает уровня IV ребра, увеличивается и переднезадний размер грудной клетки. При пальпации печень очень плотная (каменистой консистенции), иногда с гладкой поверхностью и твердым и острым передним краем. Увеличение печени сопровождается ощущением распирания в эпигастральной области. Более чем у половины больных поверхность печени и передний ее край - с множеством узелков различной величины, чаще плотной консистенции. В более редких случаях наблюдается очаговое увеличение печени, при этом пальпаторно удается определить нечетко отграниченную опухоль в правой или левой половине печени. Увеличивающаяся в размерах опухоль сдавливает ветви воротной вены. Следствием этого являются портальная гипертензия, увеличение размеров селезенки, иногда - расширение вен пищевода.
На боль в правом подреберье, эпигастрии или поясничной области жалуются около 70 % больных. Боль вызывается быстрым ростом опухоли и растяжением вследствие этого глиссоновой капсулы печени, иногда - сопутствующим перигепатитом. Болевой симптом вначале периодический, возникает при ходьбе и физическом напряжении. Позже боль может стать постоянной, умеренно интенсивного характера, обычно проявляется ощущением тяжести в эпигастрии и правом подреберье.
Желтуха - симптом непостоянный, как правило, она ярко не выражена и наблюдается примерно у половины больных. При первичном раке печени желтуха механическая - причиной ее возникновения является сдавление опухолью внутрипеченочных желчных протоков. Интоксикация также приводит к недостаточности печени вследствие дегенеративных изменений ее клеточных структур. Интенсивность желтухи не всегда является признаком, характеризующим степень распространенности опухолевого процесса.
Асцит наблюдается у половины госпитализированных больных и соответствует синдрому портальной гипертензии, возникающей иногда вследствие внутрипеченочной блокады из-за ЦП, а иногда в результате внепеченочной блокады, обусловленной тромбозом воротной вены. Часто асцит бывает геморрагического характера. Асцитическая жидкость обычно не содержит опухолевых клеток.
Температура тела повышена у большинства больных - субфебрильная, обусловлена раковой интоксикацией. Иногда температура обусловлена инфицированием некротических очагов или развитием холангита.
Признаками, сопутствующими ЦП, на фоне которого возник первичный рак, являются развитие коллатерального кровообращения, увеличение селезенки, сосудистые звездочки, ладонная эритема, гинекомастия и др. Паранеопластические синдромы, наблюдающиеся примерно у 10-15 % больных, сопровождаются гипогликемией, эритроцитозом, гиперкальциемией, гиперхолестеринемией. Наиболее часто встречается гипогликемический
паранеопластический синдром, который проявляется нарастающей сонливостью, прогрессирующей слабостью и спутанностью сознания.
ДИАГНОСТИКА Диагностика рака печени представляет определенные трудности.
В клиническом анализе крови больного первичным раком печени выявляются повышенная СОЭ, нейтрофильный лейкоцитоз, иногда - эритроцитоз.
Лабораторная диагностика рака печени основана на обнаружении в сыворотке крови зародышевого белка α-
фетопротеина.
РЭA и СA 19-9 имеют большое значение в диагностике больных холангиоцеллюлярным раком, а также в выявлении больных метастатическим раком печени. При MTS рака печени РЭA чаще позитивный, при локальном раке - негативный.
Радиоизотопное сканирование печени с 131I, 198Au позволяет обнаружить «холодные» очаги в печени, соответствующие локализации опухоли.
УЗИ позволяет визуализировать опухолевый очаг, увеличенные регионарные лимфатические узлы, выявить асцит и метастатическое поражение печени.
Первичный рак печени на сонограмме представляет собой округлой формы образование с эхопозитивными и эхонегативными участками, иногда с полостью распада в центре.
Одним из методов топической диагностики новообразований печени является КТ МРТ также применяется с целью диагностики первичного рака печени; ее преимуществом является возможность
получения изображения печени в различных срезах, вследствие чего повышается информативность метода в отношении уточнения локализации опухоли и внутри- и внепеченочного ее распространения.
Методом морфологической диагностики первичного рака печени является тонкоигольная пункционная биопсия, которую выполняют под контролем УЗИ и лапароскопии. Наиболее достоверный диагноз первичного рака печени устанавливают при лапароскопии с биопсией опухоли.
ЛЕЧЕНИЕ Несмотря на успехи медицины и научный прорыв в ряде ее областей, при злокачественных новообразованиях печени
современная онкология пока не может предложить более радикального средства, чем хирургическое лечение,
которое сегодня остается «золотым стандартом».
5-летняя выживаемость (при метастазировании колоректального рака в печень), по литературным данным, составляет от 25-28 до 35-40 %. В комбинации с химиотерапией в адъювантном режиме, по данным Ю.И. Патютко и соавт. (2003), 5-летняя выживаемость при метастазах колоректального рака в печень повышается до 48 %. К сожалению, как известно, операбельность при злокачественных опухолях печени, по сводным данным, не превышает 15-20 % (рис. 23.3), т.е. более 80 % больных подлежат нехирургическим методам противоопухолевого воздействия.
Методы нехирургического лечения можно условно разделить на лекарственные (системная/регионарная химиотерапия, химиоэмболизация), местно-деструирующие способы воздействия (аблация, радиоэмболизация) и лучевую терапию. В ряде случаев эффективной оказывается комбинация нескольких методов.
Эффективность химиотерапии при лечении больных с нерезектабельными колоректальными метастазами в печень была столь незначительна, а ее токсичность так велика, что до 1990-х годов считалось более этичным не проводить ее вообще. Углубленные исследования в области канцерогенеза, изучения механизмов функционирования опухолевых клеток стали стимулом к синтезу препаратов для таргетной терапии - таких, как бевацизумаб (авастин) - ингибитор рецепторов сосудистого фактора роста эндотелиальных клеток, цетуксимаб - ингибитор рецепторов эпидермального фактора роста, целекоксиб - ингибитор циклооксигеназы-2. Предварительные результаты многочисленных работ, посвященных изучению эффективности химиотерапии с включением в схему лечения этих препаратов, демонстрируют потенциальную возможность увеличения частоты объективного ответа, времени до прогрессирования и общей выживаемости. Для снижения общей токсичности и повышения концентрации химиопрепарата в опухолевой ткани с 1970-х годов применяют методику регионарной внутриартериальной инфузии препаратов в общую печеночную артерию.
Химиоэмболизация применяется как самостоятельно, так и в сочетании с другими способами лечения.
В основе метода лежит особенность кровоснабжения печени и опухолевых узлов. 75 % притекающей к печени крови доставляется по портальной вене и лишь 25 % - по печеночной артерии, в то время как кровоснабжение опухолевой ткани на 95 % осуществляется за счет более оксигенированной артериальной крови из бассейна печеночной артерии. Таким образом, при эмболизации ветвей печеночной артерии создается зона ишемии, к которой высокочувствительны опухолевые клетки. В этой зоне развивается ишемический некроз.
Лучевая терапия. Дистанционная лучевая терапия не получила широкого распространения из-за того, что малые (субтерапевтические) дозы не давали желаемого результата, а при подведении терапевтических доз крайне высока вероятность развития лучевого гепатита. С целью снижения лучевой нагрузки на неизмененную паренхиму печени
был разработан метод местного лучевого воздействия на опухоль посредством доставки радиоизотопа непосредственно к опухоли.
Поиски новых, эффективных методов воздействия на новообразования печени сегодня входят в список приоритетных задач большинства противораковых центров.
В последнее 10-летие активно развивается и получает широкое применение сравнительно новый метод лечения опухолей печени - аблация опухолей, т.е. локальное деструктивное воздействие, приводящее к развитию некроза с последующей организацией. Важно отметить, что метод может применяться как во время полостных операций, так и чрескожно. Это существенно расширяет контингент больных, подлежащих лечению.
Аблация (от лат. ablation) - методика прямого направленного умертвления ткани. Выделяют термическую аблацию и химическую (введение этилового спирта либо уксусной кислоты в опухоль) деструкцию, электрохимический лизис. Сфокусированный высокоинтенсивный УЗ - это методика гипертермической деструкции тканей, использующая УЗ-энергию, которая сфокусирована в точке приложения на определенной глубине в теле человека. При этом поверхностные и глубокие структуры и органы, находящиеся на пути луча, остаются интактными. Эффект достигается посредством двух механизмов: сначала температура повышается из-за поглощения энергии звуковых волн, что приводит к выраженному в различной степени термическому повреждению ткани. Второй механизм - это явление переходной или инерционной кавитации.
51. Рак ободочной кишки. Группы риска. Особенности клинического течения. Методы диагностики. Принципы лечения,
Рак ободочной кишки (РОК) занимает 2-3 место в структуре злокачественных новообразований ЖКТ и составляет от 4до6 % всей онкологической заболеваемости. Преимущественный возраст заболевших - более 50 лет.
ЭТИОЛОГИЧЕСКИЕ И ПАТОГЕНЕТИЧЕСКИЕ ФАКТОРЫ По мнению большинства исследователей, на рост заболеваемости РОК оказывают влияние следующие этиологические и патогенетические факторы:
1)характер питания населения: малошлаковая пища с преобладанием животных жиров, белков и рафинированных углеводов (сахар);
2)малоподвижный образ жизни - гипокинезия, ожирение, возраст старше 50 лет;
3)гипотония и атония кишечника в пожилом возрасте - хронический запор;
4)наличие в кишечном содержимом эндогенных канцерогенов (индола, скатола, гуанидина, метаболитов стероидных гормонов) и их воздействие на слизистую оболочку кишки в условиях длительного застоя каловых масс;
5)хроническая травматизация калом слизистой оболочки толстой кишки в местах физиологических изгибов.
ПРЕДРАКОВЫЕ ЗАБОЛЕВАНИЯ К предраковым заболеваниям относятся:
•хронический колит, в частности хронический неспецифический язвенный колит и гранулематозный колит (болезнь Крона), которые составляют основную группу факультативных предраковых заболеваний;
•дивертикулы (дивертикулез) ободочной кишки (дивертикулит). Малигнизируются редко;
•полипозное поражение ободочной кишки (облигатный предрак):
а) одиночные полипы (аденоматозный, ворсинчатый), которые малигнизируются в 45-50 % случаев, особенно полипы величиной >2 см; ворсинчатые полипы озлокачествляются чаще; б) множественный полипоз ободочной кишки,
ПРОФИЛАКТИКА
1.Профилактические осмотры необходимы для выявления групп населения повышенного риска и ранних форм рака ободочной и прямой кишок. Современные автоматизированные скрининги предусматривают использование разработанных карт-анкет с последующей их обработкой на ЭВМ. Огромное значение при этом имеет использование гемокульт-теста для отбора групп повышенного риска с целью последующего эндоскопического исследования (ректороманоскопия, фиброколоноскопия с морфологическим исследованием биоптатов опухоли).
2.Диспансеризация, наблюдение и лечение больных с предопухолевыми заболеваниями и доброкачественными опухолями.
3.Формирование и пропаганда здорового образа жизни, рационального питания.
4.Оздоровление экологической обстановки.
5.У излеченных больных с учетом возможности рецидива или появления второй опухоли, при первичномножественных поражениях показана диспансеризация, включающая периодические активные осмотры с применением рентгенологических, эндоскопических, морфологических и лабораторных методов.
Клинико-анатомические формы РОК:
1)экзофитная (полиповидная, ворсинчато-папиллярная, узловая);
2)эндофитная (инфильтрирующая, язвенно-инфильтративная, циркулярно-стриктурирующая);
3)переходная или смешанная.
Согласно отечественной гистологической классификации, различают следующие формы опухолей ободочной кишки: аденокарцинома, солидный рак, слизистый (перстневидно-клеточный) и скиррозный рак. Различают также 3 степени дифференцировки рака: высокодифференцированный, средней степени дифференцировки и низкодифференцированный.
Закономерности метастазирования
Метастазирование РОК имеет свои особенности.
Лимфогенный путь. Различают 3 этапа метастазирования в регионарные лимфатические узлы:
•I этап - эпиколические или параколические лимфатические узлы;
•II этап - промежуточные или собственно брыжеечные лимфатические узлы;
•III этап - парааортальные, в область корня брыжейки ободочной кишки.
Далее лимфа собирается в лимфатическую цистерну, расположенную поперечно в области I-II поясничных позвонков. От цистерны лимфа по грудному лимфатическому протоку вливается в венозную систему в области левого венозного угла - места слияния подключичной вены с внутренней яремной. Там же обычно определяются надключичные метастазы.
Гематогенный путь метастазирования связан с прорастанием опухоли в венозную сеть с последующим распространением с током крови - прежде всего в печень, легкие, кости и другие органы.
Имплантационный путь метастазирования, или контактный, связан с прорастанием опухолью всех слоев стенки кишки, отрывом раковых клеток от основной массы опухоли и их имплантацией по брюшине. Эти раковые клетки дают начало мелкобугристому высыпанию, называемому карциноматозом брюшины. Последний обычно сопровождается раковым асцитом. Проявлением карциноматоза являются метастазы в пупок и по брюшине малого таза.
КЛИНИЧЕСКАЯ КАРТИНА Симптомы рака правой и левой половины ободочной кишки
Клинические проявления РОК весьма многообразны и определяются локализацией опухоли, анатомическим типом роста новообразования, гистологической структурой рака, стадией и степенью распространенности опухолевого процесса, осложнениями и индивидуальной реактивностью организма.
Клиническая картина РОК характеризуется следующими группами симптомов.
1.Боли в животе. Как начальный признак в 2-3 раза чаще встречаются при расположении опухоли в правой половине ободочной кишки. По характеру болевые ощущения могут быть самыми разнообразными - от тупых, ноющих незначительных болей до сильных, приступообразных, вынуждающих госпитализировать больных в хирургические стационары в порядке экстренной помощи. Появление таких болей свидетельствует о нарушении пассажа кишечного содержимого, развитии кишечной непроходимости, наблюдающейся чаще всего при левосторонней локализации опухоли.
2.Кишечный дискомфорт (потеря аппетита, отрыжка, иногда рвота, ощущение тяжести в верхней половине живота). Эти симптомы чаще наблюдаются при поражении поперечной ободочной кишки, правой ее половины, реже - при левосторонней локализации опухоли.
3.Кишечные расстройства (запор, понос, чередование запора с поносом, урчание и вздутие живота). Эти симптомы расстройства кишечного пассажа чаще всего наблюдаются при левосторонней локализации опухоли, что объясняется, во-первых, преимущественно циркулярным ростом опухоли в левой половине ободочной кишки, во-вторых, плотной консистенцией уже сформировавшихся каловых масс. Конечным этапом нарушения кишечного пассажа является развитие частичной, а затем и полной обтурационной толстокишечной непроходимости.
4.Патологические выделения в виде крови, слизи, гноя во время акта дефекации - частое проявление рака дистальных отделов сигмовидной кишки.
5.Нарушение общего состояния больных выражается недомоганием, повышенной утомляемостью, слабостью, похудением, лихорадкой, бледностью кожных покровов и нарастающей гипохромной анемией. Все эти общие симптомы заболевания связаны с интоксикацией организма, обусловленной распадающейся раковой опухолью и инфицированным кишечным отделяемым, характерным для рака правой половины ободочной кишки. Он связан с функциональной особенностью (всасывательной способностью) слизистой оболочки этого отдела толстой кишки. Наличие пальпируемой опухоли редко бывает первым симптомом заболевания, ему, как правило, предшествуют другие симптомы. Тем не менее пальпаторное определение опухоли зачастую служит основанием для постановки правильного диагноза.
Основные клинические формы
В настоящее время, по мнению большинства исследователей, целесообразно выделять 6 форм клинического течения РОК.
