
Экзаменационные ответы
.pdfКатегория N:
Nx - неизвестно о наличии метастазов в регионарных лимфатических узлах; N0 - метастазы в регионарные лимфатические узлы отсутствуют;
N1, N2, N3 - различная степень выраженности метастатического поражения регионарных лимфатических узлов. Категория М:
Мх - неизвестно, существуют ли отдаленные метастазы; М0 - отдаленные метастазы отсутствуют;
M1 - имеются отдаленные метастазы.
Кроме стадии распространенности процесса учитывается и категория G - гистологическая дифференцировка опухолей: Gх - степень дифференцировки не может быть оценена;
Gl - высокая степень дифференцировки; G2 - средняя степень дифференцировки; G3 - низкая степень дифференцировки; G4 - недифференцированные опухоли.
Категория М может быть дополнена конкретными проявлениями метастазов: ри1 - легкое, рег - брюшная полость, mar - костный мозг, bra - головной мозг, oss - кости, ski - кожа, р1е - плевра, lym - лимфатические узлы, пер - печень, oth - другие.
Стадийность рака желудка, согласно Международной классификации по системе ТNМ (1997), выглядит следующим образом. Согласно МКБ-10, рак желудка находится в рубрике С16:
Тх - недостаточно данных для оценки первичной опухоли; Т0 - первичная опухоль не определяется;
Tis - преинвазивная карцинома: интраэпителиальная опухоль без инвазии собственной пластинки слизистой оболочки (carcinoma in situ);
Tl - опухоль инфильтрирует слизистую оболочку и подслизистый слой; Т2 - опухоль инфильтрирует мышечную оболочку до субсерозного слоя;
Т3 - опухоль прорастает серозную оболочку без инвазии в соседние органы; Т4 - опухоль распространяется на соседние структуры;
Nx - недостаточно данных для оценки регионарных лимфатических узлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов; N1 - имеются метастазы в 1-6 регионарных лимфатических узлах;
N2 - имеются метастазы в 7-15 регионарных лимфатических узлах; N3 - имеются метастазы
ы более чем в 15 регионарных лимфатических узлах; Мх - недостаточно данных для определения отдаленных метастазов; М0 - отсутствие признаков отдаленных метастазов; М1 - имеются отдаленные метастазы.
8. Значение эндоскопических, цитологических, рентгенологических и иммунологических методов исследования в онкологии.
К основным видам лучевой диагностики относятся:
•рентгенодиагностика:
—базовая;
—рентгеновская КТ (РКТ);
•МРТ;
•УКТ:
—радионуклидная диагностика.
Базовая рентгенодиагностика включает в себя рентгеноскопию (рентгенотелевизионное просвечивание на аппаратах, оснащенных усилителями рентгеновского изображения - УРИ), флюорографию, рентгенографию и линейную томографию, а также специальные приемы и методики.
Рентгенотелевизионное просвечивание применяется в двух основных областях: при контрастных исследованиях ЖКТ и с целью уточнения состояния дыхательной системы. Также под рентгенотелевизионным контролем производятся пункционные биопсии и рентгеноэндоскопические процедуры.
Ирригоскопияконтрастное исследование прямой и толстой кишок (ретроградная контрастная клизма). Выявляемые при контрастной рентгеноскопии полых органов ЖКТ основные симптомы рака одинаковы, а именно:
• органическое (стойкое) сужение просвета полого органа с его деформацией; это характерно для инфильтративной формы рака с циркулярным распространением;
•дефект наполнения любой формы (отсутствие части изображения органа в месте, занятом опухолью); такие изменения характерны для экзофитно растущих новообразований внутрь просвета органа;
•ригидность стенки на ограниченном участке (определяется при тугом наполнении и при двойном контрастировании); за таким признаком чаще всего скрывается инфильтративная форма рака, растущая в стенке органа и кнаружи от него.
Специальные виды рентгенографии - холецистография, маммография (в том числе цисто- и дуктография), рентгенография в условиях искусственного пневмоторакса, пневмоперитонеума и пневморетроперитонеума, париетография, фистулография, некоторые рентгеноэндоскопические процедуры и др. являются прерогативой специализированных учреждений онкологического и иного профиля.
Компьютерная томография (КТ), или рентгеновская компьютерная томография (РКТ) - рентгеновский метод исследования, основанный на компьютерной обработке данных о степени поглощения рентгеновского излучения в разных точках изучаемого пространства. КТ как бы отражает поверхностное строение атомов вещества (рентгеновскую или электронную плотность), так как поглощение рентгеновского излучения в значительной степени связано с переходом электронов с орбиты на орбиту: чем ярче выглядит ткань на КТ, тем она плотнее.
Магнитно-резонансная томография (МРТ) относится к неионизирующему (т.е. практически безвредному) методу лучевой диагностики, основанному на использовании физического явления, называемого ядерно-магнитным резонансом (ЯМР). Диагностические преимущества МРТ (по сравнению с другими методами получения изображения) основаны на возможности построения анатомических изображений с учетом нескольких физических параметров, в частности, протонной плотности, времени релаксации Т1 и Т2, что в сочетании с применением большого количества разнообразных импульсных последовательностей (протоколов исследования) почти всегда позволяет выявить различия в отображении нормальных и патологически измененных тканей, особенно если применяются методики внутривенного введения специальных, парамагнитных контрастных препаратов, изменяющих физические параметры исследуемых органов и тканей (время релаксации и магнитную восприимчивость). Все остальные базовые диагностические методы обеспечивают построение анатомических изображений на основе лишь одного физического параметра: при УЗИ - это эхогенность тканей, при рентгенографии и РКТ - коэффициент поглощения рентгеновских лучей, при радионуклидных исследованиях - интенсивность (энергия) гаммаизлучающих или позитронизлучающих радионуклидов.По ряду показателей (точность, чувствительность и специфичность) МРТ превышает информативности КТ в одних областях на 1-2 %, в других - на 40 % и более.
Ультразвуковая диагностика (УЗД, сонотомография) стала одним из ведущих методов лучевой диагностики. Таким образом, УЗД все активнее используется в онкологии и призвана решать ряд задач:
—выявление новообразования;
—дифференциальная диагностика;
—определение распространения опухоли на соседние органы, ткани и магистральные сосуды;
—выявление отдаленных метастазов;
—динамический контроль за эффективностью лечения;
—выявление послеоперационных изменений и осложнений;
—сопровождение и контроль в реальном времени интервенционных вмешательств.
Радионуклидная диагностика (РНД) - группа методов, основанная на регистрации изображений от объектов, излучающих гамма-кванты. Чтобы человеческий организм стал источником гаммаизлучения, в него вводят радиофармацевтические препараты (РФП), различные химические или биологические субстанции, меченные радионуклидами. Органотропные РФП распределяются преимущественно в пределах органов и систем, изображение которых необходимо получить. Современной аппаратурой для РНД является эмиссионный компьютерный томограф (рис. 6.11), который позволяет проводить все виды радионуклидных исследований: функциональные (в том числе синхронизированные с ЭКГ), сканы «всего тела», томографию (однофотонная эмиссионная компьютерная томография - ОФЭКТ), прицельную планарную сцинтиграфию в любых проекциях.
Самым распространенным гамма-топографическим исследованием является сканирование скелета (рис. 6.12) с целью выявления метастазов в костную систему. Актуальными остаются исследования с такими органотропными РФП, как 99тТс-пертехнетат и 1231-натрия йодид (сцинтиграфия щитовидной железы), коллоиды, меченные 99тТс
(лимфосцинтиграфия: лимфокартирование и поиск «сторожевого» лимфатического узла), меченный 99тТс макроагрегат альбумина человеческой сыворотки (исследование перфузии легких при диагностике тромбоэмболии легочной артерии), 99mTc-HMPAO (исследование перфузии головного мозга). К наиболее широко известным исследованиям с тумотропными РФП относятся сцинтиграфия с 67Gа-цитратом (диагностика злокачественных лимфом), с 123I- метайодбензилгуанидином (МИБГ) (диагностика нейробластомы, феохромоцитомы и параганглиомы), с 111Inоктреотидом (диагностика карциноидов, нейроэндокринных опухолей поджелудочной железы), с 99mТс-технетрилом (MIBI) (диагностика опухолей молочной железы, аденомы и рака паращитовидных желез).
Существует условное деление методов получения диагностических изображений на 3 уровня по рекомендациям ВОЗ (Серия технических докладов 795), позволяющее судить об оснащенности медицинских учреждений, но не об их специализированности.
Уровень I:
•стандартная рентгенография;
•УЗИ общего назначения;
•линейная томография;
•рентгенотелевизионное просвечивание. Уровень II:
•специальные методики рентгенографии;
•допплерография и другие специальные методики УЗИ;
•маммография;
•ангиография;
•КТ;
•радионуклидная сцинтиграфия.
Уровень III:
•МРТ;
•ПЭТ;
•иммуносцинтиграфия.
9. Роль морфологических методов исследования в онкологии. Способы взятия материала для цитологического и гистологического исследований.
•По способу получения материала
•Забор материала для гистологического исследования
•Эксцизионная биопсия — забор для исследования патологического образования целиком.
•Инцизионная биопсия — забор для исследования части патологического образования либо диффузно измененного органа.
•Щипковая биопсия — с помощью биопсийных щипцов (punch-biopsy)
•Трепан-биопсия — забор столбика плотной ткани с помощью полой трубки с заострённым краем — трепана. Применяется для биопсии костей и плотных опухолей.
•Сердцевинная (core-биопсия, кор-биопсия, режущая биопсия) — забор столбика материала из мягких тканей при помощи специального трепана, состоящего из гарпунной системы и полой трубки с заострённым краем.
•Скарификационная (поверхностная) биопсия (shaving biopsy) — забор материала путём срезания с поверхности образования тонкого пласта ткани, применяется для биопсии патологических образований кожи.
•Петлевая биопсия — забор материала петлей при помощи коагулятора в режиме резания тканей либо радиочастотного хирургического аппарата. Применяется в ЛОР, гинекологии и при эндоскопических исследованиях.
•Забор материала для цитологического исследования
•Отпечаток с патологического образования (эрозии, язвы) — материал переносится на предметное стекло прикладыванием его к изъязвленной поверхности.
•Мазок-отпечаток с патологического образования — материал соскребается с патологического образования шпателем, скальпелем, цитощёткой затем переносится на предметное стекло.
•Тонкоигольная аспирационная биопсия (FNAB) — забор материала для исследования обычно с помощью пункционной иглы и шприца. Применяется как для биопсии кистозных образований, так и солидных опухолей.
•Аспирационная биопсия — вариант FNAB жидкостных образований: кист, забора жидкости из плевральной либо брюшной полости.
•По виду контроля точности:
•Классическая биопсия
•Прицельная биопсия
•Эндоскопическая
•Биопсия под контролем УЗИ
•Биопсия под рентгенологическим контролем
•Стереотаксическая биопсия

10. Факторы, способствующие развитию злокачественных опухолей. Первичная профилактика рака.
Природные условия среды обитания, генетические особенности этнических групп, населяющих определенную географическую зону, религиозные традиции, традиционные привычки питания - это далеко не весь перечень факторов, воздействующих на население и определяющих возрастные закономерности и структурные соотношения различных форм злокачественных новообразований. Многие факторы риска возникновения и развития новообразований обусловлены региональными особенностями условий жизни населения. Замечено, что у людей, проживающих в теплых климатических условиях, чаще наблюдаются системные заболевания (лейкозы, злокачественные лимфомы). По мнению исследователей, они обусловлены инициирующим влиянием вирусов и микроорганизмов, что связывают с благоприятными условиями для обитания и размножения инициирующих агентов. На показателях заболеваемости отражаются также стиль жизни и правила поведения людей, связанные с их религиозными убеждениями. Так, у мормонов, адвентистов, отказавшихся от употребления табака и алкоголя по религиозным соображениям, отмечается низкий уровень заболеваемости злокачественными новообразованиями отдельных локализаций.
Наследственный фактор в возникновении злокачественных новообразований не означает, что рак наследуется из поколения в поколение. При отягощенном злокачественными новообразованиями анамнезе по наследству передается повышенная чувствительность к воздействию некоторых канцерогенных агентов. Наследственная восприимчивость изучена и доказана лишь для некоторых заболеваний, при которых вероятность заболеть при наличии генетической предрасположенности составляет 80-90 %. Это редкие формы злокачественных новообразований - ретинобластома, меланома кожи, саркома сосудистой оболочки глаза и доброкачественные новообразования, такие, как пигментная ксеродерма, опухоли каротидных телец, полипоз кишечника, нейрофиброматоз. Описано много семей, где у трех кровных родственниц и более встречался рак одной и той же локализации (в частности, рак тела матки или рак
яичников). При углубленном изучении злокачественных новообразований, связанных с наследственной предрасположенностью, было выявлено наличие унаследованного генетического дефекта, который в условиях нарушенного гомеостаза, под воздействием модифицирующих факторов окружающей среды и образа жизни организма, способствовал развитию рака или саркомы. В настоящее время выявлено 38 мутаций гена BRCA1, тесно сцепленных с развитием опухолей молочной железы. Иммунодефицитные синдромы: синдром Вискотта-Олдрича, атаксия-телеангиэктазия, Х-связанный рецессивный признак и др. определяют предрасположенность к развитию новообразований лимфоретикулярной ткани. Генетически обусловленные дерматозы: пигментная ксеродерма, альбинизм, врожденный дискератоз, синдром Вернера. Эти синдромы наследуются по аутосомно-рецессивному типу и определяют предрасположенность к злокачественным новообразованиям кожи.
Патологическая активность периферических эндокринных желез, нарушение регулирующей функции нервной системы и сдвиг метаболических процессов в тканях и органах организма способствуют образованию эндогенных канцерогенных веществ. При изучении гормонального канцерогенеза выявлено, что эстрогены в определенных условиях не только усиливают пролиферативные процессы в тканях, но и оказывают генотоксическое действие. Курение отнесено Международным агентством по изучению рака к группе абсолютных канцерогенов. Свыше 90 % всех случаев рака легкого у мужчин и 78 % у женщин связаны с курением. У активных курильщиков курение сигарет маскирует хронический неспецифический, а часто и специфический воспалительный трахеобронхит, который при частых обострениях вызывает атипию клеток эпителия. При активном и пассивном курении сигарет табачный дым, содержащий наиболее активные ПАУ (3,4-бензпирен), ароматические амины, нитрозосоединения, неорганические вещества - радий, мышьяк, полоний и радиоактивный свинец, при непосредственном соприкосновении с внутренней стенкой бронхов и альвеолами способствует взаимовоздействию канцерогенов с мембраной чувствительных к канцерогенам клеток, повышая вероятность опухолевой трансформации. Часть канцерогенов попадает в желудок со слюной, а канцерогены с инертной способностью диффундируют в межтканевую жидкость и растворяются в крови, повышая содержание канцерогенных веществ в организме. Доказано, что никотин, специфически блокируя симпатические ганглии, вызывает снижение локального иммунитета в респираторном тракте, но сам не оказывает канцерогенного действия.
Ультрафиолетовая (УФ) часть солнечного света, занимающая диапазон 2800-3400 А, обладает способностью проникать в ткани человека через кожный покров и повреждать клетки различных слоев кожи в зависимости от длины волны. В настоящее время известно, что до 95 % случаев рака кожи возникает на открытых участках тела, подвергающихся длительному воздействию УФ-лучей. Резистентность кожи к канцерогенному воздействию солнечной радиации определяется содержанием в ней пигмента - меланина, который, поглощая УФ-лучи, препятствует их проникновению в глубину тканей. Под воздействием УФ-излучения меланоциты не только синтезируют меланин, но и начинают размножаться. предрасположенность к возникновению новообразований у людей с более светлой кожей (блондины) - с содержанием пигмента только в клетках базального слоя эпидермиса. Проблема изучения радиационного воздействия на человека и соблюдение мер предосторожности от возможного облучения становятся все более актуальными. Это связано с массовым практическим применением во всех сферах человеческой деятельности современных средств научно-технических достижений, основанных на действии ионизирующего излучения по принципу квантового усиления. Излучение вызывает в клетках ионизацию, расщепляя молекулы клеток на ионы, в результате чего одни атомы теряют электроны, а другие присоединяют их, образуя отрицательно и положительно заряженные ионы. Наиболее чувствительны к воздействию ионизирующего фактора ткани в период пролиферативной активности клеток, активного роста и развития.
1)α-частицы больших размеров, которые несут в себе положительный электрический заряд и обладают высокой токсичностью для живых клеток; α-частицы обладают почти нулевой проникающей силой. Но при введении в
организм α-излучателей алиментарным или парентеральным путем они способны высвобождаться в глубоколежащих тканях;
2)β-частицы, которые несут в себе отрицательный заряд и, проникая на глубину 5 мм, оказывают разрушающее действие на живые клетки;
3)γ-лучи, воздействие которых на клетки менее токсично, а их проникающая способность зависит от интенсивности облучения;
4)нейтроны, образующиеся в результате распада ядер, обладают способностью глубоко проникать в живые клетки. Активные вещества при столкновении с нейтронами начинают вторично излучать α-, β-частицы и (или) γ-лучи. Вирусный канцерогенез - это сложный процесс опухолеобразования, основанный на взаимодействии геномов клетки и онкогенного вируса. Согласно вирусно-генетической теории Л.А. Зильбера, любая клетка потенциально может образовывать вирус, так как содержит необходимую для этого информацию; она находится в генетическом аппарате (в ДНК-хромосомах) клетки. Этиологическое значение экзогенных онкогенных вирусов уже доказано для некоторых форм злокачественных новообразований.
1. Человеческие папилломавирусы являются одними из ведущих этиологических факторов возникновения цервикально-интраэпителиальной неоплазмы (CIN) и рака шейки матки. Известно около 74 генотипов HPV. Из них выделяют:
—доброкачественные (типы 6 и 11), с которыми связывают появление остроконечных кондилом аногенитальной области и других доброкачественных поражений;
— злокачественные (типы 16, 18, 31, 33, 35, 52), которые чаще выявляют у больных с цервикально-эпителиальной неоплазмой и генитальным раком.
Вирус папилломы человека (ВПЧ), тип 16, связывают с развитием рака вульвы, влагалища, ануса, пищевода, миндалин.
Вирусологические и электронно-микроскопические методы позволили выявить опухоли человека, ассоциированные с герпесвирусом: лимфома Беркитта, назофарингеальный рак и рак шейки матки. Вирус гепатита, повреждая гепатоциты, является частым фактором в развитии гепатоцеллюлярного рака.
Человеческий вирус Т-клеточной лейкемии
В настоящее время известны веские аргументы в пользу вирусного происхождения лимфогранулематоза, саркомы Капоши, меланомы, глиобластомы.
Особо следует отметить роль в канцерогенезе микробных агентов, в частности бактерии Helicobacter pylori (H. pylori). Эпидемиологические исследования, подтверждающие увеличение частоты случаев рака желудка, ассоциированного с H. pylori, определили их инициирующую роль в процессе канцерогенеза. В 1994 г.
Международное агентство по изучению рака отнесло эту бактерию к канцерогенам первого класса и определило ее как причину развития рака желудка у человека.
Самые распространенные химические вещества с наибольшей канцерогенной активностью следующие:
1)ПАУ - 3,4-бензпирен, 20-метилхолантрен, 7,12-ДМБА;
2)ароматические амины и амиды, химические красители - бензидин, 2-нафтиламин, 4-аминодифенил, 2- ацетиламинофлюорен и др.;
3)нитрозосоединения - алифатические циклические соединения с обязательной аминогруппой в структуре: нитрометилмочевина, ДМНА, диэтилнитрозамин;
4)афлотоксины и другие продукты жизнедеятельности растений и грибов (циказин, сафрол и т.д.);
5)гетероциклические ароматические углеводороды - 1,2,5,6- и 3,4,5,6-дибензкарбазол, 1,2,5,6-дибензакридин;
6)прочие (эпоксиды, металлы, пластмассы).
Большинство химических канцерогенов активизируются в организме при метаболических реакциях. Они называются истинными или конечными канцерогенами. Другие химические канцерогены, которые не нуждаются в предварительных превращениях в условиях организма, называются прямыми.
Основными источниками распространения канцерогенов являются предприятия черной и цветной металлургии, химической, нефтехимической, нефтяной, газовой, угольной, мясной, целлюлозно-бумажной промышленности, предприятия сельского и коммунального хозяйства. Содержание загрязнителей в атмосферном воздухе, воздухе производственных помещений, жилищ и общественных зданий обусловливает преимущественно ингаляционное воздействие веществ на организм. Водные загрязнители действуют на организм при пероральном поступлении с питьевой водой и через кожу - при использовании воды в целях личной гигиены. Кроме того, пероральное поступление веществ в организм имеет место при употреблении в пищу рыбы, морской капусты, а также сельскохозяйственных растений и мяса животных (химические вещества попадают в них при загрязнении почвы). В быту человек контактирует с химическими веществами, источниками которых являются строительные и отделочные материалы, краски, предметы бытовой химии, лекарственные средства, продукты неполного сгорания природного газа и т.д.
Комплекс социально-гигиенических мероприятий, направленных на максимальное снижение воздействия канцерогенных факторов внешней среды на чувствительные к ним клетки живого организма, а также стабилизация иммунологического статуса организма путем неспецифического воздействия на человека (пропаганда здорового образа жизни, правильного питания, отказ от вредных привычек и т.д.) называется первичной профилактикой злокачественных новообразований. Комплекс медицинских мероприятий, направленных на выявление больных с предраковыми заболеваниями, с последующим их оздоровлением и наблюдение за ними называется вторичной профилактикой. Организация и проведение мероприятий по ранней диагностике рака также рассматриваются как компонент вторичной профилактики, а предупреждение рецидива рака как третичная профилактика рака.
Индивидуальная защита организма от злокачественных новообразований должна включать:
1)соблюдение правил личной гигиены;
2)безотлагательную лечебную коррекцию нарушенных функций организма;
3)правильное рациональное питание;
4)отказ от вредных привычек;
5)оптимизацию функций репродуктивной системы;
6)ведение здорового активного образа жизни;
7)высокое самосознание человека - четкое знание факторов канцерогенного воздействия на организм и мер предосторожности, знание особенностей течения, стадийности и зависимости эффективности лечения опухолей от своевременности их выявления.
С целью выработки у курильщиков индивидуальных мер защиты производители табачных изделий стали выпускать сигареты с фильтрами и дозиметрами. Предполагалось, что предупредительная надпись на пачках сигарет: «Курение опасно для вашего здоровья», а в некоторых случаях и изображения фотографий с лицами умерших от рака легкого окажут психологическое воздействие на самосознание курильщиков.
Административные органы, действующие на основе федерального закона о борьбе с курением, запрещают курение табака в общественных местах для предотвращения вредного воздействия табачного дыма на людей, вынужденных вдыхать загрязненный дымом воздух, состоящий в основном из канцерогенных нитрозоаминов.
Антиканцерогенным эффектом обладают антиоксиданты, соли селена. К антиоксидантам относится широкий спектр биологически активных веществ, содержание которых в пище очень важно для профилактики рака, -
токоферол, фосфолипиды, убихиноны, витамины группы K, флавоноиды. Учитывая антиканцерогенное действие перечисленных ингредиентов и важность их содержания в употребляемой пище для снижения риска возникновения рака, необходимо потреблять больше продуктов растительного происхождения. Профилактической мерой для снижения риска возникновения рака служит исключение из пищевого рациона (или ограничение) продуктов, содержащих большое количество канцерогенов, - копченостей, маринадов, пищи, приготовленной с применением ранее использованного жира, консервов.
Специфические рекомендации по питанию:
—поступление калорий от сжигания жира не должно превышать 30 % общей энергетической ценности пищи, в том числе менее 10 % должны обеспечивать насыщенные жиры, 6-8 % - полиненасыщенные жиры, 2-4 % - мононенасыщенные;
—следует потреблять разнообразные свежие овощи и фрукты несколько раз в день;
—необходимо сбалансировать физическую нагрузку и рацион для сохранения нормальной массы тела;
—ограничить потребление соли, пищи, консервированной с помощью нитритов, нитратов и соли. Норма потребления соли - не более 6 г в день;
—ограничить потребление алкогольных напитков.
11. Роль экзогенных (химические и физические агенты, онковирусы) и эндогенных (факторов в возникновении опухолей человека.
Выделяют 3 категории химических соединений, групп соединений и производственных процессов в зависимости от степени их канцерогенности.
•Группа 1. Вызывают ЗН у человека (получены достоверные эпидемиологические доказательства причинной связи между воздействием и ЗН). К этой группе относят бензол, хром, некоторые нефтепродукты, бериллий, мышьяк, никель, кадмий, диоксины.
•Группа 2. Возможно, канцерогенны для человека (кобальт, свинец, цинк, никель, продукты переработки
нефти, формальдегид).
• Группа 3. Канцерогенность для человека не доказана. Основные источники загрязнения атмосферного воздуха, почвы,водных бассейнов - предприятия металлургической, коксохимической, нефтеперерабатывающей, химической, целлюлозно-бумажной промышленности, а также транспорт. Поступление канцерогенных веществ в организм происходит ингаляционным путём, а также с пищей и водой.
Этанол - наиболее мощный канцерогенный агент, сознательно потребляемый человеком. Связь употребления алкоголя с повышенным риском развития ЗН полости рта, глотки, пищевода, гортани, печени, молочной железы, лёгкого, толстой кишки подтверждена материалами многочисленных эпидемиологических исследований. Канцерогенами являются как крепкие, так и слабоалкогольные напитки.
12. Принципы патогенеза злокачественных новообразований. Опухолевые стволовые клетки.
Опухолевый процесс - это процесс, сопровождающийся прибавлением клеточной массы. Для новообразований характерен автономный тип роста. В норме количество клеток регулируется посредством точной балансировки двух противоположных процессов - клеточного деления и клеточной элиминации. При онкологическом заболевании прибавление клеточной массы опережает клеточную гибель либо за счет активации процессов пролиферации, либо вследствие угнетения процессов апоптоза, а чаще всего - при сочетанном нарушении этих процессов. Существенно, что дисбаланс регуляции количества клеток вызван неспособностью трансформированного клона реагировать на внешние сигналы; таким образом, объем клеточной массы перестает зависеть от потребностей организма, что и подразумевается под понятием «автономность».
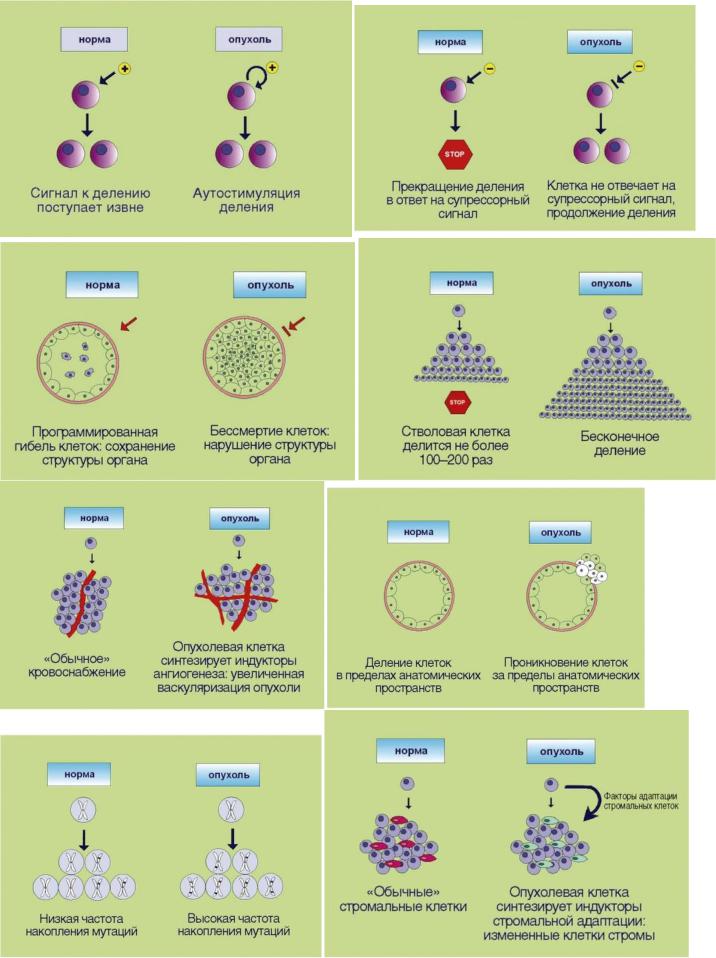
В настоящее время существуют различные теории и гипотезы онкогенеза - наследственная, химическая, вирусная, хромосомная и т.д., из которых ни одна пока не может считаться единой, общепринятой. Все теории отражают лишь различные стороны одного процесса - повреждения генома клетки.
К настоящему времени доказано, что любая живая клетка содержит в структуре ДНК протоонкогены. Это участки генома клетки, некие полипептидные соединения, которые при тех или иных условиях переходят в активную форму - онкогены. Последние, в свою очередь, обусловливают бласттрансформацию клетки (злокачественное перерождение, канцерогенез), которая дает начало росту опухоли. Факторов, способствующих переходу протоонкогена в активную форму, великое множество - химикаты, радиация, инсоляция, вирусы и т.п.
Процесс онкогенеза имеет свои закономерности и стадии. Основные стадии таковы: инициация, промоция, деление измененной клетки и, наконец, собственно рост опухоли. В фазу инициации происходят необратимые нарушения генотипа клетки: мутации, хромосомные перестройки, клетка становится предрасположенной к трансформации. Этот скрытый период имеет разную длительность и различный исход. Такая клетка может остаться и какое-то время существовать среди неизмененных клеток, может погибнуть, не превратившись в опухолевую. Далее на этой же доклинической стадии по завершении фазы инициации наступает фаза промоции. Происходит усиленная трансформация протоонкогенов в онкогены. Вторая фаза характерна тем, что клетка приобретает фенотип, соответствующий измененному генотипу. Фенотип трансформированной клетки реализуется в процессе ее жизнедеятельности в виде атипии, той или иной степени внешних изменений. Этот этап также обратим, клетка может вернуться к нормальному фенотипу. Чтобы трансформированный фенотип стал устойчивым, необходимо длительное воздействие канцерогенов.
Инициация и промоция обусловлены действием канцерогенов внешней или внутренней среды. Вторая фаза доклинического рака завершается делением такой трансформированной клетки. Это и есть начало роста собственно опухоли, который почти сразу приобретает автономный характер. Следующий этап - закрепление нарушенного генотипа в дочерних клетках - клонирование.
Значительная роль на этом этапе принадлежит ангиогенезу, что обеспечивает поступление питательных веществ к месту развития опухоли. Этот процесс зависит от выработки соответствующего фактора роста эндотелия сосудов. Выработка ферментов, называемых металлопротеиназами, разрушает межклеточное вещество. На этом месте происходят рост сосудов и усиленное размножение измененных клеток, наступает собственно фаза опухолевого роста. Колония опухолевых клеток получает условия для дальнейшего роста и распространения и выхода из первичного очага. Накопление массы опухоли происходит не только за счет интенсивного размножения клеток, но и за счет более длительного срока жизни, а также за счет усиленного обеспечения опухоли пластическими средствами, что происходит за счет процессов неоангиогенеза.
13. Злокачественные опухоли как социальная проблема. Канцерогенные вещества во внешней среде, их основные источники.
Злокачественные новообразования представляют собой проблему высокой социальной значимости, так как приводят к утрате трудоспособности и инвалидизации значительной части населения.
См выше
14. Лучевая терапия как метод лечения злокачественных новообразований. Виды лучевой терапии.
Лучевая терапия представляет собой прикладную медицинскую дисциплину, в основе которой лежит использование различных видов ионизирующего излучения. Лучевую терапию применяют как самостоятельный метод или в составе комбинированного и комплексного лечения (в сочетании с хирургическим или лекарственным). За последние десятилетия она претерпела существенные изменения, позволившие значительно расширить показания и улучшить результаты ее применения. В настоящее время лучевой терапии подвергается 60-70 % всех онкологических больных. При правильном назначении и проведении облучение приводит к стойкому излечению почти половины пациентов. При неустойчивом соотношении протонов и нейтронов образуются радиоактивные элементы. Большая часть радиоактивных изотопов, используемых в медицине, создается искусственно на реакторах или циклотроне.
В современной лучевой терапии применяют разнообразные виды излучений, различающихся по биологическому воздействию, проникающей способности и распределению энергии в пучке излучения. В клинической практике применяют фотонное и корпускулярное ионизирующее излучение.
Фотонное излучение представляет собой электромагнитные колебания, характеризующиеся различной частотой и длиной волны. К нему относятся:
1)γ-излучение (электромагнитное излучение естественных или искусственно получаемых радионуклидов, способное проникать на глубину 1 м и более);
2)рентгеновское излучение (электромагнитное излучение, образующееся при переходе электронов между орбитами внутри ядра, которое получают с помощью рентгеновских аппаратов);
3)тормозное излучение (электромагнитное излучение, получаемое с помощью ускорителей электронов при энергиях, достигающих десятков мегаэлектронвольт - МэВ); Корпускулярное излучение представляет собой поток ядерных частиц. К этому виду ионизирующего излучения относятся:
1)β-излучение (корпускулярное излучение потока отрицательно заряженных электронов, способного проникать в ткани на глубину от нескольких миллиметров до 1 см);
2)позитронное излучение (корпускулярное излучение потока положительно заряженных частиц, равных по массе электронам). Позитроны также могут проникать в ткани на глубину до нескольких миллиметров;
3)α-частицы (корпускулярное излучение ядер атомов гелия, состоящих из двух нейтронов и двух протонов и способных распространяться в тканях на глубину 10-20 клеток).
К основным источникам ионизирующего излучения относятся:
•радиоактивные вещества (естественные или искусственно получаемые радионуклиды);
•специальные электрофизические аппараты (рентгеновские аппараты, ускорители электронов и протонов, генераторы нейтронов).
Для дистанционного облучения применяют рентгеновские аппараты (с энергией 60-100 кэВ), гамма-аппараты «Агат» и «Рокус». Аппараты имеют радиационную головку, которая может вращаться вокруг больного, что облегчает его укладку и центрацию пучка излучения. Дальнодистанционное тормозное и электронное облучение осуществляется с помощью линейных ускорителей электронов и циклотронов (бетатроны, микротроны). Электронное излучение с энергией 20-30 МэВ имеет преимущество по сравнению с рентгеновским при облучении поверхностных очагов.
Наиболее распространенным источником как дистанционного, так и контактного облучения является радиоактивный изотоп кобальта (60Co), период полураспада которого составляет 5,24 года. Помимо него, для контактных методов лучевой терапии используются радиоактивные изотопы цезия (137Cs), иридия (192Ir), золота (198Au), свинца (32P), иода (132I) и др. Выделяют закрытые и открытые источники контактного облучения. Закрытые радиоактивные источники (60Со, 137Cs, 192Ir, 198Au), имеющие вид проволоки, игл, шариков, вводят в полости или ткани непосредственно или через проводники. Открытые источники (32P, 132I, 198Au) вводят в организм больного в виде водных или коллоидных растворов per os, внутривенно или интратуморально.
В настоящее время облучение проводится двумя основными способами.
1.Дистанционное облучение, при котором источники излучения находятся на расстоянии 80-100 см от больного. К дистанционному облучению относятся рентгенотерапия, гамма-терапия, протонная и нейтронная терапия, а также облучение быстрыми электронами.
2.Контактное облучение (брахитерапия), при котором источники излучения находятся в непосредственной близости от больного (на расстоянии, не превышающем 30 см) или контактируют с опухолью. При контактном облучении относительно высокая доза может быть доставлена к ограниченному объему пораженной ткани.
К основным видам контактного облучения относятся:
а) внутриполостное, при котором источники излучения вводят в естественные (полость рта, мочевого пузыря, матки или влагалища, прямой кишки, пищевода) или искусственные (послеоперационная рана) полости; б) внутритканевое (или интерстициальное), при котором закрытые или открытые источники излучения помещаются
через специальный катетер в опухоль. Наиболее часто интерстициальная брахитерапия с радиоактивным 137Cs применяется в лечении злокачественных новообразований головы и шеи, а также сарком мягких тканей;
в) аппликационное, при котором источники излучения (β-аппликаторы, содержащие 90Sr и 90Y, γ-аппликаторы, содержащие 60Co) помещают на поверхность тела больного;
г) внутреннее (или системное), при котором открытые радионуклиды (например, 131I, 198Au) вводят внутривенно или перорально.
Для определения количества радионуклида и силы его воздействия на ткани используют следующие понятия:
•экспозиционная доза (Х), характеризующая энергию фотонного излучения, затраченную на ионизацию массы сухого воздуха (измеряется в рентгенах);
•поглощенная доза (D), характеризующая количество энергии, переданной облучаемому объекту, приходящейся на единицу его массы. В современной медицинской радиологии единицей поглощенной дозы является 1 Грей (Гр). При поглощении дозы 1 Гр облучаемому веществу массой 1 кг передается энергия, равная 1 Дж. Мощность поглощенной дозы соотнесена с единицей времени (1 Гр/с). Для измерения поглощенной дозы используется и внесистемная единица - рад (1 Гр = 100 рад).
