
- •2. Строение ферментов
- •3. Множественные формы ферментов.
- •6. Механизм действия ферментов
- •1. Роль металлов в присоединении субстрата в активном центре фермента
- •2. Роль металлов в стабилизации третичной и четвертичной структуры фермента
- •3. Роль металлов в ферментативном катализе
- •4. Роль металлов в регуляции активности ферментов
- •8. Основы кинетики ферментативных реакций
- •Регуляция активности ферментов
- •1. Доступность субстрата или кофермента
- •2. Компартментализация
- •3. Генетическая регуляция
- •4. Ограниченный (частичный) протеолиз проферментов
- •5. Аллостерическая регуляция
- •6. Белок-белковое взаимодействие
- •7. Ковалентная (химическая) модификация
- •12. Применение ферментов в медицине
- •Основная роль цтк заключается в
- •5. Анаболизм
- •Катаболизм
- •Моносахариды
- •2. Олигосахариды
- •3. Полисахариды или полиозы
- •Эпидемиология галактоземии
- •Чем вызывается галактоземия?
- •Симптомы галактоземии
- •Дефицит галактозо-1-фосфатуридилтрансферазы
- •Дефицит галактокиназы
- •Дефицит уридилдифосфат-галактозо-4-эпимеразы
- •Классификация галактоземии
- •Диагностика галактоземии
- •Гликоген печени. Концентрация глюкозы в крови
- •Регуляция концентрации глюкозы в крови
- •8. Гипергликемия
- •9. Нарушения регуляции углеводного обмена
- •10. Гликолиз
- •Распад гликогена (гликогенолиз)
- •1. Этапы аэробного гликолиза
- •2. Реакции аэробного гликолиза
- •3. Окисление цитоплазматического nadh в митохондриалъной дыхательной цепи. Челночные системы
- •4. Баланс атф при аэробном гликолизе и распаде глюкозы до со2 и н2о
- •14. Переключение между аэробным и анаэробным окислением происходит автоматически
- •Эффект Пастера
- •15. Глюконеогенез
- •17. Пентозофосфатный путь окисления углеводов
3. Множественные формы ферментов.
ИЗОФЕРМЕНТЫ
Изоферменты, или изоэнзимы,– это множественные формы фермента, катализирующие одну и ту же реакцию, но отличающиеся друг от друга по физическим и химическим свойствам, в частности по сродству к субстрату, максимальной скорости катализируемой реакции (активности), электрофоретической подвижности или регуляторным свойствам.
В живой природе имеются ферменты, молекулы которых состоят из двух и более субъединиц, обладающих одинаковой или разной первичной, вторичной или третичной структурой. Субъединицы нередко называют протомерами, а объединенную олигомерную молекулу – мультимером
Виды изоферментов:
-
Органные — ферменты гликолиза в печени и мышцах.
-
Клеточные — малатдегидрогеназа цитоплазматическая и митохондриальная (ферменты разные, но катализируют одну и ту же реакцию).
-
Гибридные — ферменты с четвертичной структурой, образуются в результате нековалентного связывания отдельных субъединиц (лактатдегидрогеназа — 4 субъединицы 2 типов).
-
Мутантные — образуются в результате единичной мутации гена.
-
Аллоферменты — кодируются различными аллелями одного и того же гена.
Термин «множественные формы фермента» применим к белкам, катализирующим одну и ту же реакцию и встречающимся в природе в организмах одного вида. Термин «изофермент» применим только к тем множественным формам ферментов, которые появляются вследствие генетически обусловленных различий в первичной структуре белка (но не к формам, образовавшимся в результате модификации одной первичной последовательности).
Собственно множественные формы (истинные) — это ферменты, синтез которых кодируется одним и тем же аллелем одного и того же гена, у них одинаковая первичная структура и свойства, но после синтеза на рибосомах они подвергаются модификации и становятся разными, не смотря на то, что и катализируют одну и ту же реакцию.
4. Тип катализируемой химической реакции в сочетании с названием субстрата (субстратов) служит основой для систематического наименования ферментов. Согласно международной классификации, ферменты делят на шесть главных классов по механизму действия, в каждом из которых несколько подклассов: 1) оксидоредуктазы; 2) трансферазы; 3) гидролазы; 4) лиазы; 5) изомеразы; 6) лигазы (синтетазы).

Оксидоредуктазы. К классу оксидоредуктаз относят ферменты, катализирующие с участием двухсубстратов окислительно-восстановительные реакции, лежащие в основе биологического окисления. Систематические названия их составляют по форме «донор: акцептор оксидоредуктаза». Например, лактат: НАД+ оксидоредуктаза для лактатдегидрогеназы (ЛДГ).
Различают следующие основные оксидоредуктазы: аэробные дегидрогеназы или оксидазы, катализирующие перенос протонов (электронов) непосредственно на кислород; анаэробные дегидрогеназы, ускоряющие перенос протонов (электронов) на промежуточный субстрат, но не на кислород; цитохромы, катализирующие перенос только электронов. К этому классу относят также гемсодержащие ферменты каталазу и пероксидазу, катализирующие реакции с участием перекиси водорода.
Трансферазы. К классу трансфераз относят ферменты, катализирующие реакции межмолекулярного переноса различных атомов, групп атомов и радикалов. Наименование их составляется по форме «донор: транспортируемая группа – трансфераза».
Различают трансферазы, катализирующие перенос одноуглеродных остатков, ацильных, гликозильных, альдегидных или кетонных, нуклеотидных остатков, азотистых групп, остатков фосфорной и серной кислот и др. Например: метил- и формилтрансферазы, ацетилтрансферазы, амино-трансферазы, фосфотрансферазы и др.
Гидролазы. В класс гидролаз входит большая группа ферментов, катализирующих расщепление внутримолекулярных связей органических веществ при участии молекулы воды. Наименование их составляют по форме «субстрат-гидролаза». К ним относятся: зстеразы – ферменты, катализирующие реакции гидролиза и синтеза сложных эфиров; гликозидазы, ускоряющие разрыв гликозидных связей;фосфатазы и пептидгидролазы, катализирующие гидролиз фосфоангидридных и пептидных связей; амидазы, ускоряющие разрыв амидных связей, отличных от пептидных, и др.
Лиазы. К классу лиаз относят ферменты, катализирующие разрыв химических связей без участия воды. Эти реакции сопровождаются образованием двойной связи или присоединением групп к месту разрыва двойной связи. Ферменты обозначают термином «субстрат-лиазы». Например, фумарат-гидратаза (систематическое название «L-малат-гидролаза») катализирует обратимое отщепление молекулы воды от яблочной кислоты с образованием фумаровой кислоты. В эту же группу входят декарбоксилазы (карбоксилиазы), амидин-лиазы и др.
Изомеразы. К классу изомераз относят ферменты, катализирующие изомерные превращения. Систематическое название их составляют с учетом типа реакции: «субстрат – цис-транс-изомераза». Если изомеризация включает внутримолекулярный перенос группы, фермент получает название «мутаза».
К этому же классу относят рацемазы и эпимеразы, действующие на амино- и оксикислоты, углеводы и их производные; внутримолекулярные оксидоредуктазы, катализирующие взаимопревращения альдоз и кетоз; внутримолекулярные трансферазы, переносящие ацильные, фосфорильные и другие группы, и т.д.
Лигазы (синтетазы). К классу лигаз относят ферменты, катализирующие синтез органических веществ из двух исходных молекул с использованием энергии распада АТФ (или другого нуклеозидтрифосфата). Систематическое название их составляют по форме «X : Y лигаза», где X и Y обозначают исходные вещества. В качестве примера можно назвать L-глутамат: аммиак лигазу (рекомендуемое сокращенное название «глутаминсинтета-за»), при участии которой из глутаминовой кислоты и аммиака в присутствии АТФ синтезируется глутамин.
5. ОСНОВНЫЕ СВОЙСТВА ФЕРМЕНТОВ
К ферментам применимы три основных критерия, характерных и для неорганических катализаторов. В частности, они остаются неизмененными после реакции, т.е. освобождаясь, могут вновь реагировать с новыми молекулами субстрата (хотя нельзя исключить побочных влияний условий среды на активность фермента). Ферменты способны оказывать действие в ничтожно малых концентрациях (например, одна молекула фермента реннина, содержащегося в слизистой оболочке желудка теленка, створаживает около 106 молекул казеиногена молока за 10 мин при температуре 37°С).
Наличие либо отсутствие фермента или любого другого катализатора не оказывает влияния на величину константы равновесия и свободной энергии (ΔG). Катализаторы лишь повышают скорость, с которой система приближается к термодинамическому равновесию, не сдвигая точки равновесия. Химические реакции с высокой константой равновесия и отрицательной величиной ΔG принято называть экзергоническими. Реакции с низкой константой равновесияи соответственно положительной величиной ΔG (они обычно не протекают спонтанно) называются эндерго-ническими. Для начала и завершения этих реакций необходим приток энергии извне. В живых системах экзергонические процессы обычно сопряжены с эндергоническими реакциями, обеспечивая последние необходимым количеством энергии.
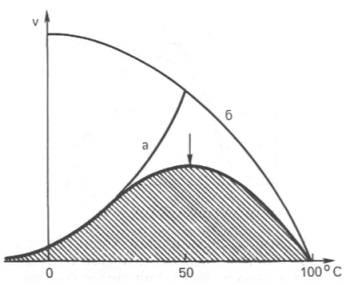
Рис. 4.16. Зависимость скорости катализируемой ферментом реакции от температуры.
а - повышение скорости реакции как функция температуры; б - снижение скорости реакции как функцияденатурации белка-фермента; стрелка указывает оптимум температуры.
Ферменты, являясь белками, обладают рядом характерных для этого класса органических соединений свойств, отличающихся от свойств неорганических катализаторов.
Термолабильность ферментов. Скорость химических реакций зависит от температуры, поэтому катализируемые ферментами реакции также чувствительны к изменениям температуры. Установлено, что скорость большинства биохимических реакций повышается в 2 раза при повышении температуры на 10°С и, наоборот, снижается в 2 раза при понижении температуры на 10°С. Этот показатель получил название температурного коэффициента. Однако вследствие белковой природы фермента тепловая денатурация при повышении температуры будет снижать эффективную концентрацию фермента с соответствующим снижением скорости реакции. Так, при температуре, не превышающей 45–50°С, скорость реакции увеличивается согласно теории химической кинетики. При температуре выше 50°С на скорость реакциибольшое влияние начинает оказывать тепловая денатурация белка-фермента, приводящая к полному прекращению ферментативного процесса
Зависимость активности ферментов от рН среды. Ферменты обычно наиболее активны в пределах узкой зоны концентрации водородных ионов, соответствующей для животных тканей в основном выработанным в процессе эволюции физиологическим значениям рН среды 6,0–8,0. При графическом изображении на кривой колоколообразной формы имеется определенная точка, в которой ферментпроявляет максимальную активность; эту точку называют оптимумом рН среды для действия данногофермента (рис. 4.17). При определении зависимости активности фермента от концентрации водородныхионов реакцию проводят при разных значениях рН среды, обычно при оптимальной температуре и наличии достаточно высоких (насыщающих) концентраций субстрата. В табл. 4.3 приводятся оптимальные значения рН среды для ряда ферментов.

Из данных табл. 4.3 видно, что рН-оптимум действия ферментов лежит в пределах физиологических значений. Исключение составляют пепсин, рН-оптимум которого 2,0 (при рН 6,0 он не активен и не стабилен). Объясняется это, во-первых, структурной организацией молекулы фермента и, во-вторых, тем, что пепсин является компонентом желудочного сока, содержащего свободную соляную кислоту, которая создает оптимальную кислую среду для действия этого фермента. С другой стороны, рН-оптимум аргиназы лежит в сильнощелочной зоне (около 10,0); такой среды нет в клетках печени, следовательно, in vivo аргиназа функционирует, по-видимому, не в своей оптимальной зоне рН среды.
