
- •Опыт 4. Свойства фенола
- •Лабораторная работа №3. Альдегиды и кетоны опыт 1. Реакции окисления альдегидов
- •Опыт 3. Получение и свойства предельных высших кислот и их солей
- •1. Пробирки (3 шт.).
- •Опыт 4. Сложные эфиры органических кислот. Реакция этерификации
- •2. Термометр.
- •4. Пробирки (2шт).
- •Опыт 5. Непредельные одноосновные карбоновые кислоты Свойства олеиновой кислоты
- •1. Пробирки (2шт).
- •Лабораторная работа №4. Азотсодержащие соединения опыт 1. Образование солей анилина
- •Опыт 2. Реакции на карбонильные группы в моносахаридах
- •Опыт 3. Реакция на гидроксильные группы дисахаридов. Реакция дисахаридов с гидроксидом меди (II) в щелочном растворе
- •1. Пробирки (2шт.).
- •Опыт 4. Реакции дисахаридов по карбонильным группам (сравнение свойств восстанавливающих и невосстанавливающих дисахаридов)
- •1. Пробирки (3 шт.).
- •Лабораторная работа № 6. Качественные реакции на аминокислоты и белки
- •Лабораторные работы по вмс углеводы
Опыт 3. Получение и свойства предельных высших кислот и их солей
Необходимые реактивы и оборудование
1. Пробирки (3 шт.).
2. Пипетки.
3. Мыло, стружки.
4. Мыло, 1%-ный раствор водный.
5. Мыло, спиртовой раствор.
6. Серная кислота Н2SО4, 10%-ный раствор.
7. Фенолфталеин, 1%-ный спиртовой раствор.
8. Подсолнечное масло.
Гидролиз натриевых солей высших жирных кислот (мыла)
В сухую пробирку налить 1 мл спиртового раствора мыла и прибавить несколько капель спиртового раствора фенолфталеина. Затем полученный бесцветный спиртовой раствор мыла, содержащий фенолфталеин, осторожно (по стенке) прилить в пробирку с водой. На границе раздела слоев воды и мыла появится кольцо малинового цвета.
Почему появляется окраска? Напишите уравнение реакции гидролиза мыла.
Выделение высших жирных кислот из мыла
В стакане растворить 1 г мыльной стружки в 4 мл дистиллированной воды. К полученному раствору прилить 1 мл 10%-ного раствора серной кислоты.
Что вы наблюдаете? Напишите уравнение реакции.
Смесь нагреть почти до кипения. Расплавившиеся жирные кислоты всплывают в виде слоя, затвердевающего при охлаждении пробирки. Какие высшие предельные кислоты входят в состав мыла?
К охлажденной смеси добавить 1 мл диэтилового эфира. Пробирку закрыть корковой пробкой и энергично встряхнуть. Водный слой становится прозрачней, жирные кислоты растворяются в эфире. Эфирный раствор осторожно с помощью пипетки перенести на часовое или предметное стекло. После испарения эфира на стекле остается осадок, напоминающий парафин.
Эмулъгирующие свойства мыла
В две пробирки налить по 2-3 капли подсолнечного масла. В одну из них прилить 2 мл дистилированной воды, а в другую – 2 мл 1%-ного раствора мыла. Энергично встряхнуть обе пробирки. В пробирке с мылом образуется довольно устойчивая молочно-белая эмульсия, в пробирке с водой капельки масла выделяются и постепенно всплывают: эмульсия масла в воде неустойчива. Моющие свойства мыла объясняются его эмульгирующими свойствами, понижающими поверхностное натяжение капелек масла. Это приводит к значительному увеличению устойчивости пены и эмульсии.
Опыт 4. Сложные эфиры органических кислот. Реакция этерификации
Необходимые реактивы и оборудование
1. Водяная баня.
2. Термометр.
3. Обратные холодильники к приборам.
4. Пробирки (2шт).
5. Спирт этиловый С2Н5ОН.
6. Уксусная кислота СН3СООН, ледяная.
7. Серная кислота H2SO4, концентрированная.
8. Хлорид натрия NaCl, насыщенный раствор.
9. Спирт изоамиловый (СН3)2СНСН2СН2ОН.
Получение этилацетата (уксусноэтилового эфира)
В сухой пробирке смешать 2 мл этилового спирта, 2 мл уксусной кислоты и 1 каплю концентрированной серной кислоты. Минеральные кислоты (серная, соляная) служат катализаторами реакции этерификации. Механизм реакции этерификации – см. //, 1972, с. 164; 1982, с. 157. Катализатор (ионы Н+) увеличивает электрофилъные свойства углерода карбоксильной группы.
Пробирку закрыть пробкой с обратным холодильником. Смесь в пробирке перемешать встряхиванием и нагреть в течение 8-10 мин в водяной бане при температуре воды 65-70°С. (Реакционная смесь не должна кипеть!) Затем пробирку охладить. Для выделения из раствора этилацетата к содержимому пробирки добавить 2-3 мл насыщенного раствора хлорида натрия (выслаивание). Этилацетат всплывает в виде бесцветной жидкости с приятным запахом.
Написать уравнение реакции образования этилацетата и рассмотреть механизм реакции этерификации. В чем заключается роль минеральной кислоты? Почему при добавлении избытка минеральной кислоты сложный эфир органической кислоты не образуется?
Получение изоамилацетата (уксусноизоамилового эфира)
В сухой пробирке смешать 2 мл изоамилового спирта, 2 мл ледяной уксусной кислоты и 1 каплю концентрированной серной кислоты. Пробирку соединить с обратным холодильником. Реакционную смесь нагревать в кипящей водяной бане 8-10 мин, после чего охладить и вылить в пробирку с холодной водой. Сложный эфир (изоамилацетат) всплывает. Обратите внимание на его запах. Пары изоамилацетата вызывают раздражение дыхательных путей, они могут вызвать кашель, поэтому нюхать изоамилацетат нужно осторожно.
Получение изоамилацетата (грушевой эссенции):
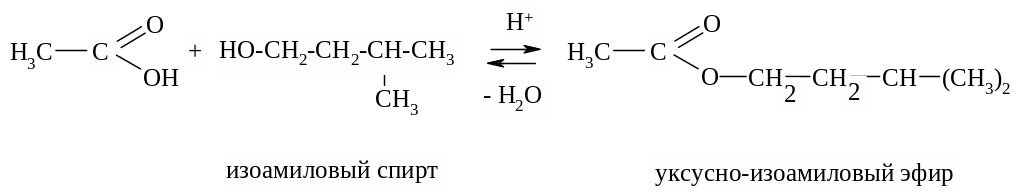
Многие сложные эфиры обладают приятным фруктовым запахом. Так, муравьино-амиловый эфир обладает запахом вишни, муравьино-этиловый – рома, уксусно-амиловый – бананов, масляно-этиловый – абрикосов, масляно-бутиловый – ананасов, изовалериано-этиловый – запахом яблок. Их широко применяют для приготовления фруктовых эссенций. Напишите структурные формулы всех перечисленных сложных эфиров.
