
- •И.М.Лузанова, е.Ю.Калинина, а.И.Сергеев
- •Оглавление
- •18.Фз № Об обращении лекарственных средств»……………………….Стр – 286
- •Всеобщая декларация прав человека
- •Преамбула
- •Статья 1
- •Статья 2
- •Статья 22
- •Статья 23
- •Статья 24
- •Статья 25
- •Статья 26
- •Статья 27
- •Статья 28
- •Статья 29
- •Статья 30
- •Декларация о политике в области обеспечения прав пациента в Европе
- •Основы концепции прав пациента в Европе: общие положения
- •Конвенция о защите прав человека и основных свобод
- •Статья1 Обязательство соблюдать права человека
- •Раздел I права и свободы Cтатья2 Право на жизнь
- •Статья3 Запрещение пыток
- •Статья4 Запрещение рабства и принудительного труда
- •Статья5 Право на свободу и личную неприкосновенность
- •Статья6 Право на справедливое судебное разбирательство
- •Статья7 Наказание исключительно на основании закона
- •Статья8 Право на уважение частной и семейной жизни
- •Статья9 Свобода мысли, совести и религии
- •Статья10 Свобода выражения мнения
- •Статья11 Свобода собраний и объединений
- •Статья22 Выборы судей
- •Статья23 Срок полномочий
- •Статья24 Освобождение от должности
- •Статья25 Секретариат и правовые референты
- •Статья26 Пленарные заседания Суда
- •Статья27 Комитеты, Палаты и Большая Палата
- •Статья28 Объявления комитетов о неприемлемости жалобы (заявления)
- •Статья29 Решения Палат о приемлемости жалобы и по существу дела
- •Статья35 Условия приемлемости
- •Статья36 Участие третьей стороны
- •Статья37 Прекращение производства по делу
- •Статья38 Процедура рассмотрения дела с участием заинтересованных сторон и процедура мирового соглашения
- •Статья44 Окончательные постановления
- •Статья45 Мотивировка постановлений и решений
- •Статья46 Обязательная сила и исполнение постановлений
- •Статья47 Консультативные заключения
- •Статья57 Оговорки
- •Статья58 Денонсация
- •Статья59 Подписание и ратификация
- •Международный кодекс медицинской этики
- •Кодекс врачебной этики рф
- •Федеральный закон «Об обязательном медицинском страховании»
- •Глава 1. Общие положения Статья 1. Предмет регулирования настоящего Федерального закона
- •Статья 2. Законодательство об обязательном медицинском страховании
- •Статья 3. Основные понятия и термины, используемые в настоящем Федеральном законе
- •Статья 4. Основные принципы осуществления обязательного медицинского страхования
- •Глава 2. Субъекты обязательного медицинского страхования Статья 5. Субъекты обязательного медицинского страхования
- •Статья 6. Застрахованные лица
- •Статья 7. Страхователи
- •Статья 8. Страховщик
- •Статья 9. Территориальные фонды
- •Статья 10. Страховая медицинская организация
- •Статья 11. Медицинские организации в системе обязательного медицинского страхования
- •Глава 3. Права и обязанности застрахованных лиц, страхователей, страховых медицинских организаций и медицинских организаций Статья 12. Права и обязанности застрахованных лиц
- •Статья 13. Права и обязанности страхователей
- •Статья 14. Ответственность за нарушение требований о регистрации и снятии с регистрационного учета страхователей для неработающих граждан
- •Статья 15. Права и обязанности страховых медицинских организаций
- •Статья 16. Права, обязанности и ответственность медицинских организаций
- •Глава 4. Финансовое обеспечение обязательного медицинского страхования Статья 17. Средства обязательного медицинского страхования
- •Статья 18. Страховые взносы на обязательное медицинское страхование работающего населения
- •Статья 19. Размер страхового взноса на обязательное медицинское страхование неработающего населения
- •Статья 20. Период, порядок и сроки уплаты страховых взносов на обязательное медицинское страхование неработающего населения
- •Статья 21. Ответственность за нарушения в сфере уплаты страховых взносов на обязательное медицинское страхование неработающего населения
- •Статья 22. Состав бюджетов Федерального фонда и территориальных фондов и отчеты об их исполнении
- •Статья 23. Дотации для финансового обеспечения территориальных программ обязательного медицинского страхования в субъектах Российской Федерации
- •Статья 24. Формирование и расходование средств страховой медицинской организацией
- •Статья 25. Размещение временно свободных средств Федерального фонда, территориальных фондов и страховых медицинских организаций
- •Статья 26. Тарифы на оплату медицинской помощи при обязательном медицинском страховании
- •Статья 28. Компенсация расходов на оказание медицинской помощи в случае причинения вреда здоровью застрахованного лица вследствие тяжелого несчастного случая на производстве
- •Глава 5. Правовое положение Федерального фонда и территориальных органов Статья 29. Правовое положение, полномочия и органы управления Федерального фонда
- •Статья 30. Правовое положение, полномочия и органы управления территориальных фондов
- •Глава 6. Программы обязательного медицинского страхования Статья 31. Базовая программа обязательного медицинского страхования
- •Статья 32. Территориальная программа обязательного медицинского страхования
- •Глава 7. Договоры в системе обязательного медицинского страхования Статья 33. Система договоров в обязательном медицинском страховании
- •Статья 34. Договор о финансовом обеспечении обязательного медицинского страхования
- •Статья 35. Договор на оказание медицинской помощи по обязательному медицинскому страхованию
- •Статья 38. Обжалование заключений страховой медицинской организации по оценке контроля объемов, сроков и качества медицинской помощи в системе обязательного медицинского страхования
- •Статья 40. Сведения о застрахованном лице и оказанной ему медицинской помощи, содержащиеся в системе персонифицированного учета
- •Статья 41. Полис обязательного медицинского страхования
- •Статья 42. Порядок выдачи полиса обязательного медицинского страхования застрахованным лицам
- •Статья 43. Взаимодействие медицинской организации и страховой медицинской организации в системе персонифицированного учета сведений о медицинской помощи, оказанной застрахованному лицу
- •Статья 44. Взаимодействие страховой медицинской организации и территориального фонда в системе персонифицированного учета сведений о медицинской помощи, оказанной застрахованным лицам
- •Глава 10. Переходные и заключительные положения Статья 46. Программы модернизации здравоохранения Российской Федерации
- •Статья 47. Переходные положения
- •Статья 48. Нормативные правовые акты Российской Федерации, утрачивающие силу в связи с принятием настоящего Федерального закона
- •Статья 49. Вступление настоящего Федерального закона в силу
- •Типовые правила обязательного медицинского страхования граждан
- •Типовой договор территориального фонда обязательного медицинского страхования со страховой медицинской организацией
- •Концепция развития системы здравоохранения в Российской Федерации до 2020 г.
- •О санитарно-эпидемиологическом благополучии населения (с изменениями от 30 декабря 2001 г., 10 января, 30 июня 2003 г., 22 августа 2004 г., 9 мая, 31 декабря 2005 г.)
- •Глава I. Общие положения
- •Глава II. Права и обязанности граждан, индивидуальных предпринимателей и юридических лиц в области обеспечения санитарно-эпидемиологического благополучия населения
- •Глава III. Санитарно-эпидемиологические требования обеспечения безопасности среды обитания для здоровья человека
- •Глава IV. Санитарно-противоэпидемические (профилактические) мероприятия
- •Глава V. Государственное регулирование в области обеспечения санитарно-эпидемиологического благополучия населения
- •Глава VI. Государственный санитарно-эпидемиологический надзор в сфере обеспечения санитарно-эпидемиологического благополучия населения
- •Глава VII. Ответственность за нарушение санитарного законодательства
- •Глава VIII. Заключительные положения
- •Федеральный Закон о защите прав юридических лици индивидуальных предпринимателей при осуществлении государственного контроля (надзора)и муниципального контроля
- •Глава 1. Общие положения
- •Глава 2. Государственный контроль (надзор),
- •Глава 3. Права юридических лиц, индивидуальных предпринимателей при осуществлении государственного контроля (надзора), муниципального контроля и защита их прав
- •Глава 4. Заключительные положения
- •Положение о лицензировании медицинской деятельности (утверждено постановлением Правительства рф от 4 июля 2002г. № 499 )
- •Председатель Правительства Российской Федерации в. Путин
- •Российская федерация федеральный закон об обращении лекарственных средств
- •Глава 1. Общие положения
- •Глава 2. Полномочия федеральных органов исполнительной
- •Глава 3. Государственная фармакопея
- •Глава 4. Государственный контроль при обращении
- •Глава 5. Разработка, доклинические исследования
- •Глава 6. Осуществление государственной регистрации
- •Глава 7. Клинические исследования лекарственных
- •Глава 8. Производство и маркировка лекарственных средств
- •Глава 9. Ввоз лекарственных средств на территорию
- •Глава 10. Фармацевтическая деятельность
- •Глава 11. Уничтожение лекарственных средств
- •Глава 12. Государственное регулирование цен
- •Глава 13. Мониторинг безопасности лекарственных препаратов,
- •Глава 14. Информация о лекарственных препаратах
- •Глава 15. Ответственность за нарушение законодательства
- •Глава 16. Заключительные положения
- •Федеральное медико-биологическое агентство приказ от 30 марта 2007 года n 88 о добровольном информированном согласии на медицинское вмешательство
- •Федеральное медико-биологическое агентство информированное добровольное согласие на медицинское вмешательство
- •Федеральное медико-биологическое агентство Информированное добровольное согласие на оперативное вмешательство, в т.Ч. Переливание крови и ее компонентов
- •Отказ от проведения медицинского вмешательства
- •Инструкция по заполнению бланков добровольного информированного согласия
- •I. Общие положения
- •Венецианская декларация о терминальном состоянии
- •Декларация об эвтаназии
- •Декларация о трансплантации человеческих органов
- •Лиссабонская декларация о правах пациента
- •Мадридская декларация о профессиональной автономии и самоуправлении врачей
- •Хельсинкская декларация всемирной медицинской ассоциации Рекомендации для врачей, проводящих медико-биологические исследования с участием людей (1964 г.)
- •I. Общие положения
- •II. Порядок выбора (замены) страховой медицинской организации застрахованным лицом
- •III. Единые требования к полису обязательного медицинского страхования
- •IV. Порядок выдачи полиса обязательного медицинского страхования либо
- •V. Порядок ведения реестра
- •VI. Порядок ведения реестра медицинских организаций,
- •VII. Порядок направления территориальным фондом
- •VIII. Порядок оплаты медицинской помощи по обязательному медицинскому страхованию
- •IX. Порядок осуществления расчетов
- •X. Порядок утверждения для страховых медицинских организаций дифференцированных подушевых нормативов финансового обеспечения обязательного медицинского страхования
- •XII. Положение о Комиссии по разработке территориальной
- •XIV. Требования к размещению страховыми медицинскими организациями информации в сети «Интернет» и опубликованию
- •1. Сведения о застрахованном лице
- •2. Сведения о представителе застрахованного лица2
- •Сведения о застрахованном лице
- •2. Сведения о застрахованном лице до изменения или исправления анкетных данных4
- •3. Сведения о представителе застрахованного лица2
Концепция развития системы здравоохранения в Российской Федерации до 2020 г.
Эффективное функционирование системы здравоохранения определяется основными системообразующими факторами:
совершенствованием организационной системы, позволяющей обеспечить формирование здорового образа жизни и оказание качественной бесплатной медицинской помощи всем гражданам Российской Федерации (в рамках государственных гарантий);
развитием инфраструктуры и ресурсного обеспечения здравоохранения, включающего финансовое, материально-техническое и технологическое оснащение лечебно-профилактических учреждений на основе инновационных подходов и принципа стандартизации;
наличием достаточного количества подготовленных медицинских кадров, способных решать задачи, поставленные перед здравоохранением Российской Федерации.
По состоянию на 1 октября 2008 года численность постоянного населения Российской Федерации составила 141,9 млн. человек, что на 116,6 тысяч человек меньше, чем на соответствующую дату 2007 года.
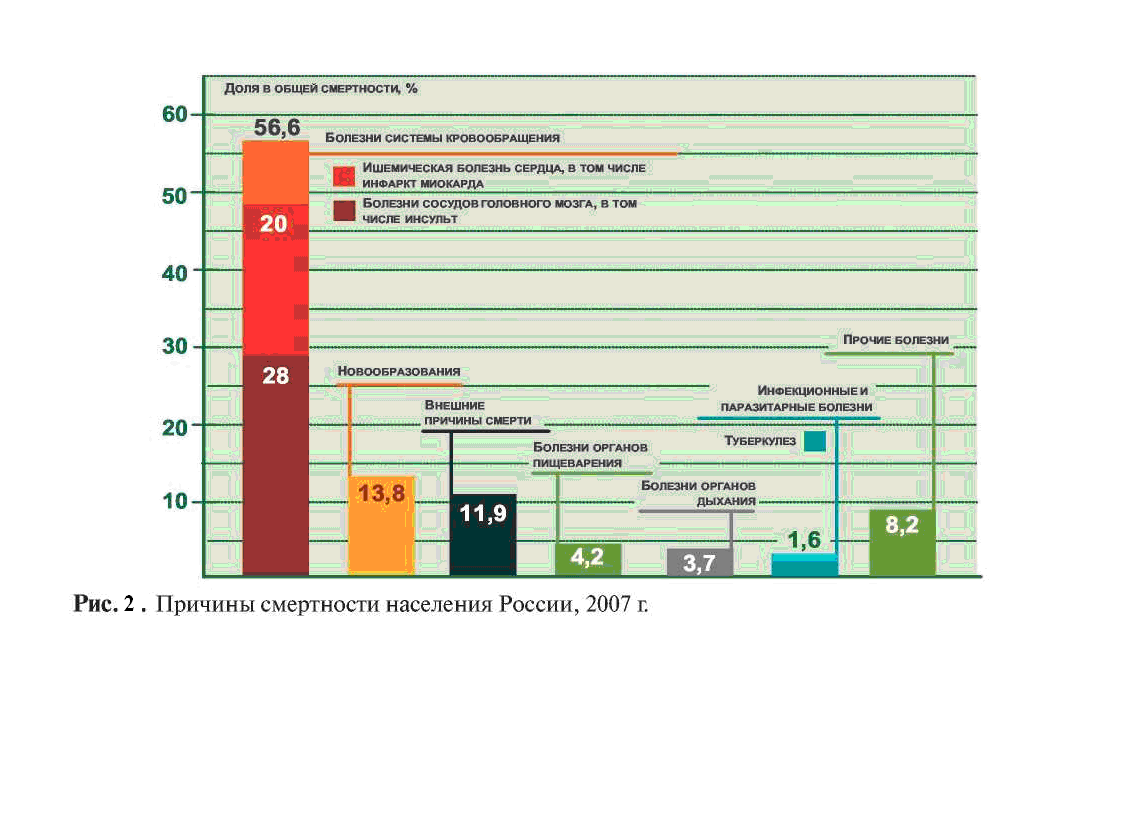
Законодательством Российской Федерации установлен страховой принцип финансирования медицинской помощи. В 1993 году в дополнение к бюджетной системе здравоохранения была создана система обязательного медицинского страхования (ОМС), в результате в России сложилась бюджетно-страховая модель финансирования государственной системы здравоохранения.
С 1998 года Правительством Российской Федерации ежегодно принимается Программа государственных гарантий оказания гражданам Российской Федерации бесплатной медицинской помощи, обеспечиваемая за счет средств бюджетной системы Российской Федерации.
Начиная с 2005 года, Правительством Российской Федерации ежегодно утверждаются нормативы финансового обеспечения медицинской помощи на одного жителя (подушевые финансовые нормативы).
Расходы на оказание бесплатной медицинской помощи из государственных источников финансирования в 2007 году составили 897,3 млрд. руб. и возросли в текущих ценах в 3,8 раза по сравнению с 2001 годом. Программа обеспечивалась в отчетном году за счет федерального бюджета, бюджетов субъектов Российской Федерации и местных бюджетов (63,4 %) и средств системы ОМС (36,6 %).
Необходимо отметить постоянное снижение доли ОМС в финансовом обеспечении программы государственных гарантий, при этом страхование неработающего населения осуществлялось в отсутствии единых принципов формирования страховых платежей, а остальные источники формирования системы ОМС носили налоговый, а не страховой характер. Это произошло за счет увеличения бюджетного финансирования в рамках приоритетного национального проекта в сфере здравоохранения.
В 2007 году стоимость базовой программы обязательного медицинского страхования составляла 328,2 млрд. рублей. Эти расходы включали статьи на заработную плату с начислениями, медикаменты, мягкий инвентарь, продукты питания, расходные материалы. Субъектами Российской Федерации и муниципальными образованиями напрямую осуществлялось финансовое обеспечение деятельности бюджетных учреждений в размере 361,9 млрд. рублей. При этом из указанных 361,9 млрд. рублей, 187,2 млрд. рублей – ассигнования, подлежащие передаче через систему ОМС, поскольку осуществляются по тем же статьям, которые входят в тарифы ОМС. Кроме того, 111,8 млрд. рублей были направлены субъектами Российской Федерации и муниципальными образованиями на оплату коммунальных и прочих услуг, содержание имущества, приобретение основных средств.
Анализ финансовых показателей реализации территориальных программ государственных гарантий в 2007 году позволил установить их дефицит в 60 субъектах Российской Федерации, который составил 65,4 млрд. рублей.
Средства системы ОМС доводятся до лечебных учреждений через частные страховые организации (СМО), которые никак не заинтересованы в повышении качества медицинской помощи застрахованным и снижении издержек на ее оказание.
Дополнительным каналом поступления средств в лечебно-профилактические учреждения (ЛПУ) являются платные медицинские услуги и программы ДМС. Наличие этих источников, с одной стороны, позволяет ЛПУ (в условиях недофинансирования) получить дополнительные средства для зарплаты сотрудников и текущего содержания ЛПУ, но, с другой стороны (в отсутствии жесткой регламентации этих услуг), приводит к снижению доступности и качества медицинской помощи населению, обслуживаемому по программе государственных гарантий.
Основными проблемами реализации государственных гарантий оказания гражданам Российской Федерации бесплатной медицинской помощи в Российской Федерации являются:
недостаточное финансовое обеспечение прав граждан Российской Федерации на бесплатную медицинскую помощь, сильная дифференциация среди субъектов Российской Федерации в части реализации территориальных программ государственных гарантий бесплатной медицинской помощи;
раздробленность источников финансирования медицинской помощи, не позволяющая внедрить в полном объеме систему обязательного медицинского страхования.
Система организации медицинской помощи населению
С первой половины ХХ века по настоящее время в России реализуется двухуровневый принцип построения системы медицинской помощи населению, представленный самодостаточными и мало интегрированными между собой структурами: амбулаторно-поликлинической, скорой и стационарной.
В настоящее время медицинская помощь населению Российской Федерации оказывается в 9 620 учреждениях здравоохранения, в том числе в 5 285 больницах, 1 152 диспансерах, 2 350 самостоятельных амбулаторно-поликлинических учреждениях, 833 самостоятельных стоматологических поликлиниках.
Первичная медико-санитарная помощь — совокупность медико-социальных и санитарно-гигиенических мероприятий, обеспечивающих оздоровление, профилактику неинфекционных и инфекционных заболеваний, лечение и реабилитацию населения. Первичная медико-санитарная помощь представляет первый этап непрерывного процесса охраны здоровья населения, что диктует необходимость ее максимального приближения к месту жительства и работы людей. Основным принципом ее организации является территориально-участковый.
Несовершенства в работе амбулаторно-поликлинического звена здравоохранения, в частности, отсутствие системы патронажа и неэффективное наблюдение за больными с хронической патологией привели к тому, что скорая медицинская помощь является самым распространенным видом оказания внегоспитальной медицинской помощи населению страны, взяв на себя часть функций амбулаторно-поликлинического звена.
В настоящее время в Российской Федерации скорую медицинскую помощь (далее – СМП) обеспечивают 3 268 станций и отделений, укомплектованные общепрофильными (12 603, 31,4% от общего количества бригад), специализированными (2 987; 7,5%), фельдшерскими (22 765; 56,8%) бригадами и бригадами интенсивной терапии (1 741; 4,3%). В течение 2007 года выполнено свыше 48822 тыс. выездов к больным, при этом госпитализировано только 9199 тыс. человек, то есть только каждый 5–6-й вызов заканчивался госпитализацией в стационар.
Таким образом, низкая эффективность профилактической работы первичного звена медицинской помощи, отсутствие системы амбулаторного долечивания и патронажа, а также несовершенство организации работы скорой медицинской помощи привели к тому, что стационарная помощь выступает в качестве основного уровня в системе охраны здоровья населения. При этом, по сути, стационарная медицинская помощь необходима лишь при заболеваниях, требующих комплексного подхода к диагностике и лечению, применения сложных методов обследования и лечения с использованием современной медицинской техники, оперативных вмешательств, постоянного круглосуточного врачебного наблюдения и интенсивного ухода.
По данным работы стационаров муниципального, субъектового и федерального подчинения, среднегодовая занятость койки в 2007 году составила 318 дней, средняя длительность пребывания больного в стационаре 13,2 дня.
В системе здравоохранения в 2007 г. работало 616,4 тыс. врачей и 1 349,3 тыс. среднего медицинского персонала (в 2004 – 607,1 тыс. и 1 367,6 тыс.; в 2006 г. – 607,7 тыс. и 1 351,2 тыс. соответственно). Обеспеченность врачами на 10 тыс. населения составила 43,3 (2004 – 42,4; 2006 г. – 43,0), средним медицинским персоналом – 94,9 (2004 г. – 95,6; 2006 г. – 95,0). Соотношение врачей и среднего медицинского персонала составляет 1: 2,2.
Несмотря на то, что врачей в Российской Федерации больше на душу населения, чем, в среднем, в развитых странах, качество медицинской помощи и показатели здоровья населения в нашей стране значительно хуже, что свидетельствует о низкой эффективности отечественной системы медицинской помощи, недостаточной квалификации врачей и слабой мотивации их к профессиональному совершенствованию.
Лекарственное обеспечение граждан в амбулаторных условиях
В настоящее время в Российской Федерации существует три модели обеспечения граждан лекарственными средствами: дополнительное лекарственное обеспечение льготных категорий граждан в рамках набора социальных услуг, предусмотренного Федеральным законом от 17.07.1999 г. № 178-ФЗ «О государственной социальной помощи» и лекарственное обеспечение отдельных групп населения бесплатно или со скидкой по рецептам врача в соответствии с постановлением Правительства Российской Федерации от 30.07.1994 г. № 890, а также обеспечение дорогостоящими лекарственными средствами больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, миелолейкозом, рассеянным склерозом, а также после трансплантации органов и тканей.
Система дополнительного лекарственного обеспечения в рамках набора социальных услуг функционирует с 2005 года. В рамках указанной системы осуществляются закупки лекарственных средств по процедурам закупок товаров, работ и услуг для государственных (муниципальных) нужд.
С 2005 по 2007 год закупки осуществлялись Федеральным фондом обязательного медицинского страхования за счет средств, передаваемых из федерального бюджета, в 2008 году – органами государственной власти субъектов Российской Федерации за счет субвенций, передаваемых в территориальные фонды обязательного медицинского страхования, а в 2009 году будут переданы субвенциями из федерального бюджета в бюджеты субъектов Российской Федерации
В 2005 году на дополнительное лекарственное обеспечение было запланировано 50,8 млрд. рублей, фактические расходы составили 48,3 млрд. рублей. При этом, ограниченное использование финансовых средств было вызвано во первых сохранением солидарного принципа, а во вторых адаптацией врачей и пациентов к новой системе лекарственного обеспечения.
В 2006 году произошел законодательный отказ существенной части льготников от получения набора социальных услуг, и в системе дополнительного лекарственного обеспечения остались только граждане, нуждающиеся в регулярном приеме лекарственных средств. Кроме того, был существенно расширен список лекарственных средств. Фактические расходы составили 74,7 млрд. рублей при запланированных 34 млрд. рублей.
Кроме того, в 2005 и 2006 годах не было единой автоматизированной системы учета назначения и выписки лекарственных средств, что явилось причиной низкого уровня контроля.
В 2007 году численность граждан, оставивших право на дополнительное лекарственное обеспечение практически не изменилась, запланированы были средства в сумме 34,9 млрд. рублей, но расходы сократились на 30 процентов и составили 50,7 млрд. рублей. Снижение расходов обусловлено установлениями ограничений на выписку препаратов, а также появлением централизованной автоматизированной системы.
В 2008 году планируемые расходы на реализацию прав граждан льготных категорий на дополнительное лекарственное обеспечение составили 30,1 млрд. рублей. При этом, из системы дополнительного лекарственного обеспечения были выведены дорогостоящие препараты для лечения больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, миелолейкозом, рассеянным склерозом, а также после трансплантации органов и тканей. На закупку этих препаратов были выделены средства в сумме 33 млрд. рублей.
Кроме того, на осуществление отдельных полномочий в области лекарственного обеспечения в 2008 году субъектам Российской Федерации было дополнительно выделено 10 млрд. рублей.
В целом, существующая система льготного обеспечения граждан лекарственными средствами в амбулаторных условиях подлежит изменению по следующим причинам:
система не позволяет эффективно планировать и контролировать уровень затрат – подушевой норматив ДЛО не основан на анализе потребностей, а сформирован исходя из установленной ежемесячной денежной выплаты;
модель ДЛО с использованием процедур закупок для государственных нужд не гарантирует бесперебойное обслуживание льготных рецептов надлежащего ассортимента;
основным сдерживающим механизмом является ограничительный перечень, однако его формирование не основано на анализе клинической и экономической эффективности;
отсутствуют участники, экономически мотивированные в эффективном расходовании бюджетных средств.
Гарантированное обеспечение населения Российской Федерации качественной медицинской помощью
Качественная медицинская помощь основана на применении современных технологий организации и оказания диагностических, лечебных, реабилитационных и профилактических услуг, эффективность и безопасность которых (при конкретных заболеваниях или патологических состояниях) подтверждена в соответствии с принципами доказательной медицины.
Гарантированное обеспечение каждого гражданина Российской Федерации качественной медицинской помощью должно обеспечиваться следующими мероприятиями:
конкретизация государственных гарантий оказания бесплатной медицинской помощи;
стандартизация медицинской помощи;
организация медицинской помощи;
обеспечение лекарственными средствами граждан в амбулаторных условиях;
осуществление единой кадровой политики;
инновационное развитие здравоохранения;
модернизация системы финансового обеспечения оказания медицинской помощи;
информатизация здравоохранения.
Конкретизация государственных гарантий оказания бесплатной медицинской помощи
Государственные гарантии оказания гражданам Российской Федерации бесплатной медицинской помощи должны быть законодательно определены, включая:
источники финансового обеспечения государственных гарантий оказания гражданам Российской Федерации бесплатной медицинской помощи;
объем государственных гарантий оказания гражданам Российской Федерации бесплатной медицинской помощи в части видов, порядка и условий оказания медицинской помощи;
порядок оценки эффективности исполнения государственных гарантий бесплатной медицинской помощи;
ответственность за неисполнение показателей государственных гарантий бесплатной медицинской помощи;
порядок разработки нормативных актов, конкретизирующих установленный законодательством Российской Федерации объем государственных гарантий бесплатной медицинской помощи.
В соответствии с положениями законодательства Российской Федерации Правительство Российской Федерации должно принимать Программу государственных гарантий на три года, содержащую:
минимальный размер подушевого норматива финансового обеспечения государственных гарантий оказания бесплатной медицинской помощи;
нормативы финансовых затрат на единицу объема медицинской помощи;
подушевые нормативы объемов медицинской помощи по видам;
минимальные значения критериев оценки качества и доступности медицинской помощи.
На основании утвержденной Правительством Российской Федерации ПГГ, субъекты Российской Федерации принимают территориальные программы государственных гарантий, в зависимости от финансовой обеспеченности, устанавливая собственные финансовые нормативы (не ниже установленных Правительством Российской Федерации), а также включая при необходимости дополнительные виды медицинской помощи.
Одним из основных факторов создания системы качественной и доступной медицинской помощи является наличие единых для всей территории Российской Федерации порядков и стандартов оказания медицинской помощи при наиболее распространенных и социально-значимых заболеваниях и патологических состояниях.
Стандарты медицинской помощи разрабатываются в соответствии с показателями Программы государственных гарантий, и их выполнение гарантируется гражданам на всей территории Российской Федерации.
Создание стандартов медицинской помощи позволит рассчитать реальную стоимость медицинских услуг в каждом субъекте Российской Федерации, определить затраты на реализацию государственных и территориальных программ медицинской помощи населению, рассчитать необходимое лекарственное обеспечение этих программ (список жизненно необходимых и важнейших лекарственных средств), обосновать подушевые нормативы финансирования и оптимизировать варианты проведения реструктуризации сети учреждений здравоохранения.
Организация медицинской помощи
В целях обеспечения качества и доступности медицинской помощи необходимо создание организационной системы, предусматривающей:максимально быструю доставку пациента в лечебно-профилактическое учреждение, оснащенное лечебно-диагностическим оборудованием, укомплектованное подготовленными медицинскими кадрами и обеспеченное необходимыми лекарственными препаратами и изделиями медицинского назначения согласно соответствующим стандартам;
при необходимости, поэтапное продолжение лечения в других медицинских учреждениях (преемственные долечивание и реабилитация, вторичная профилактика, санаторно-курортное восстановительное лечение) или на дому, в соответствии с порядком оказания медицинской помощи при конкретном заболевании или состоянии, до достижения наилучшего результата (выздоровление, функциональное восстановление).
Для создания системы оказания медицинской помощи, удовлетворяющей указанным критериям необходимо:
создание правовых и экономических условий для формирования саморегулируемой системы оказания медицинской помощи населению, обеспечивающей мотивированную эффективную работу медицинских служб каждого уровня, преемственность их действий на всех этапах лечения для достижения наилучшего результата;
развитие первичной медико-санитарной помощи, в том числе уменьшение количество прикрепленного взрослого населения до 1,2 – 1,5 тыс. человек, детского – до 600–800 детей и подростков на 1 участок с уменьшением нагрузки на одного участкового врача, придание приоритета профилактической работе, усиление патронажной и реабилитационной функции, внедрение системы «стационаров на дому», обеспечиваемых мобильными специально оснащенными патронажными бригадами, дооснащение учреждений, совершенствование и расширение стационар-замещающих медицинских технологий;
совершенствование работы скорой медицинской помощи, в том числе оптимизация маршрутов доставки больных в стационар в зависимости от вида патологии, тяжести состояния больного, внедрение целевых показателей работы скорой медицинской помощи (время приезда на вызов, время транспортировки в стационар, догоспитальная летальность), внедрение порядков оказания медицинской помощи в части догоспитального ведения больных с разными видами патологии;
оптимизацию работы учреждений стационарного уровня в части установления целевых показателей работы учреждений, отражающих не только виды и объемы оказанной медицинской помощи, но и ее качество, внедрения этапности медицинской помощи и разработанных маршрутов транспортировки больных на основе рационального распределения функциональных обязанностей стационаров (муниципальные (городские и районные) – для оказания первичной помощи при неотложных состояниях; субъектовые межрайонные – для оказания специализированной помощи, в том числе при неотложных состояниях и состояниях, требующих восстановительного лечения и реабилитации; субъектовые и федеральные – для оказания специализированной, в том числе высокотехнологичной, помощи), развития специализированных учреждений для оказания диагностической и лечебной помощи больным с онкологическими заболеваниями, создания в каждом стационаре службы маршрутизации, ответственной за организацию долечивания и реабилитации выписывающихся больных, а также расширения объемов и внедрение и новых видов высокотехнологичной помощи, в том числе при неотложных состояниях;
развитие патронажно-реабилитационной медицинской помощи, включающее создание сети учреждений (отделений) восстановительного лечения (долечивания), реабилитации, медицинского ухода, в том числе за счет перепрофилизации работающих стационаров и санаторно-курортных учреждений, расширения сети дневных стационаров, создание системы целевых показателей работы учреждений патронажно-реабилитационного уровня, отражающих качество медицинской помощи (степень восстановления нарушенных функций, показатели первичной инвалидности и утяжеления инвалидности), внедрение высокотехнологичных реабилитационных технологий;
разработку и внедрение системы управления качеством медицинской помощи на основе порядков и стандартов ее оказания, в том числе осуществление аудита медицинской помощи на основе аудита лечебного процесса в соответствии с индикаторами качества и технологических отклонений;
унификацию оснащения медицинских организаций оборудованием в соответствии со стандартами и порядками оказания медицинской помощи;
расширение хозяйственной самостоятельности учреждений здравоохранения, а также повышение их ответственности за экономические результаты своей деятельности в том числе с изменением организационно-правовых форм на основе единой системы критериев.
Создание системы «внегоспитальной лечебной помощи, патронажа и реабилитации» будет происходить путем ее организационного выделения из первичной медико-санитарной и специализированной медицинской помощи.
Законодательное и нормативно – правовое обеспечение реализации Концепции
Правовое обеспечение Концепции предусматривает как издание новых законодательных актов, так и совершенствование действующего законодательства, которое должно осуществляться поэтапно.
Первоначальный этап правового обеспечения заключается в принятии законодательных актов, направленных на реализацию задач по конкретизации государственных гарантий оказания гражданам бесплатной медицинской помощи, созданию эффективной модели управления финансовыми ресурсами программы государственных гарантий, перехода на современную систему организации медицинской помощи, по улучшению лекарственного обеспечения.
В целях реализации указанных задач потребуется уточнение федерального законодательства, закрепляющего систему организации здравоохранения и оказания медицинской помощи в Российской Федерации, права пациентов и медицинских работников, а также гарантированный механизм реализации этих прав, устанавливающего требования к организациям здравоохранения, к квалификации медицинских работников, оснащению организаций здравоохранения.
Потребуется разработка и принятие федерального закона «О государственных гарантиях оказания гражданам бесплатной медицинской помощи», включающего порядок, условия и стандарт объема предоставления гражданам бесплатной медицинской помощи, порядок финансового обеспечения предоставляемой медицинской помощи с учетом потребности граждан Российской Федерации в медицинской помощи, а также с учетом принимаемых стандартов медицинской помощи. Указанный федеральный закон также должен содержать порядок разработки и принятия медико-экономических стандартов, критерии качества предоставляемых медицинских услуг, порядок контроля и порядок проведения медико-экономической экспертизы качества оказанной медицинской помощи.
Необходимо отметить, что действующее в настоящее время законодательство Российской Федерации не обеспечивает в полной мере четкого разграничения между порядком получения гражданами бесплатной медицинской помощи и платных медицинских услуг, не содержит в себе положений, регулирующих вопросы ценообразования на медицинские услуги, предоставляемые гражданам за плату.
В связи с этим, помимо конкретизации условий и порядка оказания бесплатной медицинской помощи, потребуется совершенствование законодательства по установлению механизма правового регулирования оказания платным медицинских услуг.
Реализация программы государственных гарантий бесплатной медицинской помощи должна осуществляться через систему обязательного медицинского страхования. Потребуется разработка и принятие федерального закона «Об обязательном медицинском страховании», который должен будет определить правовые, экономические и организационные основы ОМС, включающие права и обязанности субъектов обязательного медицинского страхования, установить централизованную систему центральных и территориальных органов фондов, порядок формирования источников финансирования медицинского страхования как для работающего, так и неработающего населения, включающего порядок уплаты страховых взносов на обязательное медицинское страхование и установления страховых тарифов на ОМС, порядок ведения персонифицированного учета застрахованных граждан и оказанной им медицинской помощи, введение системного контроля за осуществлением ОМС.
В целях создания финансовой основы новой модели медицинского страхования потребуется внести изменения в Налоговый кодекс Российской Федерации в части отмены единого социального налога, зачисляемого в Федеральный фонд ОМС и территориальные фонды ОМС, а также направления части налога на доходы физических лиц в бюджеты территориальных фондов обязательного медицинского страхования.
В целях развития здравоохранения потребуется принятие решения о включении лекарственного обеспечения граждан в программу государственных гарантий оказания бесплатной медицинской помощи и в медико-экономические стандарты в качестве их составной части, и, как следствие, включение лекарственного обеспечения в медицинское страхование, что потребует соответствующего отражения в перечисленных федеральных законах.
После принятия основополагающих законодательных актов потребуется принятие необходимых подзаконных нормативных правовых актов Президента Российской Федерации, Правительства Российской Федерации и федеральных органов исполнительной власти, в первую очередь, Минздравсоцразвития России.
Кроме того, в настоящее время наблюдается рост количества гражданских исков, связанных с качеством оказания медицинской помощи. В связи с этим, на втором этапе правового обеспечения реализации постановленных задач по развитию здравоохранения, в целях создания правовых и финансовых основ для урегулирования вопросов, связанных с качеством оказания медицинской помощи, должны быть приняты федеральные законы «О защите прав пациента» и «Об обязательном страховании профессиональной ответственности медицинских работников».
В целях развития рынка медицинских услуг, предоставляемых организациями здравоохранения, а также в целях расширения финансовой самостоятельности указанных организаций здравоохранения следует внести изменения в Федеральный закон от 3 ноября 2006 г. № 174-ФЗ «Об автономных учреждениях» в части отмены ограничения по запрету создания автономного учреждения здравоохранения путем изменения типа существующего учреждения здравоохранения. Кроме того, потребуется пересмотр законодательства об автономных учреждениях с целью установления более гибких механизмов управления автономными учреждениями, а также в части определения состава затрат на оказание государственной услуги, чтобы не допустить перекрестного субсидирования расходов на содержание имущества автономных учреждений при внедрении полного тарифа на медицинскую помощь в системе обязательного медицинского страхования.
На данном этапе правового обеспечения Концепции потребуется также совершенствование законодательства, регулирующего вопросы донорства крови и ее компонентов, трансплантации органов и тканей.
Учитывая, что в настоящее время судебная практика Европейского суда указывает на не совершенство российского законодательства о психиатрической помощи в части нарушения прав пациента, требуется внести изменения в Закон Российской Федерации «О психиатрической помощи и гарантиях прав граждан при ее оказании».
Следующим этапом нормативного правового регулирования, обеспечивающего выполнение задач по развитию здравоохранения, должно являться совершенствование действующего санитарно-эпидемиологического законодательства. При этом нормативно-правовое регулирование в указанной сфере должно быть направлено на формирование здорового образа жизни населения, предупреждение инфекционных и социально-значимых заболеваний, ужесточение ответственности за несоблюдение санитарно-эпидемиологического законодательства.
Федеральный закон от 24 июля 2009 г. N 213-ФЗ "О внесении изменений в отдельные законодательные акты Российской Федерации и признании утратившими силу отдельных законодательных актов (положений законодательных актов) Российской Федерации в связи с принятием Федерального закона "О страховых взносах в Пенсионный фонд Российской Федерации, Фонд социального страхования Российской Федерации, Федеральный фонд обязательного медицинского страхования и территориальные фонды обязательного медицинского страхования"
В связи с принятием Федерального закона N 212-ФЗ, устанавливающего порядок исчисления и уплаты страховых взносов в ПФР (на обязательное пенсионное страхование), ФСС РФ (на обязательное социальное страхование на случай временной нетрудоспособности и в связи с материнством), ФФОМС и ТФОМС (на обязательное медицинское страхование), вносятся изменения в законодательные акты РФ.
С 1 января 2010 г. утрачивают силу положения Налогового кодекса о едином социальном налоге, порядке его исчисления и уплаты. ЕСН заменяется страховыми взносами на конкретные виды социального страхования.
Федеральный закон N 213-ФЗ направлен на дальнейшее развитие системы обязательного социального страхования и повышение с 2010 г. уровня пенсионного обеспечения граждан.
В частности, предусмотрен новый механизм начисления различных социальных выплат и пенсий.
Вместо базовой части трудовой пенсии (1 950 руб. в месяц) вводится фиксированный базовый размер страховой части трудовой пенсии. Так, для граждан, не имеющих на иждивении нетрудоспособных членов семьи, он составит 2 562 руб. в месяц, а для граждан, достигших возраста 80 лет или являющихся инвалидами I группы, - 5 124 руб. в месяц.
В результате пересчета размера пенсионных прав, полученных до 2002 г. (начало пенсионной реформы), среднегодовая прибавка к пенсии в 2010 г. составит 2 340 руб. В итоге среднегодовой размер трудовой пенсии составит 7 946 руб., в том числе трудовой пенсии по старости - 8 602 руб.; трудовой пенсии по инвалидности (для новых назначений) - 6 974 руб.; трудовой пенсии по случаю потери кормильца (для новых назначений) - 7 123 руб.; трудовой пенсии для лиц, проживающих в районах Крайнего Севера и приравненных к ним местностях, - 10 570 руб. Размер социальной пенсии достигнет 4 917 руб. Для сравнения, средний размер пенсии на 1 марта 2009 г. составлял 4 845 руб.
Следует отметить, что в любом случае доход пенсионера не будет ниже прожиточного минимума в регионе его проживания. Пенсия тех, кто вступил в систему пенсионного страхования после 2002 г. и проработает более 30 лет, составит 40% от заработка.
Начиная с 1 января 2010 г., при расчёте размера трудовых пенсий величина расчётного пенсионного капитала будет увеличиваться на 10% и сверх того на 1% за каждый полный год общего трудового стажа, приобретённого до 1 января 1991 г.
При наличии у пенсионеров продолжительного трудового стажа (более 30 лет у мужчин и 25 лет у женщин) за каждый год сверх этого стажа фиксированный базовый размер страховой части трудовой пенсии будет увеличен на 6%.
Увеличен максимальный размер пособия по временной нетрудоспособности. Теперь он составит при страховом стаже до 5 лет 20 750 руб., при страховом стаже от 5 до 8 лет - 27 666 руб.; при страховом стаже 8 и более лет - 34 583 руб. (ранее максимальный размер этого пособия независимо от стажа равнялся 18 720 руб.). Максимальный размер пособия по беременности и родам за полный календарный месяц составит 34 583 руб. (прежде - 25 390 руб.).
Федеральный закон вступает в силу с 1 января 2010 г., за исключением положений, для которых предусмотрены иные сроки вступления в силу.
Национальный стандарт РФ ГОСТ-Р 52379-2005 «Надлежащая клиническая практика» (ICH E6 GCP), утвержденным приказом Федерального агентства по техническому регулированию и метрологии от 27.09.2005 № 232-ст (Извлечения)
1. Термины и определения
…1.12 информированное согласие (informed consent): Процедура добро-вольного подтверждения субъектом своего согласия на участие в конкретном исследовании после получения информации обо всех значимых для принятия им решения аспектах исследования. Информированное согласие документируется посредством подписания и датирования формы информированного согласия…
1.29 Независимый этический комитет; НЭК (independent ethics committee; IEC): Независимый орган (экспертный совет или комитет, действую-щий на уровне организации, региональном, национальном или международном уровне), состоящий из медицинских работников, а также лиц, не имеющих отношения к медицине, который обеспечивает защиту прав, безопасности и благополучия субъектов исследования и выступает для общества гарантом такой защиты, в частности путем рассмотрения, утверждения/одобрения протокола исследования, кандидатур исследователей, исследовательских центров, а также материалов и методов, которые предполагается использовать для получения и документирования информированного согласия субъектов исследования.
Правовой статус, состав, функции, деятельность независимых этических комитетов, а также относящиеся к ним нормативные требования могут различаться в разных странах, тем не менее, НЭК должны функционировать в соответствии с GСР…
3. ЭКСПЕРТНЫИ СОВЕТ ОРГАНИЗАЦИИ/НЕЗАВИСИМЫЙ ЭТИЧЕСКИЙ КОМИТЕТ (ЭСО/НЭК)
3.1 Обязанности 3.1.1 Экспертный совет организации/Независимый этический комитет при-зван защищать права, безопасность и благополучие всех субъектов исследования. Исследованиям с участием уязвимых субъектов должно быть уделено особое внимание. 3.1.2 ЭСО/НЭК должен получить следующие документы: - протокол исследования/поправки; - письменную форму информированного согласия и ее последующие редак-ции, предлагаемые исследователем для использования в исследовании; - описание действий, направленных на привлечение субъектов к участию в исследовании (например, рекламные объявления); - письменные материалы, которые будут предоставлены субъектам; - брошюру исследователя; - известную информацию, касающуюся безопасности; - информацию о выплатах и компенсациях субъектам исследования; - текущую версию научной биографии исследователя (curriculum vitae) и/или другие материалы, подтверждающие его квалификацию; - любые другие документы, которые могут потребоваться ЭСО/НЭК для выполнения его обязанностей. ЭСО/НЭК должен рассмотреть вопрос о проведении предлагаемого клинического исследования в разумные сроки и документально оформить свое мнение, четко идентифицируя исследование, рассмотренные документы и даты при вынесении следующих решений: - утверждения/одобрения; - требования о внесении изменений, необходимых для получения утверждения/одобрения; - отрицательного заключения/неодобрения; - отмены/приостановления данных ранее утверждения/одобрения. 3.1.3 ЭСО/НЭК должен оценить соответствие квалификации исследователя предлагаемому исследованию на основании его научной биографии (curriculum vitae) и/или другой соответствующей документации, запрошенной ЭСО/НЭК. 3.1.4 ЭСО/НЭК должен рассматривать каждое текущее исследование с периодичностью, адекватной риску для субъектов исследования, но не реже одного раза в год. 3.1.5 ЭСО/НЭК может потребовать, чтобы субъектам исследования помимо информации, указанной в 4.8.10, были предоставлены дополнительные сведения об исследовании, если, по мнению ЭСО/НЭК, эта информация позволит существенно повысить степень защиты прав, безопасности и/или благополучия субъектов. 3.1.6 Если согласие на участие субъекта в исследовании, не связанном с лечением, дает его законный представитель (см. 4.8.12 и 4.8.14), ЭСО/НЭК должен убедиться, что предоставленный протокол и/или другая документация соответствуют этическим нормам и нормативным требованиям для таких исследований. 3.1.7 Если протокол предусматривает невозможность получения согласия на участие в исследовании у субъекта или его законного представителя (см. 4.8.15) до момента включения субъекта в исследование, ЭСО/НЭК должен убедиться, что предоставленный протокол и/или другая документация соответствуют этическим нормам и нормативным требованиям для таких исследований (например, при не-отложных состояниях). 3.1.8 ЭСО/НЭК рассматривает размер и порядок выплат субъекту исследования, чтобы убедиться в отсутствии необоснованной заинтересованности или принуждения субъектов исследования. Размер выплат субъектам должен быть заранее определен и не должен целиком зависеть от того, завершил субъект исследование полностью или нет. 3.1.9 ЭСО/НЭК должен убедиться в том, что информация, касающаяся выплат субъектам исследования, включая методы, суммы и график выплат, отражена в письменной форме информированного согласия и любой другой письменной информации, предоставляемой субъектам. Должно быть указано, каким образом будет определен размер выплат.
3.2 Состав, функции и порядок работы 3.2.1 ЭСО/НЭК должен иметь в своем составе достаточное число лиц, суммарно обладающих необходимым опытом и квалификацией для оценки научных, медицинских и этических аспектов предлагаемого исследования. Рекомендуется, чтобы в ЭСО/НЭК входили: а) не менее пяти членов; б) как минимум один член, чьи интересы лежат вне сферы науки; в) как минимум один член, который не зависит от организации/исследовательского центра. Голосовать/выражать мнение по исследованию имеют право только те члены ЭСО/НЭК, которые не зависят от исследователя и спонсора данного исследования. ЭСО/НЭК должен вести список своих членов с указанием их квалификации. 3.2.2 ЭСО/НЭК должен осуществлять деятельность в соответствии с письменными процедурами, документировать свою работу, вести протоколы заседаний, а также соблюдать GCP и нормативные требования. 3.2.3 ЭСО/НЭК принимает решения на объявленных заседаниях при наличии кворума, установленного его письменными процедурами. 3.2.4 Право голосовать/высказывать свое мнение и/или рекомендации имеют только те члены ЭСО/НЭК, которые участвуют в рассмотрении документации и обсуждении. 3.2.5 Исследователь может предоставлять информацию по любым аспектам исследования, но не может участвовать в прениях или в голосовании/выработке мнения ЭСО/НЭК. 3.2.6 ЭСО/НЭК может обращаться за помощью к экспертам, не являющимся его членами.
3.3 Процедуры ЭСО/НЭК должен разработать, документально оформить и соблюдать свои процедуры, определяющие: 3.3.1 Его состав (фамилии и квалификацию членов) и учредивший его орган. 3.3.2 Порядок назначения заседаний, оповещения его членов о предстоящих заседаниях, а также организацию заседаний. 3.3.3 Порядок первичного и последующего рассмотрения документации по исследованию. 3.3.4 Периодичность последующего рассмотрения документации по исследованию. 3.3.5 Порядок, согласно нормативным требованиям, ускоренного рассмотрения и утверждения/одобрения незначительных изменений для исследований, ранее утвержденных/одобренных им же. 3.3.6 Недопустимость включения субъектов в исследование до того, как ЭСО/НЭК выдаст письменное утверждение/одобрение на проведение исследования. 3.3.7 Недопустимость отклонений от протокола или его изменений без предварительного утверждения/одобрения соответствующих поправок ЭСО/НЭК, кроме тех случаев, когда необходимо устранить непосредственную угрозу субъектам исследования или когда изменения касаются только административных или технических аспектов исследования (например, замена монитора, изменение номера телефона) (см. 4.5.2). 3.3.8 Обязанность исследователя незамедлительно сообщать ЭСО/НЭК: а) об отклонениях от протокола или изменениях протокола, произведенных для устранения непосредственной угрозы субъектам исследования (см. 3.3.7, 4.5.2, 4.5.4); б) об изменениях, увеличивающих риск для субъектов и/или существенно влияющих на проведение исследования (см. 4.10.2); в) обо всех нежелательных реакциях, которые являются одновременно серьезными и непредвиденными; г) о новых данных, которые могут свидетельствовать о возрастании риска для субъектов или неблагоприятно повлиять на ход исследования. 3.3.9 Обязанность ЭСО/НЭК незамедлительно в письменном виде сообщать исследователю/организации: а) о своих решениях/заключениях, касающихся исследования; б) о причинах принятия решений/заключений; в) о порядке обжалования его решений/заключений.
3.4 Документация ЭСО/НЭК должен хранить все документы (например, свои процедуры, списки членов с указанием рода деятельности и места работы, представленные на рас-смотрение документы, протоколы заседаний и переписку) в течение минимум трех лет после завершения исследования и предоставлять их по запросу уполномочен-ных органов. Исследователи, спонсор, уполномоченные органы могут запрашивать у ЭСО/НЭК его процедуры и списки членов…
4.4 Контакты с ЭСО/НЭК 4.4.1 Перед тем как начать исследование, исследователь/организация должны получить письменное и датированное утверждение/одобрение ЭСО/НЭК протокола исследования, письменной формы информированного согласия и ее последующих редакций, мер, направленных на привлечение субъектов к участию в исследовании (например, рекламных объявлений), и любых других письменных материалов, которые предполагается предоставить субъектам. 4.4.2 Вместе с другими документами исследователь/организация должны предоставить ЭСО/НЭК последнюю редакцию брошюры исследователя. Если брошюру исследователя дополняют в ходе исследования, исследователь/организация обязаны предоставить ЭСО/НЭК новую редакцию брошюры исследователя. 4.4.3 В течение исследования исследователь/организация должны предоставлять ЭСО/НЭК все подлежащие рассмотрению документы….
4.8 Информированное согласие субъектов исследования 4.8.1 При получении и документальном оформлении информированного согласия исследователь должен соблюдать нормативные требования, придерживаться GCP и этических принципов, заложенных в Хельсинкской декларации ВМА. До начала исследования исследователь должен получить письменное утверждение/одобрение ЭСО/НЭК письменной формы информированного согласия и любых других письменных материалов, предоставляемых субъектам. 4.8.2 Письменная форма информированного согласия и любые другие письменные материалы, предоставляемые субъектам, следует дополнять/исправлять по мере появления новой важной информации, которая может оказаться существенной для согласия субъекта. Любая дополненная/исправленная письменная форма информированного согласия и любые другие дополненные/исправленные письменные материалы, предоставляемые субъектам, должны быть утверждены/одобрены ЭСО/НЭК до их использования в исследовании. Субъект или его законный представитель должен быть своевременно ознакомлен с новой информацией, способной повлиять на желание субъекта продолжать участие в исследовании. Факт передачи этой информации должен быть документально оформлен. 4.8.3 Ни исследователь, ни другие занятые в исследовании лица не должны принуждать субъекта или использовать иные некорректные методы воздействия с целью склонить его к участию либо продолжению участия в исследовании. 4.8.4 Ни устная, ни письменная информация, касающаяся исследования, включая письменную форму информированного согласия, не должна содержать формулировок, прямо или косвенно склоняющих субъекта или его законного представителя отказаться от законных прав, а также формулировок, прямо или косвенно освобождающих исследователя, организацию, спонсора или их представителей от ответственности за халатность. 4.8.5 Исследователь или назначенное им лицо должно в полной мере проинформировать субъекта или, если субъект не способен дать информированное согласие, его законного представителя обо всех значимых аспектах исследования, в том числе ознакомить с письменной информацией об исследовании и одобрением/положительным заключением ЭСО/НЭК. 4.8.6 Устная и письменная информация об исследовании, включая письменную форму информированного согласия, должна содержать как можно меньше специальных терминов и быть понятна субъекту или, в соответствующих случаях, его законному представителю и незаинтересованному свидетелю. 4.8.7 Перед получением информированного согласия исследователь или назначенное им лицо должно предоставить субъекту или его законному представителю достаточное количество времени и возможность для получения более подробной информации об исследовании и принятия решения об участии в нем или отказе от такого участия. Субъект или его законный представитель должен получить исчерпывающие ответы на все вопросы об исследовании. 4.8.8 До начала участия в исследовании субъект или его законный представитель, а также лицо, проводившее разъяснительную беседу, должны подписать и собственноручно датировать письменную форму информированного согласия. 4.8.9 Если субъект или его законный представитель не способен читать, то в течение всей разъяснительной беседы должен присутствовать незаинтересованный свидетель. После того как субъекту или его законному представителю прочитали и разъяснили письменную форму информированного согласия и другие предоставля-емые субъекту письменные материалы и после того как субъект или его законный представитель дал устное согласие на участие субъекта в исследовании и, если способен, подписал и собственноручно датировал письменную форму информированного согласия, свидетель должен ее подписать и собственноручно датировать. Подписывая форму согласия, свидетель подтверждает, что информация, содержащаяся в форме согласия и всех других письменных материалах, была точно разъяснена и понята субъектом или его законным представителем и что согласие на участие в ис-следовании дано субъектом или его законным представителем добровольно. 4.8.10 Как в ходе разъяснительной беседы, так и в письменной форме информированного согласия, а также любых других письменных материалах, предоставляемых субъектам, должно быть разъяснено следующее: а) Исследование носит экспериментальный характер. б) Цель исследования. в) Варианты лечения в процессе исследования и вероятность случайного распределения в одну из групп лечения. г) Процедуры исследования, включая все инвазивные процедуры. д) Обязанности субъекта. е) Те аспекты исследования, которые носят экспериментальный характер. ж) Ожидаемый риск или неудобства для субъекта, а также, в соответствующих случаях, для эмбриона, плода или грудного ребенка. з) Ожидаемые выгода и/или польза. Если пользы с медицинской точки зрения не предполагается, то субъект должен быть поставлен об этом в известность. и) Иные, помимо предусмотренных в исследовании, процедуры или методы лечения, которые могут быть доступны субъекту, а также их значимые потенциальные выгода и/или польза, а также риск. к) Компенсация и/или лечение, доступные субъекту в случае причинения вре-да его здоровью в результате участия в исследовании. л) Планируемые выплаты субъекту за его участие в исследовании, если таковые предусмотрены. м) Планируемые расходы субъекта, если таковые ожидаются, связанные с его участием в исследовании. н) Участие субъекта в исследовании является добровольным, и он может отказаться от участия или выйти из исследования в любой момент без каких-либо санкций для себя или потери положенных выгод. о) Мониторы, аудиторы, ЭСО/НЭК и уполномоченные органы, в той мере, в какой это допускается законодательством, будут иметь прямой доступ к оригинальным медицинским записям субъекта для проверки процедур и/или данных клинического исследования, не нарушая при этом конфиденциальности данных субъекта, и что субъект или его законный представитель, подписывая письменную форму информированного согласия, дает разрешение на такой доступ. п) Записи, идентифицирующие субъекта, будут сохранены в тайне и могут быть раскрыты только в той мере, в какой это допускается законодательством. При публикации результатов исследования конфиденциальность данных субъекта будет сохранена. р) Субъект или его законный представитель будет своевременно ознакомлен с новой информацией, способной повлиять на желание субъекта продолжать участие в исследовании. с) Лица, к которым можно обратиться для получения дополнительной информации об исследовании и правах субъектов исследования, а также в случае причинения вреда здоровью субъекта в результате его участия в исследовании. т) Возможные обстоятельства и/или причины, по которым участие субъекта в исследовании может быть прекращено. у) Предполагаемая длительность участия субъекта в исследовании. ф) Приблизительное количество субъектов, которое предполагается включить в исследование. 4.8.11 Перед включением в исследование субъект или его законный представитель должен получить подписанный и датированный экземпляр письменной формы информированного согласия и все другие предоставляемые субъектам письменные материалы. Во время участия субъекта в исследовании субъект или его законный представитель должен получать подписанные и датированные экземпляры всех последующих редакций формы информированного согласия и копии всех поправок к другим письменным материалам, предоставляемым субъектам. 4.8.12 Если в клиническом исследовании (связанном либо не связанном с лечением) участвуют субъекты, которые могут быть включены в исследование только на основании согласия их законных представителей (например, несовершеннолетние, пациенты с выраженным слабоумием), то субъект должен быть проинформирован об исследовании в соответствии с его способностью понять эту информацию, и, если субъект в состоянии, он должен подписать и собственноручно датировать письменную форму информированного согласия. 4.8.13 Кроме случаев, описанных в 4.8.14, в исследование, не связанное с лечением (т.е. исследование, в котором не предполагается непосредственной с медицинской точки зрения пользы для субъекта), могут быть включены только субъекты, которые лично дают свое согласие и собственноручно подписывают и датируют письменную форму информированного согласия. 4.8.14 В исследования, не связанные с лечением, субъекты могут быть включены с согласия их законных представителей при соблюдении следующих условий: а) Цели исследования не могут быть достигнуты посредством исследования с участием субъектов, которые могут дать свое согласие лично. б) Ожидаемый риск для субъектов незначителен. в) Отрицательное воздействие на здоровье субъекта сведено к минимуму и незначительно. г) Исследование не запрещено законодательством. д) Для включения таких субъектов должно быть запрошено специальное утверждение/одобрение ЭСО/НЭК, учитывающее этот аспект. Подобные исследования (за исключением обоснованных случаев) должны проводиться с участием пациентов, имеющих заболевание, для лечения которого предназначен исследуемый продукт. Субъекты в таких исследованиях должны находиться под особо тщательным наблюдением, и их участие должно быть прекращено, если есть основания полагать, что они испытывают чрезмерный дискомфорт. 4.8.15 При неотложных состояниях, когда до включения в исследование не-возможно получить согласие самого субъекта, оно должно быть запрошено у его законного представителя, если таковой присутствует. Если предварительное согласие самого субъекта невозможно и отсутствует его законный представитель, то для включения субъекта в исследование должны быть предприняты предусмотренные протоколом и/или другими документами и утвержденные/одобренные ЭСО/НЭК меры, направленные на защиту прав, безопасности и благополучия субъекта, а также обеспечивающие соответствие нормативным требованиям. Субъект или его законный представитель должен быть в кратчайшие сроки поставлен в известность об исследовании, и у него должно быть запрошено согласие на продолжение участия в исследовании, а также другое согласие, как это положено (см. 4.8.10)…
5.11 Подтверждение рассмотрения ЭСО/НЭК 5.11.1 Спонсор должен получить от исследователя/организации: а) наименование и адрес ЭСО/НЭК исследователя/организации; б) подтверждение от ЭСО/НЭК того, что он организован и действует согласно ОСР и соответствующему законодательству; в) документально оформленное утверждение/одобрение ЭСО/НЭК и, по требованию спонсора, копию текущей версии протокола, письменной формы информированного согласия и любых других предоставляемых субъектам письменных материалов, а также описание действий по привлечению субъектов к участию в исследовании, документов, относящихся к предусмотренным для субъектов выплатам и компенсациям, и любых иных документов, которые могли быть затребованы ЭСО/НЭК. 5.11.2 Если ЭСО/НЭК обусловливает выдачу своего утверждения/одобрения внесением изменений в какие-либо аспекты исследования, например в протокол, письменную форму информированного согласия или любые иные предоставляемые субъектам письменные материалы и/или другие процедуры, спонсор должен получить от исследователя/организации копии всех измененных документов и да-ту полученного утверждения/одобрения ЭСО/НЭК. 5.11.3 Спонсор должен получить от исследователя/организации документацию и даты любых повторных утверждений/одобрений ЭСО/НЭК, а также решений об отзыве или приостановке ранее выданного утверждения/одобрения…
Федеральный закон №52-ФЗ от 30.03.1999
