
- •Основные типы химических реакций и процессов в функционировании живых систем
- •Основные типы химических реакций и процессов в функционировании живых систем
- •Содержание
- •Техника безопасности при работе в химической лаборатории Общие правила работы
- •Работа с легковоспламеняющимися, взрывоопасными и ядовитыми веществами
- •Тушение местного пожара и горящей одежды
- •Первая помощь при несчастных случаях
- •Занятие 1. Протолитические реакции. Гетерогенные реакции в растворах электролитов.
- •Основные типы химических реакций.
- •Теория кислот и оснований.
- •Константа диссоциации
- •Взаимосвязь степени диссоциации и константы диссоциации
- •Ионное произведение воды. Водородный показатель.
- •Гидролиз солей
- •Кислотность желудочного сока
- •Гетерогеннные равновесия в системе «раствор-осадок».
- •Вопросы и задачи для самоконтроля
- •Примеры решения задач
- •Тесты для самоконтроля
- •Ответы к тестам для самоконтроля
- •Занятие 2. Растворы.
- •2.1. Вода. Свойства воды как растворителя.
- •2.2. Растворы.
- •2.3. Способы выражения концентрации растворов.
- •2.4. Способы приготовления стандартных растворов.
- •2.5. Посуда, применяемая в объемном анализе.
- •Вопросы для самоконтроля
- •Примеры решения задач
- •Тесты для самоконтроля Тест № 1
- •Тест № 2
- •Тест № 3
- •Тест № 4
- •Тест № 5
- •Ответы к тестам для самоконтроля
- •Занятие 3. Коллигативные свойства растворов
- •Температуры кипения и отвердевания растворов.
- •Осмотическое давление и его измерение
- •Роль осмоса и осмотического давления в биологических системах.
- •Вопросы для самоконтроля.
- •Тесты для самоконтроля Тест 1
- •Тест 2
- •Тест 3
- •Тест 4
- •Тест 5
- •Ответы к тестам для самоконтроля
- •Занятие 4. Буферные растворы
- •Буферные растворы. Классификация буферных растворов. Механизм их действия.
- •Буферная ёмкость
- •Буферные системы организма.
- •Кислотно-основное равновесие
- •Применение реакции нейтрализации в фармакотерапии.
- •Примеры решения задач
- •Вопросы для самоконтроля
- •Лабораторные работы
- •Тесты для самоконтроля. Тест 1
- •Тест 2
- •Тест 3
- •Тест 3
- •Тест 5
- •Ответы к тестам для самоконтроля
- •Занятие 5. Реакции замещения лигандов
- •Комплексообразование в организме
- •Основные положения и понятия координационной теории.
- •Классификация и номенклатура комплексных соединений.
- •Комплексообразующая способность s-, р- и d- элементов
- •Характер химической связи в комплексных соединениях.
- •Внешнеорбитальные и внутриорбитальные комплексы
- •5.7. Представления о строении металлоферментов и других биокомплексных соединений
- •Устойчивость комплексных соединений в растворах
- •Механизм токсического действия тяжелых металлов.
- •Значение комплексных соединений в медицине.
- •Вопросы для самоконтроля
- •Упражнения
- •Лабораторные работы
- •Литература
Применение реакции нейтрализации в фармакотерапии.
Для проведения коррекции кислотно-основного состояния необходимо выявить, какое звено в его регулировке нарушено. Для этого необходимо определить значения рН биологических жидкостей и содержание буферных оснований.
В основе фармакологических действий лежит реакция нейтрализации.
Например, в качестве экстренной меры при ацидозе применяется внутривенное вливание раствора гидрокарбоната натрия 4,5%, а в острых случаях – 8,4%. Второе эффективное средство – трисамин 3,66%, который связывает избыточные протоны. Он эффективен только при внутривенном введении. Также в качестве средства, коррегирующего ацидоз, используют лактат натрия 11% раствор.
Для устранения явления алкалоза в некоторых случаях используют раствор аскорбиновой кислоты 5%. В гастроэнтерологии применяют средства, нормализующие секреторную функцию желудка. При пониженной кислотности желудочного сока назначают разбавленную соляную кислоту, при повышенной кислотности – различные антацидные препараты: оксид магния, основной карбонат магния, карбонат кальция, гидрокарбонат натрия.
Примеры решения задач
Задача 1. Рассчитать рН аммиачного буферного раствора, содержащего 0,02 М раствора NH4ОН и 0,2М раствора NH4Сl. рК(NH4ОН)=4,75,
рОН
= 4,74 +
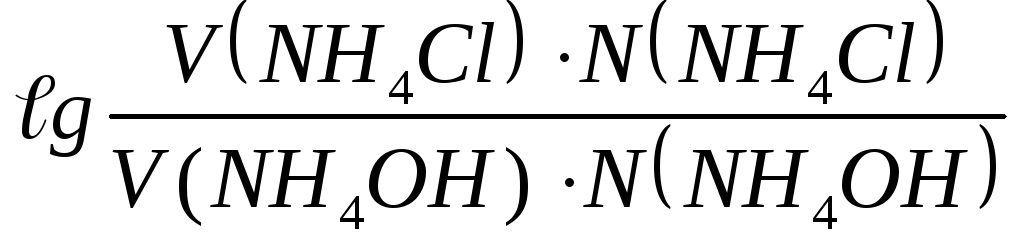
Задача 2. Можно ли приготовить аммиачный буфер с рН = 4,7, когда КД (NH4OH) = 1,8 · 10-5 ?
Решение:
1. Определяем рК NH4OH:
КД (NH4OH) = 1,8 · 10-5 рК = -ℓg КД = - ℓg 1,8 · 10-5 =
-(ℓg 1,8 - ℓg 10-5) = -0,26 = 5 = 4,74.
2. Определяем интервал буферного действия по формуле:
рОН = рК ± 1.
рОН = 4, 74 ± 1; рН = 3,74 -5,74.
Ответ: значение рОН = 4,74 входит в интервал рК 3,74 – 5,74, поэтому такой аммиачный буфер можно приготовить.
Задача 3. Для приготовления буфера взяты 70 мл 2 N р-ра NH4OH и 140 мл 0,1 N р-ра NH4С1. Как изменится рОН этого раствора, если: а) этот раствор разбавить в 10 раз, б) добавить к нему 10 мл 0,1 N р-ра NaОН ?
КД (NH4OH) = 1,8 · 10-5
Решение:
1. Определяем рК NH4OH:
рК = -ℓg КД = - ℓg 1,8 · 10-5 = 4,74 (см. предыдущую з-чу)
2. Определяем начальное значение рОН:
рОН
= 4,74 +
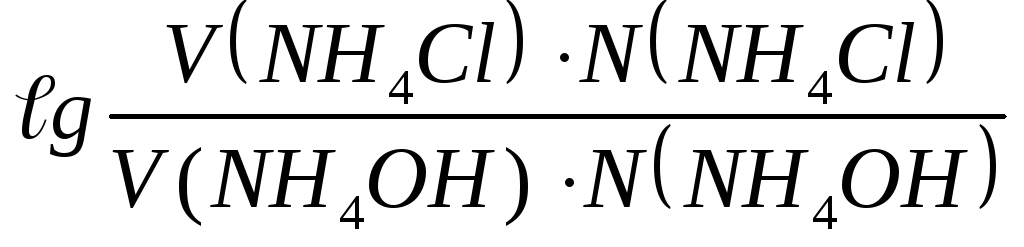
при разбавлении и добавлении NaOH
рОН=4,74+ℓg![]()
Определяем конечное значение рОНК после добавления NaOH:
рОНК
= рК +ℓg +
![]() :
:
рОНК
= 4,74 +ℓg +![]() ;
;
Определяем изменение рОН (ΔрОН): рОНН – рОНК = 3,74 – 3,66 = 0,08
Ответ: рОН не изменяется при разбавлении буфера в любое число раз, так как при этом не изменится соотношение концентраций компонентов буфера; ΔрОН = 0,08
Задача 4. Какова буферная ёмкость фосфатного буфера, если при добавлении 3 мл 0,01N раствора НС1 к 20 мл этого буфера рН меняется от 7,4 до 7,1?
Решение:
1. Определяем (ΔрН): Δ рН = рНН – рНК, Δ рН = 7,4 – 7,1 = 0,3
2. Определяем буферную ёмкость по формуле:
В
=
![]() ;
В =
;
В =![]()
Ответ: В = 0,005 мэ/л.
Вопросы для самоконтроля
Какие растворы называются буферными растворами ?
Классификация буферных растворов.
Механизм буферного действия.
Уравнение Гендерсона – Гассельбаха для определения рН и рОН протолитических буферных растворов.
Факторы, влияющие на рН и рОН буферных растворов.
Буферная ёмкость.
Зона буферного действия.
Количественное определение буферной ёмкости.
Буферные системы крови: гидрокарбонатная, фосфатная, гемоглобиновая и протеиновая.
Взаимодействие буферных систем в организме.
Кислотно-основное равновесие.
Основные показатели КОР
Возможные причины и типы нарушений КОР организма
Применение реакции нейтрализации в фармакотерапии для коррекции КОР: лекарственные средства с кислотными и основными свойствами.
