
- •Основные типы химических реакций и процессов в функционировании живых систем
- •Основные типы химических реакций и процессов в функционировании живых систем
- •Содержание
- •Техника безопасности при работе в химической лаборатории Общие правила работы
- •Работа с легковоспламеняющимися, взрывоопасными и ядовитыми веществами
- •Тушение местного пожара и горящей одежды
- •Первая помощь при несчастных случаях
- •Занятие 1. Протолитические реакции. Гетерогенные реакции в растворах электролитов.
- •Основные типы химических реакций.
- •Теория кислот и оснований.
- •Константа диссоциации
- •Взаимосвязь степени диссоциации и константы диссоциации
- •Ионное произведение воды. Водородный показатель.
- •Гидролиз солей
- •Кислотность желудочного сока
- •Гетерогеннные равновесия в системе «раствор-осадок».
- •Вопросы и задачи для самоконтроля
- •Примеры решения задач
- •Тесты для самоконтроля
- •Ответы к тестам для самоконтроля
- •Занятие 2. Растворы.
- •2.1. Вода. Свойства воды как растворителя.
- •2.2. Растворы.
- •2.3. Способы выражения концентрации растворов.
- •2.4. Способы приготовления стандартных растворов.
- •2.5. Посуда, применяемая в объемном анализе.
- •Вопросы для самоконтроля
- •Примеры решения задач
- •Тесты для самоконтроля Тест № 1
- •Тест № 2
- •Тест № 3
- •Тест № 4
- •Тест № 5
- •Ответы к тестам для самоконтроля
- •Занятие 3. Коллигативные свойства растворов
- •Температуры кипения и отвердевания растворов.
- •Осмотическое давление и его измерение
- •Роль осмоса и осмотического давления в биологических системах.
- •Вопросы для самоконтроля.
- •Тесты для самоконтроля Тест 1
- •Тест 2
- •Тест 3
- •Тест 4
- •Тест 5
- •Ответы к тестам для самоконтроля
- •Занятие 4. Буферные растворы
- •Буферные растворы. Классификация буферных растворов. Механизм их действия.
- •Буферная ёмкость
- •Буферные системы организма.
- •Кислотно-основное равновесие
- •Применение реакции нейтрализации в фармакотерапии.
- •Примеры решения задач
- •Вопросы для самоконтроля
- •Лабораторные работы
- •Тесты для самоконтроля. Тест 1
- •Тест 2
- •Тест 3
- •Тест 3
- •Тест 5
- •Ответы к тестам для самоконтроля
- •Занятие 5. Реакции замещения лигандов
- •Комплексообразование в организме
- •Основные положения и понятия координационной теории.
- •Классификация и номенклатура комплексных соединений.
- •Комплексообразующая способность s-, р- и d- элементов
- •Характер химической связи в комплексных соединениях.
- •Внешнеорбитальные и внутриорбитальные комплексы
- •5.7. Представления о строении металлоферментов и других биокомплексных соединений
- •Устойчивость комплексных соединений в растворах
- •Механизм токсического действия тяжелых металлов.
- •Значение комплексных соединений в медицине.
- •Вопросы для самоконтроля
- •Упражнения
- •Лабораторные работы
- •Литература
Вопросы для самоконтроля
Раствор как гомогенная система. Растворитель, растворённое вещество. Концентрированные и разбавленные растворы.
Количественный состав раствора как одна из главных характеристик раствора.
Роль воды и растворов в жизнедеятельности.
Физико-химические свойства воды, обуславливающие ее уникальную роль как единственного биорастворителя.
Способы выражения концентрации растворов: массовая доля вещества в растворе, молярная концентрация, молярная концентрация эквивалента (или нормальная концентрация), массовая концентрация (или титр).
Химический эквивалент, закон эквивалентов.
Эквивалентная масса вещества, её связь с молярной массой, фактор эквивалентности. Правила расчёта фактора эквивалентности для различных классов неорганических соединений.
Примеры решения задач
Задача 1.
Приготовьте 500г раствора NaCl с ω=10%.
|
Дано: m раствора (NaCl)=500г ω (NaCl)=10% |
Решение ω =m вещества·100%/ m раствора 1. Определяем массу NaCl по формуле: m вещества= ω· m раствора 100% m (NaCl)=10%·500г =50г 100г 2. Определяем массу воды по формуле: m раствора= m вещества+ m растворителя m (H2O)= m раствора- m вещества m (H2O)=500г-50г=450г. Согласно формуле ρ= m/V, где ρ- плотность раствора, m-масса, V-объем V(H2O)= m (H2O)=450г =450мл ρ (H2O) 1г/мл |
|
Найти: m (NaCl)=? m (H2O)=? |
Ответ: Для того, что бы приготовить 500г раствора NaCl с ω=10%, нужно взвесить на аналитических весах 50г NaCl, поместить в любую посуду и добавить туда 450мл воды, отмерив ее цилиндром.
Задача 2.
Приготовьте 250мл 0,5М раствора CuSO4 из безводного CuSO4 мл
|
Дано: Cм(CuSO4)=0,5М V (CuSO4)=0,25л |
Решение См=n(CuSO4)/V Находим количество молей раствора CuSO4 по формуле n(CuSO4)=См·V, тогда n(CuSO4)=0,5моль/л·0,25л=0,125моль. М(CuSO4)=160г/моль Согласно формуле n=m/M, находим массу CuSO4 m (CuSO4)= n· M=0,125моль ·160г/моль=20г |
|
Найти: m (CuSO4)=? |
Ответ: Для того, что бы приготовить 250мл CuSO4 из безводного, нужно взвесить на аналитических весах 20г CuSO4, перенести в мерную колбу объемом 250мл и довести до метки водой.
Задача 3.
Приготовьте 50мл 0,025N раствора NaOH разбавлением 1N раствора NaOH.
|
Дано:
V2(NaOH)=50 мл |
Решение
тогда
|
|
Найти: V1(NaOH)= ? |
Ответ: Для того, что бы приготовить 50 мл 0,025N раствор NaOH из 1N, нужно с помощью пипетки отобрать 1,25мл 1N раствора NaOH, перенести в мерную колбу объемом 50 мл и довести до метки водой.

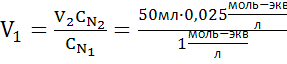 = 1,25мл
= 1,25мл