
- •I. Правила техники безопасности при работе в лаборатории
- •II. Классификация органических соединений. Номенклатура и изомерия.
- •Лабораторная работа № 1
- •Лабораторная работа № 2.
- •Предельные углеводороды.
- •Лабораторная работа № 3.
- •1.Насыщенных углеводородов.
- •2.Ненасыщенных углеводородов
- •Лабораторная работа № 5
- •Лабораторная работа № 6
- •Лабораторная работа № 7.
- •Лабораторная работа № 8.
- •Лабораторная работа № 10
- •Лабораторная работа № 11
- •Лабораторная работа № 12
- •Лабораторная работа № 13
- •Лабораторная работа № 14
- •Лабораторная работа №16
- •Лабораторная работа №17
- •Лабораторная работа №18
- •Лабораторная работа №19
- •Лабораторная работа № 20
- •Лабораторная работа № 20
- •Лабораторная работа № 21.
- •Содержание
Лабораторная работа №18
Тема: Шестичленные гетероциклы с одним гетероатомами.
Простейшим представителем этого класса является пиридин, строение которого отвечает правилу Хюккеля, поэтому он является ароматическим углеводородом. Однако, наличие гетероатома пиридинового типа обуславливает π – дефицитный характер данного гетероцикла и придает ему особенности: электрофильные частицы легко присоединяются по гетероатому, давая соли пиридиния:
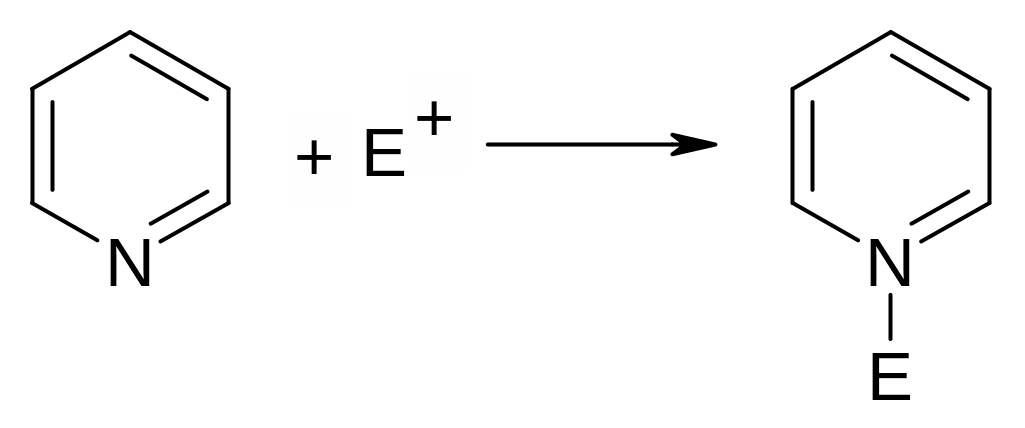
π-Дефицитность системы и легкость образования катиона пиридиния объясняет неактивность пиридина в реакциях электрофильного замещения. Как ароматическая система, пиридин устойчив к действию окислителей.
Студент должен знать:
Что пиридин ядовит и работать с ним нужно, соблюдая правила техники безопасности.
Сравнительную характеристику ароматичности бензола и пиридина.
В какое положение идут реакции электрофильного замещения в пиридине и почему?
В какое положение идут реакции нуклеофильного замещения в пиридине и почему?
Сравнительную характеристику основности пиридина и пиразола, имидазола.
Студент должен уметь:
Правильно работать с пиридином.
Записывать уравнения реакций, доказывающих основность пиридина.
Записывать уравнения реакций электрофильного и нуклеофильного замещения в пиридине.
Доказывать устойчивость пиридина к действию окислителей.
Получать четвертичные соли пиридина.
Оборудование: красная лакмусовая бумага, микроскоп.
Реактивы: пиридин, насыщенный раствор пикриновой кислоты, 0,1н.FeCI3, иодистый метил, р-р KMnO4.
Опыт 1. Растворимость пиридина в воде. К одной капле пиридина добавить 1 каплю воды – получается прозрачный раствор. Добавить ещё 4 капли воды – пиридин очень хорошо в воде. Сохранить раствор для последующих реакций.
Опыт 2. Основный характер пиридина. Узкую полоску красной лакмусовой бумажки смочить раствором пиридина – заметно слабое посинение, что соответствует нейтральной реакции на лакмус.
Переход от красного к синему у лакмуса происходит при рН 5,0-8,0.
Отчетливую реакцию, указывающую, что пиридин с водой образует основание, диссоциирующее с образованием иона ОН- , можно наблюдать с помощью полоски фильтровальной бумаги, смоченной индикатором бромтимоловым синим. Переход от жёлтого к синему этого индикатора лежит в интервале рН 6-7,6. Гидратация пиридина протекает по уравнению:
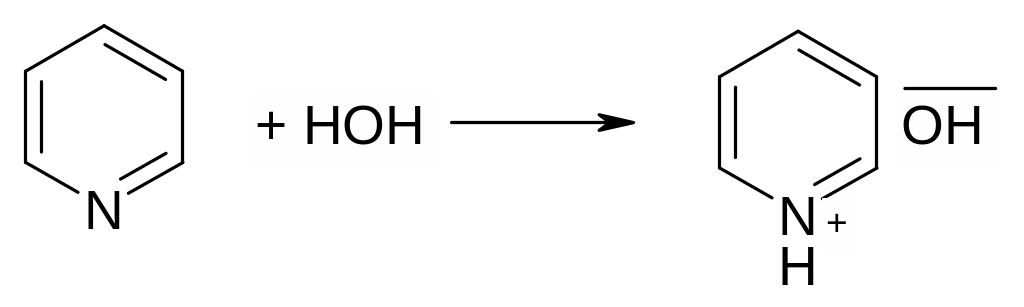
Опыт 3. Осаждение гидроксида железа (III) водным раствором пиридина. К двум каплям водного раствора пиридина добавить каплю 0,1 н. FeCl3 выпадают бурые хлопья Fe(ОН)3 с образованием легко растворимой в воде хлористоводородной соли пиридина (хлоргидрата пиридина). Образование гидроксида железа (III) подтверждает основные свойства пиридина.
Опыт 4. Образование пикрата пиридина.
К 1 капле водного р-ра пиридина добавить 3 капли насыщенного р-ра пикриновой кислоты. При встряхивании выделяются игольчатые кристаллы пикрата пиридина. В избытке пиридина кристаллы растворяются. Часть кристаллов поместить на предметное стекло и рассмотреть под микроскопом, зарисовать их в рабочем журнале. Эта реакция также подтверждает основный характер пиридина, ею пользуются для идентификации пиридина.
Опыт 5. Действие окислителей на пиридин.
Поместить в пробирку смесь равных количеств водного раствора
пиридина и перманганата калия, хорошо перемешать содержимое. Произошло ли обесцвечивание раствора? Нагреть реакционную смесь, цветраствора не меняется, что свидетельствует об устойчивости пиридина к действию окислителей.
Опыт 6. Образование четвертичной соли пиридина: к 0,5 мл безводного пиридина прилить 0,5 мл иодистого метила, хорошо перемешать. Образуется быстро кристаллизующееся желтое масло.
Объяснить, почему пиридин легко образует четвертичные соли.
Контрольные вопросы, вопросы для самостоятельной работы:
Как доказать основность пиридина?
Как доказать ароматичность пиридина?
В какое положение идут реакции электрофильного и нуклеофильного замещения в пиридине?
Как относится пиридин к действию окислителей?
Литература:
Л.Б.Дзарева Руководство к проведению лабораторных занятий по органической химии. Владикавказ, 2011
Э.Т.Оганесян Органическая химия.М. «Академия», 2011, с.329.
Под ред. Н.А.Тюкавкиной.Органическая химия. Специальный курс.– М.: Дрофа, 2008. с.6
Тестовые задания к работе №17.
Пиридин проявляет основные свойства, потому что:
является ароматическим;
относится к гетероциклическим соединениям;
реагирует с нуклеофилами.
азот имеет пару электронов;
Для пиридина по гетероатому идёт реакция:
аминирования;
солеобразования;
гидроксилирования;
бромирования;
В пиридине реакции электрофильного замещения идут в положение:
2
3
4
5
В пиридине реакции нуклеофильного замещения идут в положение:
1
2
3
4
Пиридин получают циклизацией:
этаналя и аммиака
ацетилена и сильной кислоты
ацетилены и диазометана
Атом азота в пиридине находится в состоянии гибридизации:
sp2
sp
sp3
Неподеленная пара электронов азота кольца пиридина
участвует в сопряжении с π – электронами кольца
не участвует в сопряжении с π – электронами кольца
Пиридиновый азот в цикле
облегчает реакции электрофильного замещения в кольце
затрудняет реакции электрофильного замещения в кольце
Реакции алкилирования в пиридине идут:
в кольцо
по атому азота
Продукт полного восстановления пиридина называется
а) пирролин
б) пирролидин
в) пиперидин
Ответы: 1-г; 2-б; 3-б; 4-б; 5-б; 6-а; 7- а; 8-б; 9-б; 10-в.
Занятие 22
