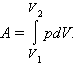- •Основы молекулярно-кинетической теории.
- •Тепловое явление. Уравнение состояния идеального газа. Изопроцессы
- •Внутренняя энергия. Термодинамика.
- •Принцип действия тепловых двигателей. Кпд теплового двигателя и его максимальное значение. Тепловые двигатели и охрана природы.
- •Испарение и конденсация. Насыщенные и ненасыщенные пары. Кипение жидкости. Зависимость температуры кипения от давления.
- •Влажность воздуха. Точка росы. Относительная влажность.
- •Деформация
- •Плавление тел. Удельная теплота плавления. Кристаллизация тел. Уравнение теплового баланса.
- •Кристаллические и аморфные тела. Свойства твердых тел.
- •Упругие деформации. Закон гука для растяжения.
- •Основы электродинамики.
- •Электрическое поле
- •Глава . Электродинамика Электрическое поле
- •Работа в электрическом поле. Потенциал
- •П pоводники в электpостатическом поле
- •Диэлектpики в электpическом поле
- •Электроемкость. Конденсаторы
- •Постоянный электрический ток. Электрический ток. Сила тока
- •Сопротивление
- •Измерение силы тока и напряжения
- •Электрические цепи. Последовательное и параллельное соединение проводников.
- •Работа и мощность постоянного тока
- •Электродвижущая сила
- •Закон ома для полной цепи
- •Электрический ток в металлах
- •Электрический ток в вакууме. Диод. Ток в вакууме.
- •Электрический ток в газах
- •Ионизация газов. Несамостоятельный газовый разряд.
- •Самостоятельный газовый разряд и его типы.
- •Электрический ток в полупроводниках
- •Магнитное поле Магнитное взаимодействие токов
- •Магнитное поле
- •Магнитное поле в веществе
- •Электромагнитная индукция. Правило Ленца.
- •Магнитные поля различной конфигурации
- •Электромагнитная индукция
- •Механические колебания и волны Механические колебания Гармонические колебания
- •Свободные колебания. Пружинный маятник.
- •Свободные колебания. Математический маятник.
- •Превращения энергии при свободных механических колебаниях
- •Механические колебания и волны Механические колебания Вынужденные колебания. Резонанс. Автоколебания
- •Механические волны.
- •Эффект Доплера .
- •Доплер-эффект широко используется в технике для измерения скоростей движущихся объектов («доплеровская локация» в акустике, оптике и радио).
- •Развитие представлений о свете.
- •Законы геометрической оптики Прямолинейность распространения света. Принцип Ферма
- •Отражение света. Плоское зеркало.
- •Сложение гармонических колебаний.
- •Метод зон Френеля.
- •Поглощение света.
- •Рассеяние света.
- •Дисперсия света. Призматический и дифракционный спектры.
- •Спектральный анализ
- •Поглощение света
- •З аконы теплового излучения. Закон Кирхгофа.
- •Инфракрасные лучи
- •Ультрафиолетовые лучи
- •Рентгеновские лучи
- •Виды и источники электромагнитных излучений
- •Применение электромагнитных излучений
- •Световые кванты. Давление света.
- •Химическое действие света
- •Процесс фотосинтеза
- •Фотография. Первые в мире снимки
- •Снимок Ньепса
- •Снимок Тальбота
- •Снимок Дагера
- •Совершенствование и развитие фотографии
- •Пpеобpазования Лоpенца
- •Релятивистская динамика
- •Современная физическая картина мира.
Внутренняя энергия. Термодинамика.
Внутренняя энергия идеального газа, способы ее изменения. Термодинамика – это наука о тепловых явлениях. В противоположность молекулярно-кинетической теории, которая делает выводы на основе представлений о молекулярном строении вещества, термодинамика исходит из наиболее общих закономерностей тепловых процессов и свойств макроскопических систем. Выводы термодинамики опираются на совокупность опытных фактов и не зависят от наших знаний о внутреннем устройстве вещества, хотя в целом ряде случаев термодинамика использует молекулярно-кинетические модели для иллюстрации своих выводов.
Термодинамика рассматривает изолированные системы тел, находящиеся в состоянии термодинамического равновесия. Это означает, что в таких системах прекратились все наблюдаемые макроскопические процессы. Важным свойством термодинамически равновесной системы является выравнивание температуры всех ее частей.
Если термодинамическая система была подвержена внешнему воздействию, то в конечном итоге она перейдет в другое равновесное состояние. Такой переход называется термодинамическим процессом. Если процесс протекает достаточно медленно (в пределе бесконечно медленно), то система в каждый момент времени оказывается близкой к равновесному состоянию. Процессы, состоящие из последовательности равновесных состояний, называются квазистатическими.
Одним из важнейших понятий термодинамики является внутренняя энергия тела. Все макроскопические тела обладают энергией, заключенной внутри самих тел. С точки зрения молекулярно-кинетической теории внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом. В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении. Внутренняя энергия идеального газа зависит только от его температуры и не зависит от объема (закон Джоуля).
Молекулярно-кинетическая теория приводит к следующему выражению для внутренней энергии одного моля идеального одноатомного газа (гелий, неон и др.), молекулы которого совершают только поступательное движение:
|
|
|
Поскольку потенциальная энергия взаимодействия молекул зависит от расстояния между ними, в общем случае внутренняя энергия U тела зависит наряду с температурой T также и от объема V:
|
U = U(T,V). |
|
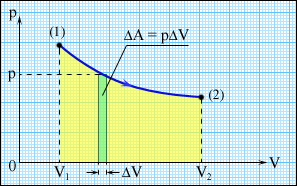
Таким образом, внутренняя энергия U тела однозначно определяется макроскопическими параметрами, характеризующими состояние тела. Она не зависит от того, каким путем было реализовано данное состояние. Принято говорить, что внутренняя энергия является функцией состояния.Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную). Например, если газ подвергается сжатию в цилиндре под поршнем, то внешние силы совершают над газом некоторую положительную работу A'. В то же время силы давления, действующие со стороны газа на поршень, совершают работу A = –A'. Если объем газа изменился на малую величину ΔV, то газ совершает работу pSΔx = pΔV, где p – давление газа, S – площадь поршня, Δx – его перемещение (рис. ). При расширении работа, совершаемая газом, положительна, при сжатии – отрицательна. В общем случае при переходе из некоторого начального состояния (1) в конечное состояние (2) работа газа выражается формулой:
|
|
|
или в пределе при ΔVi → 0:
|
|
|
|
Работа газа при расширении. |
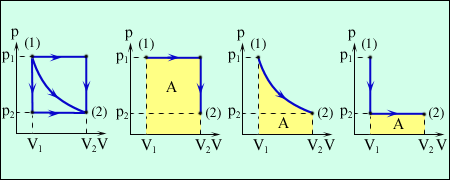
Работа численно равна площади под графиком процесса на диаграмме (p, V). Величина работы зависит от того, каким путем совершался переход из начального состояния в конечное. На рис. изображены три различных процесса, переводящих газ из состояния (1) в состояние (2). Во всех трех случаях газ совершает различную работу.
|
Три различных пути перехода из состояния (1) в состояние (2). Во всех трех случаях газ совершает разную работу, равную площади под графиком процесса. |
Процессы, изображенные на рис. можно провести и в обратном направлении; тогда работа A просто изменит знак на противоположный. Процессы такого рода, которые можно проводить в обоих направлениях, называются обратимыми.
В отличие от газа, жидкости и твердые тела мало изменяют свой объем, так что во многих случаях работой, совершаемой при расширении или сжатии, можно пренебречь. Однако, внутренняя энергия жидких и твердых тел также может изменяться в результате совершения работы. При механической обработке деталей (например, при сверлении) они нагреваются. Это означает, что изменяется их внутренняя энергия. Другим примером может служить опыт Джоуля (1843 г.) по определению механического эквивалента теплоты (рис). При вращении вертушки, погруженной в жидкость, внешние силы совершают положительную работу (A' > 0); при этом жидкость из-за наличия сил внутреннего трения нагревается, т. е. увеличивается ее внутренняя энергия. В этих двух примерах процессы не могут быть проведены в противоположном направлении. Такие процессы называются необратимыми.
Внутренняя энергия газа является функцией его абсолютной температуры.
Существуют два способа изменения внутренней энергии – теплопередача и работа.
Теплопередача – без совершения работы.
Теплопроводность – перенос тепла при взаимодействии частиц.
Конвекция – перенос тепла потоками жидкости или газа.
излучение – перенос тепла с помощью тепловых лучей
Количество теплоты, удельная теплоемкость вещества.
Количество теплоты Q – количество энергии, получаемой или отдаваемой системой при теплообмене. Передается от белее нагретых к менее нагретым телам. Для изменения температуры различных тел на одну и ту же величину требуется разное количество теплоты Q = cmT, где с – удельная теплоемкость.
![]()
Удельная теплоемкость численно равна количеству теплоты, которое необходимо сообщить одному килограмму вещества для изменения его температуры на один Кельвин.
Работа в термодинамике.
Если газ находится под поршнем массой m, площадью сечения S, то давление газа определяется атмосферным давлением и давлением поршня.
P = Pатм + mg/S
Если газ расширяется и поршень поднимается на х, то работа силы давления положительна и равна А = Fgх = PSх, т.к. Sх = V2 – V1
то А = P(V2 – V1)
В случае расширения работа газа положительна, в случае сжатия – отрицательна.
Работа силы давления при расширении газа
A = PSх
Работа внешней
силы
![]()
откуда
![]()
Работа всегда зависит от характера процесса.
Закон сохранения и превращения энергии в тепловых процессах.
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме количестве теплоты, сообщенного системе, и работы внешних сил, совершаемый над системой, т.е.
![]()
![]()
Работа внешних сил равна работе системы с обратным знаком:
откуда
![]()
Количество теплоты, сообщаемое системе, расходуется на изменение внутренней энергии системы и на совершение системой механической работы.
Адиабатный процесс.
Адиабатный процесс – процесс в какой-либо системе, который происходит без обмена теплом с окружающей средой, т.е. Q = 0. Следовательно, U = -A.
Адиабатное расширение газа сопровождается понижением его температуры, а адиабатное сжатие – повышением температуры.
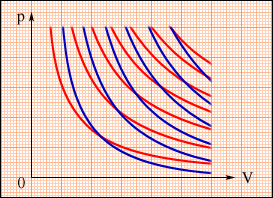
На плоскости (p, V) процесс адиабатического расширения (или сжатия) газа изображается кривой, которая называется адиабатой. При адиабатическом расширении газ совершает положительную работу (A > 0); поэтому его внутренняя энергия уменьшается (ΔU < 0). Это приводит к понижению температуры газа. Вследствие этого давление газа при адиабатическом расширении убывает быстрее, чем при изотермическом расширении (рис. ).
|
Семейства изотерм (красные кривые) и адиабат (синие кривые) идеального газа. |
В термодинамике выводится уравнение адиабатического процесса для идеального газа. В координатах (p, V) это уравнение имеет вид
|
|
|
Это соотношение
называют уравнением
Пуассона.
Здесь γ = Cp / CV
– показатель адиабаты, Cp
и CV
– теплоемкости газа в процессах с
постоянным давлением и с постоянным
объемом. Для одноатомного газа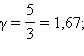 для двухатомного
для двухатомного
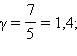 для
многоатомного
для
многоатомного
![]()
Работа газа в адиабатическом процессе просто выражается через температуры T1 и T2 начального и конечного состояний:
|
|
|
Адиабатический процесс также можно отнести к изопроцессам. В термодинамике важную роль играет физическая величина, которая называется энтропией. Изменение энтропии в каком-либо квазистатическом процессе равно приведенному теплу ΔQ / T, полученному системой. Поскольку на любом участке адиабатического процесса ΔQ = 0, энтропия в этом процессе остается неизменной.
Адиабатический процесс (так же, как и другие изопроцессы) является процессом квазистатическим. Все промежуточные состояния газа в этом процессе близки к состояниям термодинамического равновесия. Любая точка на адиабате описывает равновесное состояние.
Применение первого начала термодинамики к различным процессам.
Изотермический процесс. (T=const). Т.к. температура постоянна, то внутренняя энергия не изменяется U = 0, то Q = A, т.е. все количество теплоты сообщаемое системе, идет на совершение механической работы. Изотермический газ нагреть нельзя.
Изобарный процесс (P = const). Если Q > 0, то газ и нагревается и совершает механическую работу: Q = U + A, A = PV
Изохорный процесс (V = const). При изохорном процессе механическая работа газом не совершается, следовательно Q = U , т.е. все количество теплоты идет на изменение внутренней энергии.